Beurteilung des Substanzrisikos und Einschätzung der Ovarialfunktion – Fertilität nach zytostatischer Chemotherapie
Während des reproduktiven Lebensabschnittes werden in erster Linie folgende Tumorentitäten beobachtet: Mammakarzinom, Melanom, Zervixkarzinom, Morbus Hodgkin, Non-Hodgkin-Lymphom, Leukämien, Osteosarkom und multiples Myelom.
Prämature Ovarialinsuffizienz nach zytostatischer Chemotherapie: Die prämature Ovarialinsuffizienz (Premature Ovarian Failure = POF) ist häufig die langfristige Konsequenz einer zytostatischen Chemotherapie. Die Zytotoxizität ist bei Organen mit hohen Zellteilungsraten, wie z. B. Knochenmark, Gastrointestinaltrakt oder Thymus, weitgehend reversibel, die Ovarien hingegen weisen nicht nur eine begrenzte Zahl an Keimzellen auf, sondern charakteristisch ist außerdem die fehlende Zellregeneration, insbesondere der Eizellen.
Während sich zum Zeitpunkt der Geburt in den Ovarien insgesamt noch 1-2 Millionen Primordialfollikel finden, beträgt der Bestand zum Zeitpunkt der Pubertät nur mehr 300.000-500.000. Mit zunehmendem Lebensalter nimmt die ovarielle Reserve und damit die Wahrscheinlichkeit, schwanger zu werden, weiter kontinuierlich ab. Eine systemische Chemotherapie beschleunigt in Abhängigkeit von ihrer Zusammensetzung, Dosis und Therapiedauer den physiologischen Alterungsprozess.
Die ersten Studien, die sich mit dem Thema der Ovarialinsuffizienz nach Chemotherapie beschäftigten, wurden schon in den 1960er-Jahren durchgeführt. Seither wurden die Folgen verschiedener Chemotherapie-Schemata auf das Ovarialgewebe untersucht. Die meisten Studien betrafen Patientinnen mit Mammakarzinom, da dieses Karzinom auch in der Prämenopause das häufigste Malignom der Frau ist; fast 25% der Frauen mit Mammakarzinom sind zum Zeitpunkt der Erstdiagnose im fertilen Alter.
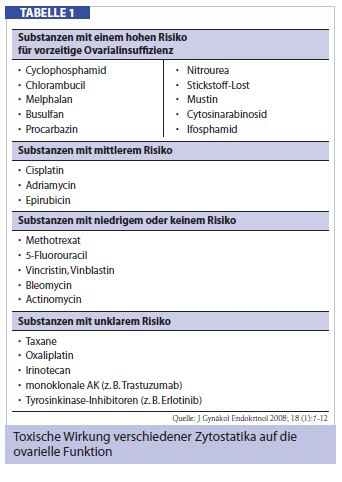
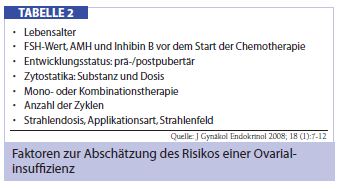
Die berichtete Inzidenz von Fällen mit prämaturer Ovarialinsuffizienz variiert entsprechend den eingesetzten Substanzen (Tab. 1). Am stärksten gonadotoxisch wirken Alkylantien. In diesem Kontext ist allerdings festzuhalten, dass die Beurteilung der Gonadotoxizität von Einzelsubstanzen schwer zu bewerten und wahrscheinlich auch wenig relevant ist, da Zytostatika zumeist in Form von Polychemotherapie-Schemata eingesetzt werden. Überdies ist das Risiko, durch Chemotherapie eine prämature Ovarialinsuffizienz zu bekommen, altersabhängig; Patientinnen über dem 40. Lebensjahr haben eine deutlich höhere Amenorrhö-Rate im Vergleich zu jüngeren Patientinnen.
Beurteilung der Ovarialfunktion nach Chemotherapie: Nach dem Abschluss einer Chemotherapie bzw. Antihormontherapie sollte mit der Beurteilung der Ovarialfunktion zumindest 2 Monate gewartet werden. Hilfreich sind biochemische Analysen, wobei das Anti-Müller-Hormon (AMH) der wahrscheinlich zuverlässigste Parameter ist. AMH wird im Gegensatz zu FSH und Inhibin B durch exogene Steroidzufuhr nur wenig oder nicht beeinflusst und stellt während des gesamten Zyklus einen mehr oder wenig stabilen Parameter dar. Der AMH-Wert ist somit ein gutes Maß für die Ovarialreserve, während FSH- und Inhibin-B-Werte lediglich Momentaufnahmen darstellen. Zur klinischen Beurteilung der Ovarialfunktion eignen sich weiters die Bestimmung von Östradiol (E2) im Serum, Ultraschalluntersuchungen der Ovarien (Darstellung von Follikeln und der antrale Follikelcount) und die sonographische Beurteilung der Endometriumdicke.