EULAR- versus GRAPPA-Empfehlungen zur Therapie der PsA
Mehr als die Hälfte aller Psoriasisarthritispatienten (PsAPatienten) leiden an einer Polyarthritis, seltener kommen asymmetrische Oligoarthritiden und Monoarthritiden vor. Aber auch die Wirbelsäule und die Sehnenansätze können bei der PsA entzündet sein, sodass es zu einem der ankylosierenden Spondylitis sehr ähnlichen Erkrankungsbild kommen kann. Typisch für die PsA ist die Beteiligung der distalen Interphalangealgelenke sowie eine Daktylitis, die klinisch durch eine wurstartige Schwellung von Fingern und/oder Zehen imponiert.
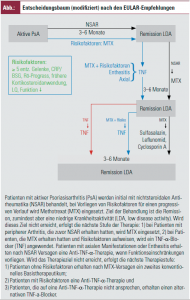
Für die Behandlung der PsA wurden in den letzten Jahren zwei wichtige internationale Richtlinien veröffentlicht: die Empfehlungen1 der „Group for Research and Assessment of Psoriasis and Psoriatic arthritis“ (GRAPPA) aus dem Jahr 2008 und die erst kürzlich (2011) publizierten Guidelines2 der „European League Against Rheumatism“ (EULAR). Während die GRAPPA-Empfehlungen vor allem allgemeine Therapieempfehlungen bzw. Richtlinien zur Erstlinientherapie beinhalten, wird in den EULAR-Guidelines ein Entscheidungsbaum dargestellt, der neben Vorschlägen zur Therapieauswahl auch ein zu erreichendes Therapieziel sowie die regelmäßige Überprüfung des Behandlungserfolgs vorsieht.
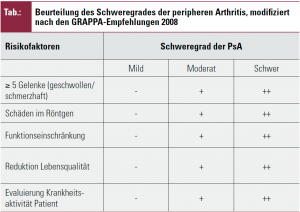
Initiale Therapieentscheidung: abhängig von Risikofaktoren für einen progressiven Verlauf
Sowohl den GRAPPA- als auch den EULAR-Empfehlungen zufolge werden bei den meisten PsA-Patienten initial nichtsteroidale Antirheumatika (NSAR) eingesetzt. Zusätzlich können Kortikosteroidinfiltrationen an einzelnen Gelenken und/oder Sehnen durchgeführt werden. Bei Vorliegen von ein oder mehreren Risikofaktoren für einen progredienten Verlauf der Erkrankung (GRAPPA und EULAR: mindestens 5 entzündete Gelenke, progrediente strukturelle Schäden, funktionelle Einschränkungen; nur EULAR: hohe Entzündungswerte, Kortikosteroidbehandlung in der Vergangenheit; nur GRAPPA: hohe Krankheitsaktivität nach Einschätzung des Patienten) sollten von Beginn an DMARD („disease modifying antirheumatic drugs“) eingesetzt werden. Patienten mit sehr schwerer Erkrankung können mit einem Tumornekrosefaktor-a-Blocker (TNF-a-Blocker) behandelt werden, auch wenn zuvor noch keine konventionelle Basistherapie angewendet wurde.
Basistherapeutikum. Die Empfehlungen in Bezug auf das einzusetzende synthetische DMARD unterscheiden sich: Während die GRAPPA lediglich den Evidenzgrad für die Wirksamkeit der DMARD Methotrexat (MTX), Sulfasalazin (SSZ), Leflunomid (Lef) und Cyclosporin A (Cyc) berichtet, die Auswahl des Basistherapeutikums aber dem behandelnden Arzt überlässt, sollte den EULAR-Richtlinien zufolge MTX als erstes DMARD eingesetzt werden. Interessanterweise stützt sich diese Empfehlung aber auf die Daten von lediglich 3 randomisierten Studien und die Extrapolation der Erfahrungen zur rheumatoiden Arthritis. Bei Kontraindikation oder Nebenwirkungen von MTX sollte ein synthetisches DMARD der zweiten Wahl eingesetzt werden.
Bei axialer Beteiligung und/oder Enthesitis sind konventionelle Basistherapeutika wenig wirksam. Hier stehen NSAR, und bei unzureichender Wirksamkeit TNF-a-Blocker zur Verfügung.
Systemische Kortikosteroide. Auch der Einsatz von systemischen Kortikosteroiden wird von der GRAPPA und von der EULAR unterschiedlich bewertet: Während die GRAPPA den Einsatz von Kortikosteroiden wegen der Gefahr der Verschlechterung der Hautsituation nach Dosisreduktion skeptisch beurteilt, sind laut EULAR nur wenige Daten (abgesehen von Fallserien) verfügbar, die eine negative Wirkung der Steroidtherapie auf die Haut belegen. Daher können Kortikosteroide als mögliche Behandlungsoption bei der PsA angesehen werden.
Ein klares Therapieziel wird nur von der EULAR formuliert. Demnach sollte durch die Behandlung eine Remission (definiert als das Fehlen von PsA-typischen Symptomen und klinischen Manifestationen) oder zumindest eine niedrige Krankheitsaktivität nach 3–6 Monaten erreicht werden, ansonsten sollte die bestehende Therapie geändert werden.
TNF-a-Blocker bei therapierefraktärer Erkrankung
Den GRAPPA-Empfehlungen zufolge ist der Einsatz einer TNFa- Blocker-Therapie bei Patienten mit moderater bis schwerer Arthritis, Spondylitis und/oder Enthesitis nach Versagen der Erstlinientherapie indiziert. Der Schweregrad wird dabei durch das Vorliegen ungünstiger Prognosefaktoren festgestellt. Ähnlich lauten auch die EULAR-Richtlinien, wonach TNF-a-Blocker nach Versagen von synthetischen DMARD bzw. bei Patienten mit axialer Erkrankung und/oder Enthesitis und funktionellen Einschränkungen nach Versagen einer NSARTherapie eingesetzt werden. Bei Patienten mit peripherer Arthritis ohne Risikofaktoren sollte zuvor ein zweites, konventionelles Basistherapeutikum versucht werden. Bei der Wahl des TNF-a-Blockers kann das Ausmaß der Hautbeteiligung eine Rolle spielen. Es gibt Hinweise, dass Etanercept zur Behandlung der psoriatischen Hautläsionen weniger effektiv ist als die monoklonalen Antikörper bzw. seine Wirkungen nur verzögert einsetzt. Allerdings fehlen noch direkte Vergleichsstudien, die diese Ergebnisse untermauern.
Kombination von Basistherapeutika und Biologika
Sowohl die GRAPPA- als auch die EULAR-Empfehlungen stellen fest, dass eine Kombination von konventionellen DMARD versucht werden kann, wenngleich diesbezüglich keine Daten aus randomisierten Studien verfügbar sind. Die bei der RA etablierte Kombination aus TNF-a-Blockern und konventionellen Basistherapeutika wird von der EULAR derzeit nicht ausdrücklich empfohlen, weil bisher nicht gezeigt wurde, dass die Kombinationstherapie wirksamer ist als die Anti-TNF-a-Monotherapie.
Zusammenfassung
Auf Grund des variablen klinischen Verlaufs der PsA ist für jeden Patienten eine individuell angepasste Therapie erforderlich. Die 2008 veröffentlichten GRAPPA-Richtlinien und die EULAR-Guidelines 2011 sind vor allem in Bezug auf die Empfehlung der Erstlinientherapie sehr ähnlich. Im Unterschied zu den GRAPPA-Richtlinien enthalten die EULAR-Guidelines aber einen Entscheidungsbaum mit empfohlenen Alternativbehandlungen, falls die vorgegebenen Therapieziele nicht in einer angemessenen Zeit erreicht werden.
1) Ritchlin CT, Kavanaugh A, Gladman DD, Mease PJ, Helliwell P, Boehncke WH et al., Treatment recommendations for psoriatic arthritis. Ann Rheum Dis 2009 Sep; 68(9):1387–94.
2) Gossec L, Smolen JS, Gaujoux-Viala C, Ash Z, Marzo-Ortega H, van der Heijde D et al., European League Against Rheumatism recommendations for the management of psoriatic arthritis with pharmacological therapies. Ann Rheum Dis 2012; 71:4–12.