KI in der gynäkoonkologischen Pathologie
Die Pathologie befindet sich derzeit in einer doppelten Transformation. Einerseits werden Glasobjektträger in digitale hochaufgelöste Whole Slide Images überführt, andererseits entstehen auf dieser digitalen Grundlage zunehmend KI-gestützte Auswerteverfahren. Diese Entwicklung ist auch für die gynäkologische Onkologie relevant, weil hier morphologische Veränderungen und therapierelevante Biomarker in hoher diagnostischer Präzision bewertet werden müssen. Digitale Pathologie ist damit nicht bloß ein Ersatz des klassischen Mikroskops, sondern die infrastrukturelle Voraussetzung für moderne computergestützte Diagnostik.1
KI als Assistenzsystem
Entscheidend ist, dass KI in der Pathologie heute vor allem als Assistenzsystem verstanden werden muss. Sie bearbeitet klar definierte, oftmals repetitive Teilaufgaben sehr gut, während die Gesamtinterpretation weiterhin in fachpathologischer Verantwortung bleibt. Diese Human-in-the-Loop-Perspektive ist nicht nur medizinisch sinnvoll, sondern derzeit auch regulatorisch notwendig. Es ist auch noch nicht selbstverständlich, dass neu entwickelte KI-Algorithmen mit allen Nuancen der histologischen Färbungen, die in Laboren existieren, sowie mit allen Scannertypen und Dateiformaten kompatibel sind – wir sprechen hier von Generalisierbarkeit. Eine Validierung im jeweiligen Labor ist daher jedenfalls erforderlich. Dies gelingt am besten durch den visuellen Vergleich der Ergebnisse durch die KI und die eigene, also menschliche fachärztliche Beurteilung. Wir verlassen uns derzeit nicht auf eine „Black-box“-Software, sondern auf eine überprüfbare Erklärbarkeit (Explainability). Die Leistungsfähigkeit und Qualität der KI-Systeme hängen stark von Trainingsdaten, Färbequalität, Scannertechnologie und Einsatzkontext ab.2
Anwendungsbereiche
Zytologie: Ein von vielen Forschungsgruppen und auch kommerziellen Firmen angestrebtes Anwendungsfeld ist die gynäkologische Zytologie. Dabei durchmustern erfahrene Zytoscreener:innen und Patholog:innen zehntausende Zellen pro Abstrich. Dieser Prozess ist mühsam, zeitaufwändig und für subjektive Fehler anfällig, wodurch die Sensitivität der Methode leidet. Bereits seit Jahrzehnten wird daher an der Automatisierung der PAP-Abstrich-Auswertung gearbeitet. Zuerst wurde Software entwickelt, die auf morphometrischen Parametern beruhte. Die Ergebnisse dieser Systeme waren vielversprechend, ein breiter Einsatz in Laboren blieb aber aus. Die heutigen Systeme setzen auf Convolutional-neural-Network-KI-Bildanalytik. Wahrscheinlich stehen wir damit an der Schwelle, KI routinemäßig in der zytologischen Diagnostik einzusetzen, um die Früherkennung weiter zu verbessern. Erste Labore in Österreich wenden solche Systeme bereits an. Voraussetzung ist allerdings die Verwendung der Dünnschichtzytologie (LBC), die in Österreich nicht überall finanziert wird, genauso wie es derzeit keine Abrechnungsmöglichkeit für den Einsatz von KI-Systemen in Österreich gibt. Die modernen KI-Zytologie-Systeme können atypische Zellen aus sehr großen Zellpopulationen herausfiltern, verdächtige Zellen priorisieren, in einer Bildgalerie gesammelt darstellen und potenziell auch automatisiert kategorisieren. Bei den meisten Systemen ist allerdings eine finale Interpretation und Beurteilung durch Zytolog:innen vorgesehen. Gerade im Screening, bei dem hohe Fallzahlen und Sensitivität zentral sind, ist diese Form der Vorselektion besonders hilfreich.3
Immunhistochemie: Für die gynäkologische Onkologie ist die Entwicklung rund um FRa beziehungsweise FOLR1 ein aktuelles und spannendes Thema. Die immunhistochemische Beurteilung wird heutzutage semiquantitativ durchgeführt und ist vor allem in Grenzfällen subjektiv interpretationsabhängig. Patholog:innen müssen beurteilen, ob mehr oder weniger als 75 % der Tumorzellen eine mäßige oder starke membranöse Expression aufweisen, und dies von Zellen mit schwacher oder keiner Expression abgrenzen. In vielen Fällen ist das einfach zu beurteilen, allerdings gibt es stark heterogene, mosaikartige Verteilungsmuster der Färbeintensität innerhalb eines Tumors. Eine multizentrische Studie zeigte zwar insgesamt eine hohe Reproduzierbarkeit der FOLR1-Bewertung, aber gerade in Borderline-Bereichen zwischen etwa 65 % und 85 % positiver Tumorzellen traten relevante Diskrepanzen auf.4 Genau hier liegt ein realistisches Einsatzfeld digitaler Quantifizierung und KI, nämlich nicht in der autonomen Entscheidung, sondern in der konsistenten Zellpositivitätsanalyse und Darstellung zur visuellen Kontrolle.
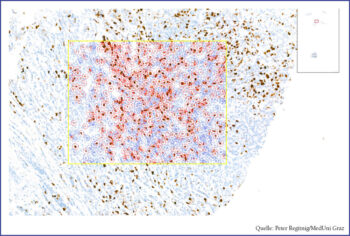
Auch die quantitative Auswertung der HER2-Immunhistochemie ist prädestiniert für KI-gestützte Bildanalytik, um die Reproduzierbarkeit zu verbessern – insbesondere in diagnostisch schwierigen Grenzbereichen wie der Unterscheidung zwischen 0 und 1+, also dort, wo therapeutische Konsequenzen zunehmend von feinen Expressionsunterschieden abhängen. In einer klinisch orientierten Studie verbesserte eine vollautomatische KI-Lösung die Konsistenz und Genauigkeit des HER2-Scorings – vor allem in der Kategorie HER2-low.5 Die Abbildung zeigt das Beispiel einer automatisierten Ki-67-Quantifizierung mittels Immunhistochemie.
Metastasendetektion: Schon recht weit fortgeschritten ist die automatisierte Detektion von Metastasen in Lymphknoten. Diese Aufgabe ist für KI gut geeignet, weil die Objektträger systematisch und ohne Ermüdung abgesucht werden. Für Patholog:innen bedeutet das eine deutliche Entlastung beim Durchmustern dieser vielen Schnittstufen und dabei, sehr kleine Tumorzellgruppen (wenige Tumorzellen) nicht zu übersehen. Für Mammakarzinom- und Zervixkarzinom-Sentinellymphknoten konnte bereits gezeigt werden, dass KI-Algorithmen eine sehr hohe Sensitivität erreichen und bei der Befundung Zeit sparen.6
Potenzieller künftiger Einsatz
Die rein morphologische Beurteilung von tumorinfiltrierenden Lymphozyten (TIL) durch Patholog:innen ist noch nicht im klinischen Alltag angelangt, ist aber ein interessanter Surrogatmarker für die Immunogenität eines Tumors und scheint eine bedeutendere Rolle als die PD-L1-Immunhistochemie zu spielen. Zugleich eröffnet eine KI-Bildanalytik zusätzliche Möglichkeiten der Analyse, die über den klassischen Prozentwert hinausgehen und durch Menschen nur sehr zeitaufwändig oder schwer erfassbar sind. In diversen Studien wurde mittlerweile nachgewiesen, dass etwa Hotspot-Identifikation und räumliche Beziehungen zwischen TIL und Tumorgewebe mehr Bedeutung haben könnten als die Auswertung von Prozentwerten der TIL. Die internationale TIL-Arbeitsgruppe weist allerdings darauf hin, dass KI-basierte TIL-Systeme im klinischen Kontext noch weiter validiert werden müssen.8
Rahmenbedingungen für den Einsatz von KI
Für Institute bedeutet die Einführung der Digitalisierung und KI-Software erhebliche Investitionen im technischen und teilweise auch im personellen Bereich. Derzeit ist die Einführung digitaler Pathologie daher ein umfassender Strukturwandel. Hinzu kommt der regulatorische Rahmen. In Europa unterliegen diagnostische In-vitro-Systeme der Verordnung (EU) 2017/746 der IVDR. Für KI in der diagnostischen Pathologie bedeutet das, dass klinisch eingesetzte Bildanalyse-Software zur Auswertung von Färbeergebnissen formal validiert sein muss. Erhebungen zeigen, dass die Zahl tatsächlich belastbar dokumentierter KI-Produkte für die digitale Pathologie bislang deutlich kleiner ist als die Zahl der technischen Prototypen. Von den Forschungserfolgen auf dem KI-Sektor bis zum Routineeinsatz liegt also noch ein beträchtlicher Weg.
Wo stehen wir heute?
KI wird in naher Zukunft in der gynäkologisch-onkologischen Pathologie weite Verbreitung finden, vor allem dort, wo Aufgaben klar umrissen, repetitiv und quantitativ zu erfassen sind, etwa bei der Immunhistochemie, der Metastasensuche im Lymphknoten oder dem zytologischen Screening. Weniger weit ist sie dort, wo komplexe Differenzialdiagnosen dominieren. Gerade deshalb ist der Begriff KI-Assistenzsystem zu unterstreichen. Für ein Fach mit steigender Komplexität und gleichzeitig knapper werdenden personellen Ressourcen ist das kein Nachteil, sondern wahrscheinlich der sinnvollste Entwicklungspfad.