Belastungsdyspnoe bei Leistungssportlerin – der Weg zurück in die Berge
Belastungsdyspnoe bei Leistungssportlerin
– der Weg zurück in die Berge
OA Dr. Christian Ebner
Interne 2 – Kardiologie, Angiologie und Interne Intensivmedizin,
Ordensklinikum Linz Elisabethinen
Mit freundlicher Unterstützung von

3500-AT-2600009, 03/2026
Anamnese und Fallbeschreibung
Alter: 40 Jahre (geb. 1985)
Geschlecht: weiblich
Vorgeschichte: Die sehr sportliche Patientin, die ihre Profikarriere im Marathon- und später Berglauf 2017 wegen eines Achillessehnenrisses beenden musste, aber weiterhin Sport wie Skitourengehen und Bergsteigen betrieb, litt seit 2022 unter intermittierendem Herzrasen.
2024 wurde zunächst eine symptomatische Rhythmusstörung – eine AV-nodale Reentry-Tachykardie – diagnostiziert und erfolgreich mit Verödung therapiert.
Erstvorstellung in der kardiologischen Ambulanz
Anfang 2025 wurde die Patientin vom niedergelassenen Kardiologen, den sie wegen zunehmender Belastungsdyspnoe (NYHA II–III) aufgesucht hatte, an unsere kardiologische Ambulanz überwiesen.
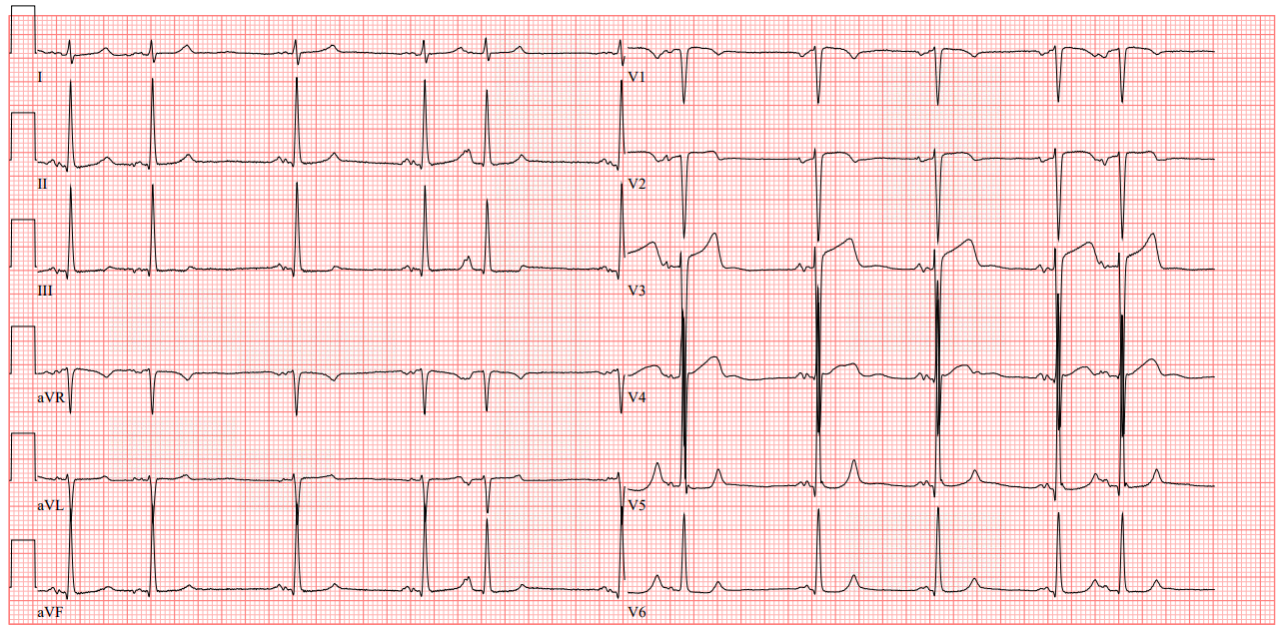
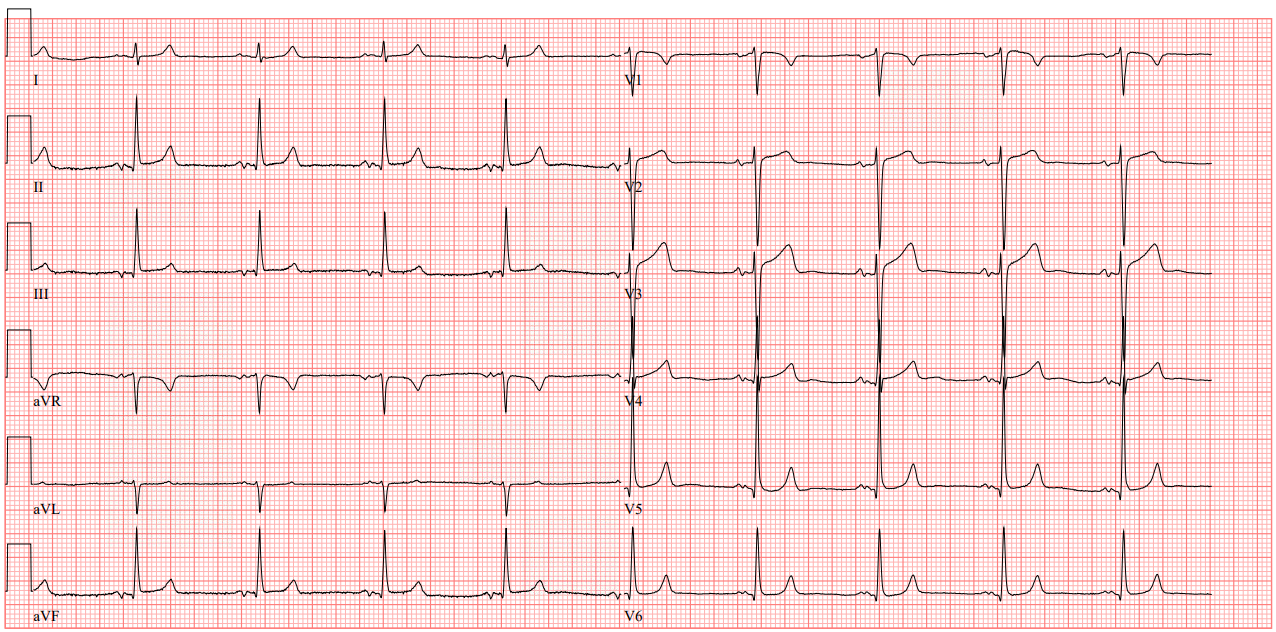
Das Elektrokardiogramm zeigte einen normfrequenten Sinusrhythmus (67/min).
Im Labor fiel der hohe NT-proBNP-Wert von 668 pg/ml auf.
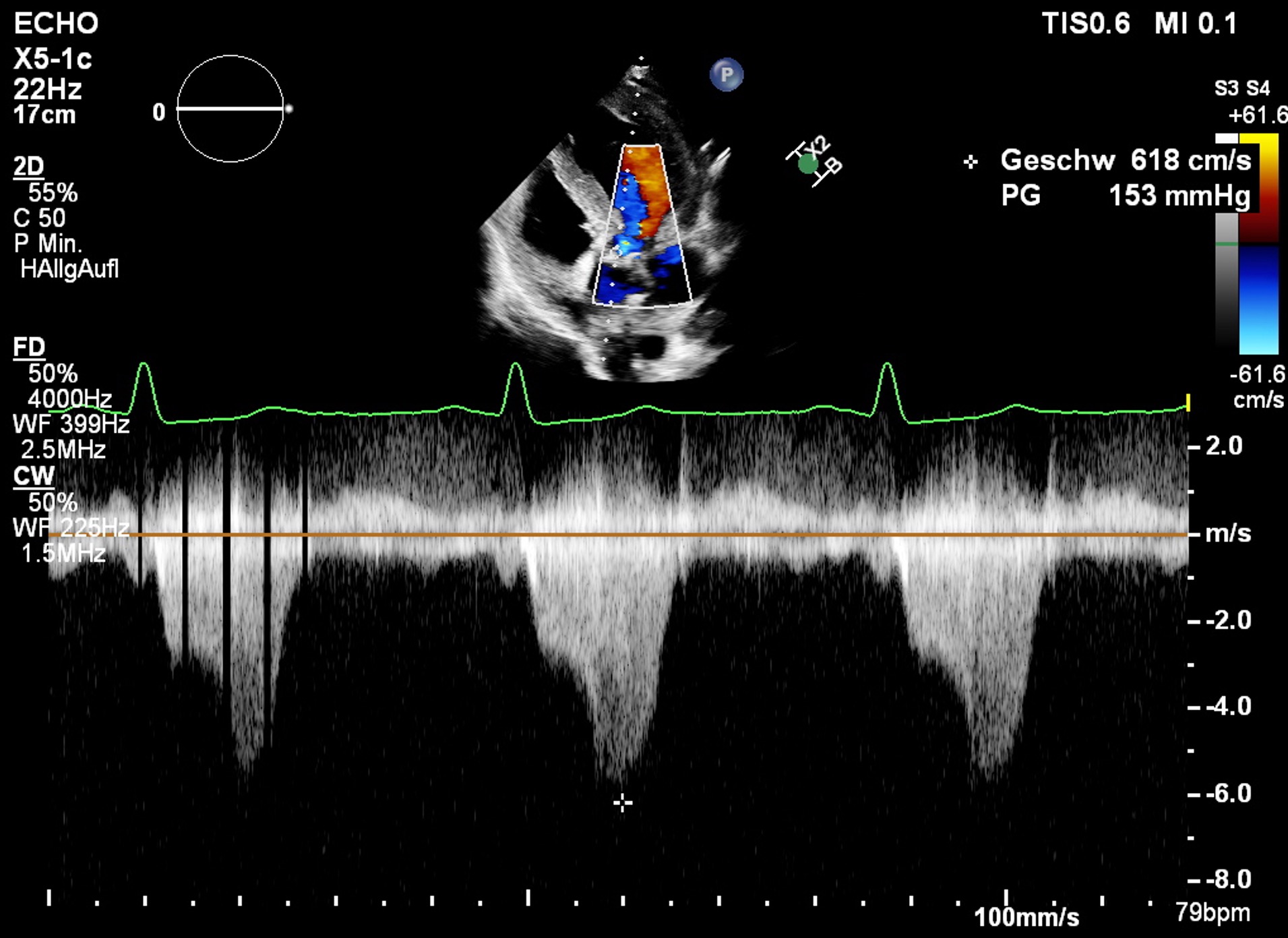
Die Echokardiografie ergab:
- basale Septumhypertrophie (16,5 mm)
- LVEF (Simpson biplan) 71 %
- hochgradige Mitralinsuffizienz (EROA 0,46 cm²)
- Gradient im LVOT in Ruhe 153 mmHg (= 6,2 m/s)
Welche Differenzialdiagnosen kommen infrage, basierend auf dem echokardiografischen Befund der Patientin? (mehrere Antworten möglich)
Diagnose
Die bildgebende Diagnostik spricht für das Vorliegen einer sarkomerischen hypertrophen Kardiomyopathie (HCM), konkret einer hypertrophen obstruktiven Kardiomyopathie (HOCM), die sich durch eine bereits in Ruhe bestehende relevante LVOT-Obstruktion auszeichnet. Daher wurde leitliniengerecht eine niedrigdosierte Betablockertherapie (Bisoprolol 1,25 mg) initiiert.
Parallel dazu erfolgte eine weiterführende Abklärung zum Ausschluss anderer Ursachen einer hypertrophen Kardiomyopathie, so konnte z. B. eine kardiale Amyloidose durch Knochenszintigrafie ausgeschlossen werden. Der Verdacht auf HOCM erhärtete sich weiter.
In der genetischen Analyse wurde im PLN-Gen eine heterozygote Variante (c.143_158delinsGC), resultierend in p.(Ile48SerextTer2), nachgewiesen. Da es sich hierbei um eine Variante unklarer Signifikanz handelt, kann derzeit kein gesicherter kausaler Zusammenhang mit der klinischen Symptomatik hergestellt werden, wenngleich pathogene PLN-Mutationen grundsätzlich mit hypertrophen Kardiomyopathien assoziiert sein können.
Welche therapeutischen Strategien stehen Ihnen im vorliegenden Fall zur Verfügung? (mehrere Antworten möglich)
Therapiestart mit Mavacamten
Nach sorgfältiger Abwägung der therapeutischen Optionen und unter Berücksichtigung des Patientenwunsches wurde die Entscheidung für eine medikamentöse Therapie mit Mavacamten getroffen.
Die Voraussetzungen für die Verschreibung von Mavacamten waren erfüllt:
- Vortherapie mit Nichtdihydropyridin-Kalziumantagonist oder Betablocker
- NYHA III
- LVOT-Gradient in Ruhe ≥ 50 mmHg
- LVEF ≥ 50 %
Zur Wahl der initialen Dosierung ist vor Therapiebeginn eine Bestimmung des CYP-Status erforderlich. Bei langsamen CYP2C19-Metabolisierern muss mit 2,5 mg Mavacamten begonnen werden, um eine zu hohe Exposition zu verhindern. Unsere Patientin erhielt entsprechend ihrem CYP2C19-Metabolisierer-Phänotyp („schnell“) die empfohlene Anfangsdosis von 1-mal täglich 5 mg (Bisoprolol wurde weitergeführt). Therapiestart war im März 2025.
Zu welcher Substanzklasse gehört Mavacamten?
Therapieverlauf
Nach erfolgter Dosisfindung (durch schrittweise Titration im Abstand von 4 Wochen anhand von LVOT‑Gradient und LVEF) wird der weitere Therapieverlauf mit Echokardiografie je nach LVEF alle 3–6 Monate evaluiert.
Klinik: Unter Mavacamten kam es zu einer raschen und deutlichen klinischen Besserung mit Rückgang der Belastungssymptomatik von NYHA-Stadium III auf NYHA-Stadium I. Die Patientin berichtete schon ab der ersten Verlaufskontrolle von unternommenen Skitouren und Bergwanderungen.
Labor: Das NT-proBNP normalisierte sich sukzessive.
Bildgebung: In der Echokardiografie zeigt sich eine deutliche Abnahme des LVOT-Gradienten in Ruhe sowie auch unter Belastung. Die Mitralinsuffizienz war rückläufig.
Im vorliegenden Fall konnte die Behandlung mit Mavacamten 5 mg, basierend auf den LVEF- und LVOT-Werten bei den Kontrolluntersuchungen, fortgeführt werden.
Wichtige Parameter im Verlauf
| vor Therapiebeginn | nach 1 Monat | nach 2 Monaten | nach 5 Monaten | nach 11 Monaten | |
|---|---|---|---|---|---|
| NYHA-Klasse | NYHA III | NYHA I | NYHA I | NYHA I | NYHA I |
| NT-proBNP | 668 pg/ml | 223 pg/ml | 134 pg/ml | 75 pg/ml | 119 pg/ml |
| LVOT (Ruhe) | 105 mmHg | 15 mmHg | 10 mmHg | 11 mmHg | 8 mmHg |
| LVOT (Belastung) | – | 21 mmHg | 33 mmHg | 25 mmHg | 24 mmHg |
| EROA | 0,46 cm2 | – | 0,15 cm2 | – | 0,18 cm2 |
Letzte Verlaufskontrolle
Klinik: Bei der vorläufig letzten Verlaufskontrolle, 11 Monate nach Therapiebeginn, präsentierte sich die Patientin beschwerdefrei und unter Alltagsbedingungen vollständig kompensiert. Wandern, einschließlich längerer Bergtouren, war problemlos möglich. Es bestanden keinerlei kardiale Symptome, insbesondere keine peripheren Ödeme, keine Angina Pectoris, keine Vertigo oder Synkopen sowie keine Palpitationen oder Episoden von Herzrasen. Die Patientin befand sich weiterhin im NYHA-Stadium I.
Labor: Das NT-proBNP lag mit 119 pg/ml im Normbereich.
Echo: Ein LVOT-Gradient von 8 mmHg in Ruhe und 24 mmHg unter Belastung spricht für eine aktuell nichtrelevante Ausflussbehinderung und damit für eine hämodynamisch günstige Situation. Die Mitralinsuffizienz war nur noch mild bis mäßig ausgeprägt (EROA = 0,18 cm2).
Fazit
Bei der vorgestellten Patientin konnte die hypertrophe obstruktive Kardiomyopathie durch Mavacamten sowohl klinisch als auch echokardiografisch rasch stabilisiert werden. Sie ist unter Erhaltungstherapie (Mavacamten 5 mg + Bisoprolol 1,25 mg) nach wie vor beschwerdefrei, bei gleichzeitig guter Verträglichkeit, und wird alle 6 Monate untersucht.

„Unter Therapie mit Mavacamten besserte sich die Beschwerdesymptomatik der Patientin rasch und nachhaltig. Im Sommer – 5 Monate nach Therapiebeginn – berichtete sie mir freudig und stolz von einer ausgedehnten Wanderung von Hinterstoder auf den Großen Priel und die Spitzmauer. Dies stellt eine beeindruckende körperliche Leistung dar und bedeutet für die Patientin einen erheblichen Gewinn an Lebensqualität, da sie ihrem Hobby wieder uneingeschränkt nachgehen kann.“
OA Dr. Christian Ebner
Bereitgestellt von:
OA Dr. Christian Ebner
Interne 2 – Kardiologie, Angiologie und Interne Intensivmedizin, Ordensklinikum Linz Elisabethinen
Redaktion:
Illustrationen © MedMedia/KI-generiert
- Camzyos® – Fachkurzinformation
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen siehe Abschnitt 4.8. der Fachinformation.
Bezeichnung des Arzneimittels: CAMZYOS 2,5 mg, 5 mg, 10 mg, 15 mg Hartkapseln. Pharmakotherapeutische Gruppe: Herztherapie, Andere Herzmittel, ATC-Code: C01EB24. Qualitative und quantitative Zusammensetzung: Jede Hartkapsel enthält 2,5 mg bzw. 5 mg bzw. 10 mg bzw. 15 mg Mavacamten. Sonstige Bestandteile: Kapselinhalt: Siliciumdioxid-Hydrat, Mannitol (Ph.Eur.)(E421), Hypromellose (E464), Croscarmellose-Natrium (E468), Magnesiumstearat (Ph.Eur.). Kapselhülle: Gelatine, Titandioxid (E171); 2,5 + 15 mg Hartkapseln: Eisen(II,III)-oxid (E172); 2,5 + 10 mg Hartkapseln: Eisen(III)-oxid (E172); 5 mg Hartkapseln: Eisen(III)-hydroxid-oxid x H2O (E172). Drucktinte: Eisen(II,III)-oxid (E172), Schellack (E904), Propylenglycol (E1520), Konzentrierte Ammoniaklösung (E527), Kaliumhydroxid (E525). Anwendungsgebiete: CAMZYOS wird angewendet bei erwachsenen Patienten zur Behandlung der symptomatischen (New York Heart Association Klassifizierung, NYHA, Klasse II–III) hypertrophen obstruktiven Kardiomyopathie (HOCM) (siehe Abschnitt 5.1 der Fachinformation). Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 der Fachinformation genannten sonstigen Bestandteile. Während der Schwangerschaft und bei gebärfähigen Frauen, die keine zuverlässige Empfängnisverhütung anwenden (siehe Abschnitte 4.4 und 4.6 der Fachinformation). Gleichzeitige Behandlung mit starken CYP3A4-Inhibitoren bei Patienten mit CYP2C19-Metabolisierer-Phänotyp „langsam” und nicht bestimmtem CYP2C19-Phänotyp (siehe Abschnitte 4.2, 4.4 und 4.5 der Fachinformation). Gleichzeitige Behandlung mit der Kombination aus einem starken CYP2C19-Inhibitor und einem starken CYP3A4-Inhibitor (siehe Abschnitt 4.5 der Fachinformation). Inhaber der Zulassung: Bristol-Myers Squibb Pharma EEIG, Plaza 254, Blanchardstown Corporate Park 2, Dublin 15, D15 T867, Irland. Kontakt in Österreich: Bristol-Myers Squibb GesmbH, Wien, Tel. +43 1 60143-0.Verschreibungspflicht/Apothekenpflicht: Rezept- und apothekenpflichtig.
Stand: 12/2024
Weitere Angaben, insbesondere zu Warnhinweisen und Vorsichtsmaßnahmen für die Anwendung, Wechselwirkungen mit anderen Mitteln oder sonstige Wechselwirkungen, Schwangerschaft und Stillzeit sowie Nebenwirkungen sind der veröffentlichten Fachinformation zu entnehmen.
 Autor: OA Dr. Christian Ebner
Autor: OA Dr. Christian Ebner
- Interne 2 – Kardiologie, Angiologie und Interne Intensivmedizin, Ordensklinikum Linz Elisabethinen