Rilzabrutinib bei refraktärer Immunthrombozytopenie
Rilzabrutinib bei refraktärer Immunthrombozytopenie
OA Dr. Michael Fillitz
3. Medizinische Abteilung, Hämatologie und Onkologie,
Mein Hanusch-Krankenhaus der ÖGK, Wien
Mit freundlicher Unterstützung von

MAT-AT-2600019 1.0 01/2026
Fallbeschreibung
Alter: 61 Jahre
Geschlecht: weiblich
Vorgeschichte: Im Oktober 2017 bestand ein respiratorischer Infekt, in dessen Zuge die Thrombozytopenie erstmals aufgefallen war. Im November 2017 erfolgte über den niedergelassenen Internisten die Zuweisung der Patientin an eine der hämatologischen Expositurambulanzen in einem Gesundheitszentrum der ÖGK zur Abklärung der neu aufgetretenen isolierten Thrombozytopenie (Hämoglobin: 13,1 g/dl, Thrombozyten: 61 G/l, Leukozyten: 4,1 G/l; Differenzialblutbild unauffällig).
Dauermedikation: Budesonid, Formoterolfumarat-Dihydrat 160/4,5 µg 2-mal 1 , Cal-D-Vita-Tbl. 2-mal 1, Dekristolvit®-D3-4000-I.E.-Tbl. 1-mal 1 jeden 2. Tag, Atorvacor® 10 mg 1-mal 1
Nebendiagnosen: COPD, Asthma bronchiale bekannt, Hyperlipidämie
Familienanamnese: unauffällig
- Allgemeiner Status:
Altersgemäß unauffälliger klinischer Status, keine spezifischen Beschwerden. Klinisch liegen zum Zeitpunkt der Erstvorstellung an der hämatologischen Ambulanz keine Blutungszeichen und kein Hinweis auf eine Infektion vor. - Spezifische Untersuchung:
Eine Citrat-/EDTA-Pseudothrombozytopenie wurde ausgeschlossen. Aufgrund des sich aus der Knochenmarkbiopsie ergebenden Verdachtes auf morphologische Veränderungen im Sinne eines myelodysplastischen Syndroms erfolgte eine Untersuchung auf das Vorliegen von thrombozytenreaktiven Antikörpern.
Befunde
Thrombozytenreaktive Antikörper:
Es zeigte sich eine Antikörperbeladung (IgG) der Thrombozyten mit Anti-GP-IIb/IIIa- und Ib/IX-Antikörpern – passend zur Diagnose einer Immunthrombozytopenie.
Labor:
- Blutbild und Differenzialblutbild bis auf die Thrombozytopenie unauffällig, Blutausstrich: keine Auffälligkeiten
- CRP, LDH, Bilirubin unauffällig, Infektserologie unauffällig; Autoimmunscreening: ANA-Titer = 1 : 80; nukleolär, zytoplasmatische Fluoreszenz, Antikörper gegen Trennzone (Midbody); ds-DNA-AK = 41,4 (Nb.)
- Schilddrüsen-Antikörper, ANCA, CCP-, Antiphospholipid-Antikörper und Lupus-Antikoagulans: negativ
- Serologische Gerinnung: unauffällig
- Coombs-Test direkt und indirekt: negativ
- Infektionsscreening (Hepatitis B + C, HIV, TPHA, HLO-Ag/-AK, CMV, EBV): negativ
Bildgebung:
Eine bildgebende Durchuntersuchung mittels Sonografie des Abdomens, der peripheren Lymphknotenstationen und ein Thorax-Röntgen waren unauffällig.
Histologie:
- Am 30. 11. 2017 erfolgte eine Beckenkammpunktion. In der zytologischen Aufarbeitung wurden diskrete Dysplasiezeichen in der Granulozytopoese beschrieben. Folglich bestand zunächst der Verdacht auf ein myelodysplastisches Syndrom/„single lineage dysplasia“ (MDS/SLD).
- Die histologische Aufarbeitung ergab jedoch weitgehend altersentsprechendes Knochenmark ohne konkreten Hinweis auf eine hämatologische Systemerkrankung. Somit wurde eine Autoimmunthrombozytopenie als Ursache der Thrombozytenverminderung angenommen (Ausschlussdiagnose).
- Die zytogenetische Untersuchung des Knochenmarks ergab keine Auffälligkeiten.
Ist eine Untersuchung auf das Vorliegen antithrombozytärer Antikörper bei vermuteter Immunthrombozytopenie (ITP) immer zur Diagnosestellung erforderlich? (2 richtige Antworten)
Diagnose
Nach Nachweis einer Antikörperbeladung der Thrombozyten mit Anti-GP-IIb/IIIa- und Ib/IX-Antikörpern und dem histologischen Befund wird folgende Diagnose gestellt:
Immunthrombozytopenie, kortisonsensibel
Im weiteren Verlauf zeigt sich ein insuffizientes anhaltendes Ansprechen auf konventionelle Behandlung der ITP mit intravenösen Immunglobulinen (IVIG), Kortikosteroiden (Prednisolon) und Thrombopoietin-Rezeptor-Agonisten (TPO-RA).
Trotz Refraktärität werden eine therapeutische Splenektomie und Immuntherapie mit dem Anti-CD20-Antikörper Rituximab mehrfach abgelehnt.
Staging: Eine anhaltende Remission der Thrombozytopenie (T > 100 G/l) war bei Unterschreiten einer Prednisolon-Dosis von 7,5 mg/d nicht zu halten, trotz gleichzeitig laufender TPO-RA-Therapie.
Welche Therapeutika werden in der Erstlinientherapie der ITP laut Empfehlungen eingesetzt? (1 richtige Antwort)
Therapie
-
2018Zunächst erfolgten lediglich therapiefreie Verlaufskontrollen. Die T-Werte lagen zwischen 60 G/l und 74 G/l, weshalb bei Fehlen von Blutungszeichen noch keine spezifische Therapie eingeleitet wurde.
-
März 2018Beginn mit Prednisolon
- Am 29. 3. 2018 kam es jedoch zum Abfall auf T = 24 G/l. Gleichzeitig zeigten sich gelenknahe Hämatome und Petechien an den Unterarmen, der Bauchhaut und den Unterschenkeln. Somit wurde zunächst Prednisolon 75 mg p. o. tägl. verabreicht.
- Im Blutbild vom 1. 4. 2018 zeigte sich kurzfristig ein promptes T-Ansprechen: T = 71 G/l.
- Kontrolle am 4. 4. 2018: T = 144 G/l. Prednisolon 50 mg/d wird bis zum 12. 4. 2018 fortgesetzt: kein Infekt, kein „wet bleeding“, mäßige Hämatomneigung, Fatigue, T = 103 G/l. Somit wurde die Prednisolon-Dosis schrittweise reduziert.
- Schon am 25. 4. 2018 kam es jedoch zu einem erneuten T-Abfall = 37 G/l.
- In weiterer Folge traten nach vorrübergehender Dosiseskalation und repetitivem IVIG-Rescue immer wieder krisenhafte Thrombozytopenien unter 10 G/l mit Blutungszeichen vor allem an Haut, Mundschleimhaut und gelegentlicher Epistaxis ohne eindeutige (infektiöse) Trigger auf.
- Darauf erfolgte reaktiv die Gabe von Rescue-Medikation je nach klinischem Erfordernis: IVIG, Prednisolon-Eskalation. Die T-Werte schwankten daher stark zwischen 3 G/l und 200 G/l.
-
Mai 2018Beginn mit Eltrombopag
- Da kein stabiles Ansprechen (Ziel: T > 30‒100 G/l) erreicht werden konnte, wurde am 29. 5. 2018 mit TPO-RA/Eltrombopag 50 mg/d unter Beibehaltung der Prednisolon-Dosis von 12,5 mg/d begonnen.
- Zunächst kam es hierunter am 13. 6. 2018 zu einem guten Anstieg der T auf 122 G/l, worauf Prednisolon auf 5 mg/d reduziert werden konnte. Die T lagen nun in weiterer Folge stabil zwischen 37 G/l und 52 G/l.
- Bis 17. 7. 2018 konnten so T= 241 G/l erreicht werden.
- Nachdem am 22. 8. 2018 sogar die Thrombozytenzahl auf T = 415 G/l anstieg, wurden Eltrombopag (zuletzt 25 mg/d) und Prednisolon weiter reduziert.
- Bis 9. 10. 2018 konnten die T > 100 G/l gehalten werden.
- Am 6. 11. 2018 kam es dann erneut zu einem Thrombozytenabfall mit T = 8 G/l und ausgedehnten Mundschleimhautblutungen bei afebrilem respiratorischem Banalinfekt mit Husten und Schnupfen. Nun wurde zunächst die Therapie mit Prednisolon auf 75 mg/d erhöht. Eltrombopag wurde weiter bei 25 mg/d belassen.
-
November 2018Eltrombopag wird pausiert; Splenektomie und Rituximab werden von Patientin abgelehnt.
- Am 14. 11. 2018 musste bei T = 737 G/l nun Eltrombopag pausiert werden. Leider kam es nach Wiederaufnahme des TPO-RA trotz Dosiserhöhungen in der Folge dennoch immer wieder zu einem krisenhaften Abfall der T-Zell-Zahl unter 30 G/l mit entsprechenden Blutungszeichen, die immer wieder IVIG- und Steroid-Rescue additiv zur weiterlaufenden Eltrombopag-Therapie erforderten. Eine therapeutische Splenektomie und Umstieg auf eine Anti-CD20-Therapie mit Rituximab wurden zu diesem Zeitpunkt von der Patientin abgelehnt.
-
bis Dezember 2019Bis zu diesem Zeitpunkt erfolgte die Betreuung auswärts an einer der Expositurambulanzen. Zur Prüfung eines eventuell möglichen Einschlusses in eine laufende Therapiestudie wurde die Patientin an das Zentrum übernommen, wo sie bis zum heutigen Tag in Betreuung verbleibt.
-
Dezember 2019Fortsetzung mit Eltrombopag
- Zunächst wurde die Behandlung mit Eltrombopag 75 mg/d und wechselnd dosiertem Steroid bei weitestgehend stabilen Thrombozytenzellzahlen > 100 G/l fortgesetzt. Nur gelegentlich kam es, offenbar immer infektgetriggert, zu einem passageren Thrombozytenabfall < 30 G/l, der jedoch in der Regel keine Modifikation der laufenden Therapie erforderte.
- Vereinzelte T-Abfälle < 20 G/l wurden additiv mit IVIG kupiert, auf welche die Patientin stets gut ansprach.
-
Februar 2020
bis Juni 2023Auch während der COVID-19-Pandemie kam es gehäuft zu solchen Thrombozytenabfällen, die auf medikamentöse Intervention nur verzögert ansprachen. Diese waren jedoch weder mit bedrohlichen Blutungszeichen noch mit einer SARS-CoV-2-Infektion bzw. mit der mehrfach durchgeführten Vakzinierung gegen dieses Virus assoziiert. -
Mai 2021Einschluss in Studie mit Efgartigimod
- 05/2021: Die Patientin wurde bei T = 22 G/l in eine doppelblinde, randomisierte Therapiestudie mit dem neonatalen Fc-Rezeptor-Blocker Efgartigimod alfa vs. Placebo eingeschlossen. In den folgenden 24 Wochen änderte sich jedoch nichts an der Gesamtsituation. Die schwankenden Thrombozytenzahlen (T = 8‒226 G/l) waren auf entsprechende medikamentöse Dosisveränderungen der Steroidmedikation bzw. additive IVIG-Gaben (Rescue) zurückzuführen. Eltrombopag wurde durchgehend mit 75 mg/d verabreicht. Ein auf die Studienmedikation zurückzuführender Thrombozytenanstieg konnte nicht festgestellt werden.
- Ab 27. 10. 2021 wurde Efgartigimod alfa als Open-Label-Medikation fortgesetzt. Leider kam es auch hierbei zu keinem Anstieg bzw. keiner nachhaltigen Stabilisierung der Thrombozytenzahlen.
- Somit wurde die Open-Label-Behandlung mit Efgartigimod alfa am 16. 2. 2022 beendet und ein TPO-RA-Switch von Eltrombopag p. o. auf Romiplostim s. c. vorgenommen.
-
März 2022Switch auf Romiplostim
- Ab 4. 3. 2022 wurde das TPO-RA Romiplostim s. c. in der Dosis von 7 µg/kg KG (= 500 µg absolut), in weiterer Folge mit 750 µg absolut (ca. 10 µg/kg KG s. c., KG: 70 kg) verabreicht. So wurde am 23. 3. 2022 T = 55 G/l erreicht.
- Doch schon am 13. 4. 2022 fielen die Thrombozyten auch nach dem Wechsel des TPO-RA erneut auf T = 10 G/l ab.
-
Mai 2022Biopsie: Aufgrund der Therapierefraktärität erfolgte erneut eine Knochenmarkbiopsie. In der histologischen und zytomorphologischen Beurteilung zeigte sich ein hyperzelluläres Knochenmark mit gesteigerter Granulozytopoese, verminderter Erythrozytopoese mit nur diskreten Dysplasiezeichen, gesteigerter Megakaryozytopoese mit in Clustern liegenden atypischen Megakaryozyten und mäßiggradiger Fibrose. Die Blastenzahl lag im Normbereich. Zytogenetisch wurden keine Auffälligkeiten festgestellt.
-
Juni 2022
-
Wiedereinstellung auf Eltrombopag 75 mg/d.
- Knochendichteröntgen: Aufgrund der nun schon lange andauernden, nichtausschleichbaren Prednisolon-Therapie (unterhalb der Cushing-Schwellendosis von 6,5 mg/d stets krisenhafter T-Abfall < 10‒0 G/l) wurde ein Knochendichteröntgen veranlasst. Der Befund vom 24. 5. 2022 ergab das Vorliegen einer Osteopenie (LWS unauffällig; Hüfte links: 71 % des Sollwertes, Risikoklasse B1).
- Die Patientin stimmte einem Therapiewechsel auf Rituximab oder einer therapeutischen Splenektomie wegen der zuvor gehäuften Infektionen abermals nicht zu.
-
Juni 2023Die Patientin wurde für die damals laufende Studie LUNA 3 mit Rilzabrutinib gescreent. Leider konnte sie nicht in die Studie eingeschlossen werden, da die Thrombozytenzellzahl nicht ohne medikamentöse Interventionen und Dosismodifikationen stabil gehalten werden konnte.
Ein alternativer Therapieversuch mit Fostamatinib konnte aufgrund der fehlenden Verfügbarkeit des Präparates in Österreich ebenso nicht erfolgen.
Mit der Patientin wurden alle anderen aus unserer Sicht sinnhaften Optionen besprochen:
- Milzentfernung (abgelehnt)
- Dosiserhöhung Eltrombopag bzw. erneuter Umstellungsversuch auf Avatrombopag
- Einschluss in eine Rezidivstudie an einem anderen Zentrum mit dem BAFF-Inhibitor Ianalumab
- Fostamatinib, wenn doch irgendwie verfügbar
-
Oktober 2023
-
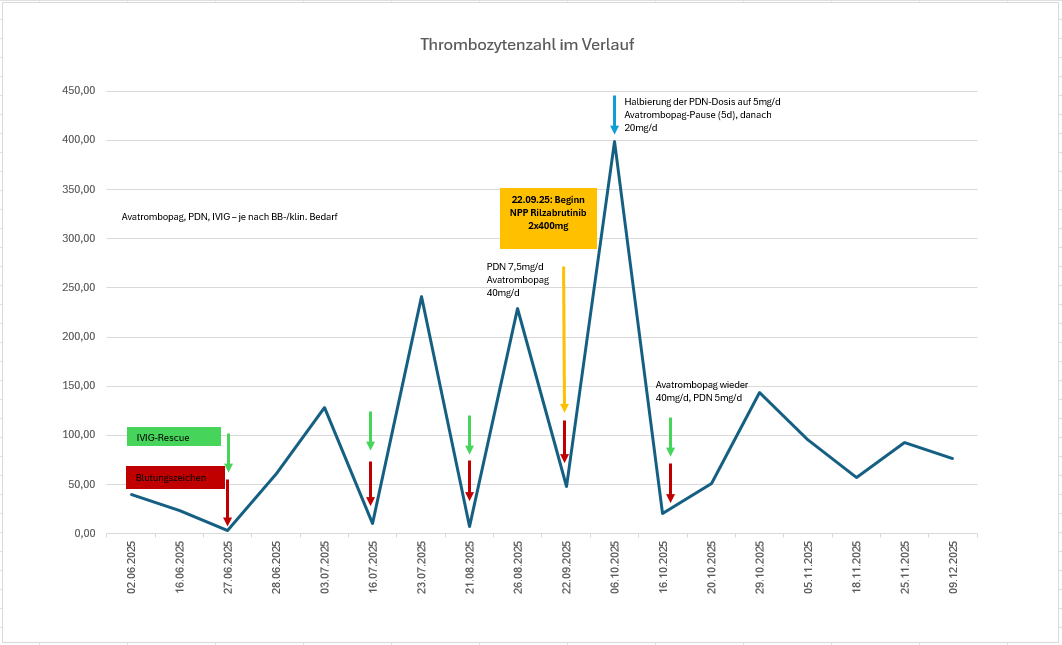
August 2025Am 21. 8. 2025 wurde die Patientin erneut mit T = 8,0 G/l und Blutungszeichen an Haut und Schleimhäuten vorstellig. Nach Rescue-Medikation (Erhöhung der Steroiddosis und IVIG-Gabe) erreichte die Patientin am 22. 9. 2025 nur T = 48 G/l.
Welche Thrombopoietin-Rezeptor-Agonisten (TPO-RA) sind in Österreich zugelassen und erhältlich? (3 richtige Antworten)
Einstellung auf BTK-Inhibitor Rilzabrutinib
-
September 2025Individueller Heilversuch mit Rilzabrutinib
Nach Rücksprache mit der Herstellerfirma und Aufklärung der Patientin konnte über einen individuellen Heilversuch (Name Patient Use, NPU) Rilzabrutinib 2-mal 400 mg/d additiv zur laufenden Therapie verabreicht werden (Tag 1 = 24. 9. 2025).
Avatrombopag verblieb zunächst auf 40 mg/d weiter, die Prednisolongabe auf 7,5 mg/d. -
Oktober 2025Schon am 6. 10. 2025 (Tag 13) stieg die Thrombozytenzahl auf 399 G/l an. Nach 5-tägiger Pausierung der parallel laufenden Avatrombopag-Therapie mit 40 mg/d wurde dessen Dosis auf 20 mg/d ab 11. 10. 2025 reduziert.
Prednison wurde ab 6. 10. 2025 von 7,5 mg/d auf letztlich 2,5 mg/d reduziert.
Am 16. 10. 2025 kam es nochmals zu einem Thrombozytenabfall auf T = 21 G/l bei jedoch nur milden Blutungszeichen (orale Petechien). Avatrombopag wurde nun wieder auf 40 mg/d gesteigert. Rilzabrutinib wurde weiterhin 2-mal tägl. mit 400 mg verabreicht. Nun kam es sukzessive zu einer langsamen Stabilisierung der Thrombozytenzellzahl.
Am 20. 10. 2025 betrug sie 51 G/l ohne Blutungszeichen.
In der Kontrolle vom 29. 10. 2025 kam es zu einem Anstieg der Thrombozytenzellzahl auf T = 144 G/l. Die Patientin berichtete über keine Nebenwirkungen unter der Einnahme von Rilzabrutinib. Subjektiv verbesserte sich der aufgrund einer schon länger bestehenden chronischen Fatigue reduzierte Allgemeinzustand. Diese Müdigkeit bestand zuletzt nicht mehr, und die Patientin verzeichnete eine Verbesserung der körperlichen Belastbarkeit unter der nun laufenden Therapie.
Die letzte ITP-spezifische medikamentöse Therapie besteht aus: Avatrombopag 40 mg/d, Prednisolon 2,5 mg/d und Rilzabrutinib 2-mal 400 mg/d.
-
November 2025Die Blutbildkontrolle vom 18. 11. 2025 ergab befriedigende Werte (Hb= 12,2 g/dl; T= 57 G/l,; L= 6,6 G/l; Retikulozyten= 14‰). Es zeigten sich keine Petechien, nur vereinzelt kleine, ältere Hämatome. Auch ein zwischenzeitlich aufgetretener milder, afebriler respiratorischer Infekt mit Husten, ohne CRP-Anstieg blieb ohne konsekutiven Thrombozytenabfall. Ein vorübergehender Thrombozytenabfall auf T = 21 G/l wurde in Zusammenhang mit einer stattgehabten Zahnextraktion gesehen und erforderte keine zusätzliche therapeutische Intervention. In kurzfristigen Folgekontrollen stiegen die Thrombozytenzahlen weiter an.
Die aktuelle Kontrolle vom 25. 11. 2025 ergab eine weiter steigende Thrombozytenzahl T = 93 G/l. Die Rilzabrutinib-Einnahme läuft nun bereits den 63. Tag. Die Begleitmedikation mit Avatrombopag 40 mg/d und Prednison 2,5 mg/d wurde noch belassen. Es zeigten sich keine Blutungszeichen, und von der Patientin wurde keine Fatigue berichtet. Nebenwirkungen der laufenden Therapie wurden ebenso nicht reportiert. Derzeit sind noch Schwankungen der Thrombozytenzahlen in den Kontrollen zu verzeichnen, die jedoch auch der Reduktion der laufenden Kortikosteroiddosis geschuldet sein dürften. In weiterer Folge ist nach Möglichkeit ein komplettes Absetzen des Steroids geplant.
Welche Feststellungen zur Therapie der ITP mit Rilzabrutinib, einem Bruton-Tyrosinkinase-Inhibitor, sind richtig? (3 richtige Antworten)
Fazit
Die Immunthrombozytopenie ist eine seltene Autoimmunerkrankung (Orphan Disease), bei der autoreaktive Antikörper gegen Thrombozyten und Megakaryozyten gebildet werden. Diese führen im retikuloendothelialen System (Milz, Leber, Knochenmark) zur Zerstörung der Thrombozyten mit entsprechenden Blutungskomplikationen. Kortikosteroide zeigen zwar initial hohe Ansprechraten bis über 70 %, sind jedoch aufgrund ihrer Nebenwirkungen für eine Langzeittherapie nicht zu präferieren. Aufgrund des häufig chronischen Verlaufs mit rezidivierend krisenhaftem Abfall der Thrombozyten besteht trotz der seit den späten 2000er-Jahren verfügbaren Thrombopoietin-Rezeptor-Agonisten und der Zulassung des SYK-Inhibitors Fostamatinib Bedarf an zusätzlichen therapeutischen Optionen. Mit dem oralen Bruton-Tyrosinkinase-Inhibitor Rilzabrutinib zeigte sich in der Verum-Gruppe in der randomisierten, placebokontrollierten, doppelblinden Phase-III-Studie LUNA 3 auch bei mehrfach vorbehandelten ITP-Patient:innen ein überlegenes Ansprechen hinsichtlich des Erreichens einer Thrombozytenzahl > 50 G/l ohne additive Rescue-Medikation in mindestens 8 der letzten 12 Wochen (primärer Endpunkt erreicht bei 46 % vs. 31 %) und eine Halbierung des Einsatzes von Rescue-Therapien. Rilzabrutinib reduzierte auch die ITP-assoziierte Fatigue. Nebenwirkungen waren mild bis moderat ausgeprägt. Eine Zulassung der Substanz in der ITP-Therapie ab der 3. Linie wird angestrebt. Die Substanz wird derzeit auch in weiteren Indikationen in Studien untersucht.
Vielen Dank, dass Sie unseren digitalen Patientenfall durchgearbeitet haben!
Bereitgestellt von:
OA Dr. Michael Fillitz
3. Medizinische Abteilung, Hämatologie und Onkologie, Mein Hanusch-Krankenhaus der ÖGK, Wien
Redaktion:
Illustrationen © MedMedia/KI-generiert
- Fachkurzinformation
FACHKURZINFORMATION:
missing Lorem Ipsum …
 Autor: OA Dr. Michael Fillitz
Autor: OA Dr. Michael Fillitz
- 3. Medizinische Abteilung, Hämatologie und Onkologie, Mein Hanusch-Krankenhaus der ÖGK, Wien