Das viszerale Angioödem
Das viszerale oder intestinale Angioödem ist eine seltene Erkrankung, welche mit hohem Leidensdruck für die Patienten einhergeht. Die Diagnostik sowie die Therapie gestalten sich oft schwierig.
Das Angioödem (AE) ist eine lokalisierte, selbstlimitierende Schwellung der Haut und der Mukosa. Ursächlich ist eine Extravasation von Flüssigkeit in das Interstitium bei zunehmender vaskulärer Permeabilität. Angioödeme können allein oder mit Urtikaria und Anaphylaxie auftreten.
Das Leitsymptom des viszeralen Angioödems sind kolikartige Bauchschmerzen. Diese können von Übelkeit, Erbrechen und/oder Diarrhö begleitet sein. Am häufigsten ist das Jejunum beteiligt, gefolgt vom Ileum und vom Duodenum. Das intestinale Angioödem kann als Schwellung der Darmwand mittels Computertomografie oder Ultraschalls dargestellt werden, wo sich typischerweise erweiterte Darmschlingen, Kokarden, verdickte Schleimhautfalten, perihepatische Flüssigkeit und/oder Aszites finden.
Viszerale Angioödeme sind bradykininmediiert und gehen daher, im Gegensatz zum mastzellmediierten Angioödem, nicht mit Pruritus und Urtikaria einher. Bradykinin ist ein potenter Vasodilatator, welcher auch die Permeabilität der Kapillaren erhöht. Somit kann vermehrt Flüssigkeit in das submukosale Gewebe übertreten, wodurch das Ödem entsteht.
ACE-Hemmer induziertes Angioödem
Das Auftreten eines ACE-Hemmer-induzierten Angioödems geht mit einer Wahrscheinlichkeit von 0,3–0,7 % unter ACE-Hemmer-Therapie einher. Hier sind die Haut, die oberen Atemwege und vor allem der Gastrointestinaltrakt betroffen.1 Die Entwicklung eines viszeralen Angioödems tritt meist innerhalb von 72 Stunden nach erstmaliger ACE-Hemmer-Einnahme auf, kann aber ebenso erst nach Jahren der Therapie auftreten.2 ACE-Hemmer-induzierte Angioödeme treten rezidivierend in einem Zeitabstand von 2–5 Tagen auf.3 Die Beschwerden beginnen meist innerhalb von Minuten nach Einnahme des Medikaments und lösen sich nach 1–3 Tagen wieder auf. Pathophysiologisch wird das ACE-Hemmer-induzierte Angioödem durch einen verminderten Abbau von mindestens 3 vasoaktiven Peptiden bedingt: Bradykinin selbst, des-Arg9-BK, einem aktiven Metaboliten von Bradykinin, und Substanz P. ACE-Hemmer blocken das ACE, das einerseits den Renin-Angiotensin-Aldosteron-Kreislauf, andererseits den Abbau von Bradykinin beeinflusst. Circa die Hälfte aller Patienten, die ein ACE-Hemmer-induziertes Angioödem entwickeln, hat zusätzlich einen Enzymdefekt im Des-Arg9-BK-Metabolismus. Mögliche Risikofaktoren zur Entwicklung eines ACE-Hemmer-induzierten Angioödems sind, neben Angioödemen in der Anamnese, Alter > 65 Jahre, weibliches Geschlecht, Nikotinabusus, bekannte Allergien, aber auch die Therapie mit Aspirin und nichtsteroidalen Antirheumatika. Die Entwicklung eines ACE-Hemmer-induzierten Angioödems ist weder vom Präparat noch der verabreichten ACE-Dosierung abhängig und somit ein Klasseneffekt.
Hereditäres Angioödem
Es gibt verschiedene Arten des hereditären Angioödems (HAE).4 Betroffen sind die Haut, die oberen Atemwege und der Gastrointestinaltrakt. Der Entwicklung des Angioödems geht meist eine Stresssituation (Operation, psychischer Stress) voraus. Dabei lassen sich zwei Erkrankungen hervorheben: die C1-Esterase-Inhibitor-(C1INH-)Defizienz (C1INH Typ 1) und die C1-Esterase-Inhibitor-Dysfunktion (C1INH Typ 2). Sie werden unter dem Sammelbegriff hereditäre Angioödeme mit C1-Esterase-Inhibitor-Defizienz (C1INH-HAE) zusammengefasst. Alle anderen Arten gehen mit unauffälligem C1INH einher. C1INH ist ein Akut-Phase-Reaktant, der zur Familie der Serin-Protease-Inhibitoren zählt. C1INH inhibiert Schritte des klassischen und des Lektin-Komplement-Weges sowie auch die intrinsische Koagulation, fibrinolytische, kallikrein- und kininproduzierende Kreisläufe. Die Funktion von C1INH in der Entwicklung des Angioödems verläuft über den kallikrein- und kininproduzierenden Kreislauf.5
C1INH-AE Typ 1 macht ca. 85 % der C1INH-HAE aus und geht mit einer verminderten Sekretion von C1INH einher. Bei Patienten ist sowohl der gesamte als auch der funktionelle C1INH-Spiegel erniedrigt.
C1INH-AE Typ 2 macht ca. 15 % der C1INH-HAE aus und geht mit einem defekten C1INH-Protein einher. Der Serumspiegel des funktionellen C1INH ist erniedrigt, die Gesamtserumkonzentration ist jedoch unauffällig.
C1INH-AE wird autosomal dominant vererbt. Allerdings sind 25 % aller Fälle De-novo-Mutationen. Fast alle betroffenen Patienten sind heterozygot, wobei sich bei ca. 10 % keine phänotypische Manifestation ausprägt.
HAE mit unauffälligem C1INH: Diese Formen des HAE weisen unauffälliges C1 und C4 auf, allerdings scheint eine positive Familienanamnese für Angioödeme und eine Mutation des Faktor XII eine Prädisposition darzustellen.6
Das hereditäre Angioödem manifestiert sich meist im Kindes- bzw. jungen Erwachsenenalter.
Angioödem bei erworbener C1-Esterase-Inhibitor-Defizienz
Das Angioödem bei erworbener C1-Esterase-Inhibitor-Defizienz (C1INH-AAE) unterscheidet sich weder in der pathophysiologischen Entstehung, noch in der Klinik vom hereditären Angioödem. Klinisch ist hervorzuheben, dass sich das Angioödem bei C1INH-AAE meist erst nach dem 40. Lebensjahr manifestiert. C1INH-AAE tritt häufig im Rahmen von lymphoproliferativen Erkrankungen und hier vor allem bei B-Zell-Malignomen auf (39 % der C1INH-AAE). Des Weiteren können Autoimmunerkrankungen, wie der systemische Lupus erythematodes oder die autoimmune hämolytische Anämie, zu Grunde liegen. Ein Großteil der Patienten mit C1INH-AAE haben nachweisbare Antikörper gegen C1INH.
Diagnose
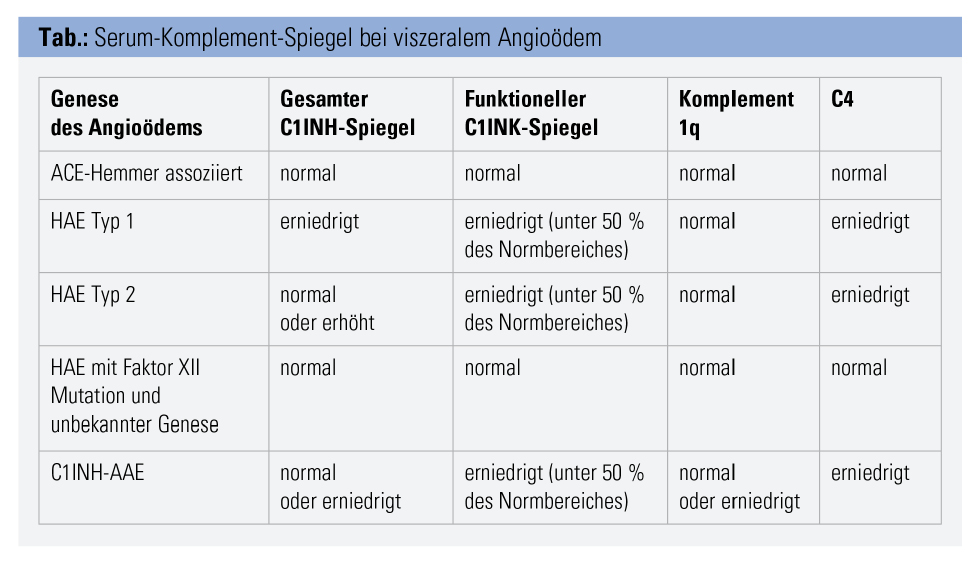
Die Diagnose des viszeralen Angioödems gestaltet sich oft schwierig und stützt sich vor allem auf die Klinik der Patienten. Viele berichten oft über eine jahrelange Krankheitsgeschichte, bevor die richtige Diagnose gestellt wird. Bei anamnestisch rezidivierenden kolikartigen Bauchschmerzen mit Erbrechen, Diarrhö und ggf. Aszites und möglichem Angioödem der Haut und der oberen Atemwege soll laborchemisch Komplementfaktor 4 (C4) sowie C1INH und das funktionelle C1INH bestimmt werden (Tab.). In Abhängigkeit davon kann das HAE Typ 1 und das HAE Typ 2 sowie das C1INH-AAE diagnostiziert werden. Die Diagnose der weiteren Formen ist rein aus Anamnese und mittels Bildgebung herzuleiten.
Therapie
Die Therapie der Wahl des ACE-Hemmer-induzierten Angioödems ist natürlich das Absetzen des ACE-Hemmers.
Beim hereditären Angioödem unterscheidet man zwischen Akutbehandlung und Prophylaxe.4 Behandlung akuter Attacken: Die Therapie sollte so bald als möglich erfolgen, da dadurch Symptome und Krankheitsdauer gelindert werden. Je früher die Therapie erfolgt, desto milder sind die Symptome. Die Prophylaxe muss auch die Prävention vor medizinischen Eingriffen (Operation, Zahnbehandlung, Entbindung) beinhalten. Sie soll bei anamnestisch mehr als zwei akuten Attacken pro Monat begonnen werden.7
Mehrere rekombinante C1-INH-Konzentrate stehen zur Behandlung akuter Attacken, Prävention vor medizinischen Eingriffen und zur Prophylaxe zur Verfügung. Cinryze® kann zur Routineprophylaxe (Kurzzeit- und Langzeitprophylaxe), präoperativen Prophylaxe und zur Behandlung akuter AE-Attacken in einer Dosierung von 1.000 I.E. intravenös verabreicht werden. Berinert® ist gewichtsabhängig zu dosieren; neben einer intravenösen Formulierung zur Behandlung akuter Attacken sowie zur präoperativen Prophylaxe, ist eine subkutane Formulierung für die Langzeitprophylaxe zugelassen.
Der Bradykinin-Rezeptor-Antagonist (Icatibant) wird zur Therapie einer akuten Attacke des HAE eingesetzt. Bei Erwachsenen werden 30 mg in einer gebrauchsfertigen Spritze subkutan appliziert, bei Kindern und Jugendlichen (2–17 Jahre) erfolgt die Dosierung gewichtsabhängig.
Plasma-Kallikrein-Inhibitoren (Lanadelumab, Avoralstat, BCX7353): Lanadelumab
ist ein voll humaner monoklonaler Antikörper gegen Plasma-Kallikrein, der die Häufigkeit von HAE-Attacken effektiv zu senken vermag.8 Die Dosierung beträgt 300 mg subkutan alle 2 Wochen. Das Präparat ist seit Kurzem in Österreich verfügbar. BCX7353 und Avoralstat sind orale Plasma-Kallikrein-Inhibitoren, die einmal täglich bzw. dreimal täglich eingenommen werden und in rezenten Studien eine sehr gute Wirkung in der Therapie bzw. bei der Verkürzung der Episoden zeigten.9, 10 Sie stehen möglicherweise in den nächsten Jahren als Alternative in der Langzeittherapie zur Verfügung.
Resümee
Zusammengefasst ist das viszerale Angioödem eine seltene Erkrankung, welche mit oder ohne Beteiligung der Haut und der oberen Atemwege einhergehen kann. Da die Erkrankung bradykininvermittelt ist, ist eine anaphylaktische Therapie nicht indiziert. Patienten mit viszeralem Angioödem stellen eine Herausforderung in der Diagnose und Behandlung dar.