Das langanhaltende Dogma einer sterilen Blase wurde in den letzten Jahren durch eine Vielzahl neuer Erkenntnisse widerlegt. Dem „Darm mit Charme“ folgten Erkenntnisse hinsichtlich des urogenitalen Mikrobioms. Die fortschreitende Entwicklung moderner Techniken zur DNA-Sequenzierung, insbesondere des Next-Generation Sequencing (NGS), ermöglicht immer tiefere Einblicke in die molekulare Charakterisierung urologischer Infektionen und eröffnet zugleich auch neue therapeutische Ansätze. Welche neuen Perspektiven bezüglich Prophylaxe und Therapie gibt es, und für welche Patientengruppen ist eine antibiotische Therapie tatsächlich sinnvoll?
Das urogenitale Mikrobiom
Es ist bereits seit Längerem bekannt, dass menschlicher Urin, auch bei beschwerdefreien Menschen, nicht steril ist. Der gesamte Urogenitaltrakt ist von unterschiedlich spezifischen kommensalen Mikroorganismen besiedelt, allein im katheterisierten Harn gesunder Erwachsener lassen sich ca. 200 verschiedene Bakteriengattungen nachweisen.1, 2 Das Mikrobiom ist für die Homöostase der Organe essenziell, bildet eine protektive biophysikalische Barriere, baut Umweltgifte und Stoffwechselmetaboliten ab, verhindert die Ansiedelung von Pathogenen und trägt maßgeblich zur Reifung von Immunzellen bei. Es unterliegt einem sensiblen Gleichgewicht, in dem sich dauerhafte Störungen der Zusammensetzung nachhaltig auswirken.2 Die Veränderung der physiologischen bakteriellen Zusammensetzung bzw. die Verringerung der bakteriellen Diversität nennt man Dysbiose.
Die physiologische Komposition ist geschlechtsspezifisch und altersabhängig. Während bei Kindern unter 4 Jahren noch ein sehr uniformes urogenitales Mikrobiom (vorwiegend charakterisiert durch Prevotella, Peptoniphilus, Escherichia, Veillonella und Finegoldia) vorherrscht, entwickelt sich im weiteren Verlauf, insbesondere durch routinierte Toilettennutzung und später in der Pubertät, eine geschlechtsspezifische Differenzierung.3 Bei Frauen finden sich später insbesondere: Actinomyces, Lactobacillaceae, Gardnerella, Prevotella und Aerococcus.4 Im Vergleich dazu ist der Urogenitaltrakt bei Männern vorwiegend mit Veillonella, Streptococcus und Corynebacterium besiedelt.5
Asymptomatische Bakteriurie
Der früher postulierte Schwellenwert einer signifikanten Bakteriurie von 105 Erregern pro ml im Mittelstrahlurin (Kass-Zahl) tritt zunehmend in den Hintergrund. Im klinischen Alltag gewinnt stattdessen die Symptomatik der Patient:innen bei der Abklärung einer Infektion an Bedeutung. Hiervon abzugrenzen ist die asymptomatische Bakteriurie (ABU). Darunter versteht man den Nachweis von Bakterien im Urin ohne Infektionsreaktion des Körpers. Je nach Methode der Uringewinnung gelten unterschiedliche Bakterienkonzentrationen (Mittelstrahlharn ≥ 105 CFU/ml, Einmalkatheterharn ≥ 102 CFU/ml).6 Bei wiederholtem Nachweis ureaseproduzierender Bakterien sollten stets mögliche Steine im Harntrakt ausgeschlossen werden.7 Ein Sonderfall ist die ABU bei Schwangeren: Hier wird ein Screening sowohl bei der Erstvorstellung als auch in der 16. Schwangerschaftswoche empfohlen. Im Falle eines Nachweises sollte eine antibiotische Therapie erfolgen, beispielsweise in Form einer einmaligen Gabe von Fosfomycin.8 Darüber hinaus entwickeln ausnahmslos alle Patient:innen mit transurethralen oder suprapubischen Kathetern, Ureterstents oder Nephrostomien eine ABU, die ohne weitere Symptome keinerlei Behandlung benötigt.
Rezidivierende Harnwegsinfektionen
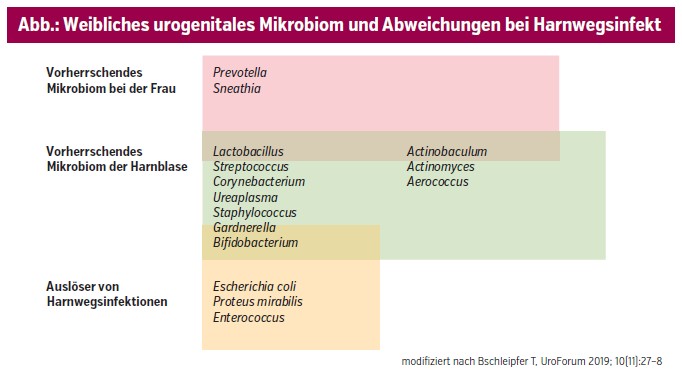
Das unangenehme Empfinden von Dysurie sowie die lästige Pollakisurie, einhergehend mit Schmerzen im Unterleib, hat ab dem 24. Lebensjahr etwa eine von 3 Frauen mindestens einmal im Leben erfahren.9 Rezidivierende Harnwegsinfektionen (rHWI) treten definitionsgemäß mindestens 2-mal binnen 6 Monaten oder 3-mal binnen 12 Monaten auf.10 Neben körperlichen und psychischen Belastungen führen rHWI zu einer Einschränkung der Lebensqualität und haben darüber hinaus sozioökonomische Auswirkungen. Zudem ist vor allem die mit der wiederholten Exposition gegenüber Antibiotika assoziierte Zunahme von bakteriellen Resistenzen von großer Bedeutung. Bei symptomatischen Patient:innen mit negativen Urinkulturen können zur exakteren Identifizierung und Differenzierung von Uropathogenen neue Methoden wie die 16S-rRNA-Sequenzierung und „expanded quantitative urine culture“ (EQUC) eingesetzt werden.11 Die Abbildung zeigt eine Übersicht über das weibliche urogenitale Mikrobiom und dessen Abweichungen bei HWI.
Steinerkrankungen
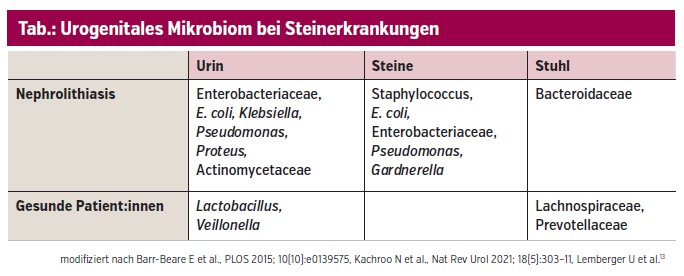
Bislang konnte weder ein spezifisches Bakterium noch eine charakteristische mikrobielle Besiedelung als Auslöser der Steinbildung identifiziert werden. Dennoch weisen, neben den klassischen Infektsteinen (Struvit), alle Steintypen ein mehr oder weniger ausgeprägtes Mikrobiom auf. Enterobacteriaceae, insbesondere E. coli, zählen zu den am häufigsten nachgewiesenen Pathogenen bei Patient:innen mit Nierensteinen.12, 13 Eine systemische Dysbiose scheint die Steinentstehung zu begünstigen (Tab.). Eine Dysbiose im Darmmikrobiom kann die Verdauung und Absorption von Nährstoffen beeinträchtigen und dadurch zu erhöhten Konzentrationen von Oxalat und Kalzium im Urin führen, was wiederum das Risiko einer Nierensteinbildung erhöht.14
Optionen zur Prophylaxe und Therapie
Die größte Gefahr für die bakterielle Homöostase des Urogenitaltraktes stellen Langzeittherapien mit Antibiotika und Manipulationen mit Fremdkörpern (z. B. Kathetern) dar. Studien zufolge sind etwa 20–50 % der in Schwerpunktkrankenhäusern verordneten Antibiotika entweder unnötig oder unpassend gewählt, was die Frage nach dem sinnvollen Einsatz von Antibiotika zunehmend in den Vordergrund rückt.15
Eine ausführliche Patientenaufklärung hinsichtlich der Vermeidung von Risikofaktoren (z. B. geringe Trinkmengen, Unterkühlung, übertriebene Intimhygiene) sowie eine adäquate Diagnostik (Harnkulturen, Restharnbestimmung) sollten einer antibiotischen Therapie vorausgehen. Bei rezidivierenden HWI können – in ausgewählten Fällen – zusätzlich eine Zystoskopie sowie bildgebende Verfahren sinnvoll sein.
Eine orale OM-89-Immunprophylaxe deckt 18 E.-coli-Stämme ab und kann über 3 Monate verabreicht werden. Alternativ besteht die Möglichkeit einer Immunisierung durch 3 parenterale Injektionen von inaktivierten spezifizierten Enterobakterien im wöchentlichen Abstand.16 Neue Ansätze mit Phytotherapeutika in Kombinationen (z. B. Xyloglucan, Hibiskus und Propolis oder Centaurii herba, Levistici radix und Rosmarini folium) zeigen in kleineren Patientenkohorten vergleichbare Ergebnisse zur antibiotischen Therapie.17, 18 Die Datenlage zu Cranberry-Produkten und D-Mannose bleibt kontrovers und ohne klare Empfehlung.19, 20 Die Gabe von nichtsteroidalen Antirheumatika (z. B. Ibuprofen) führt zur effektiven Symptomlinderung und reduziert in vielen Fällen den Einsatz von Antibiotika.21
Bei postmenopausalen Frauen kann eine vaginale Östrogentherapie das Risiko für rHWI senken. Kontraindikationen wie die Anamnese von Zervixkarzinom, Mammakarzinom oder Endometriose sind jedoch strikt zu beachten.22 Eine weitere Alternative zur antibiotischen Therapie könnten auch Probiotika wie z. B. Lactobacilli darstellen.23 Hierbei handelt es sich um Mikroorganismen, die in therapeutischer Dosierung in verschiedenen Applikationsformen verabreicht werden können. Sie sollen die natürliche Barrierefunktion der Vaginalschleimhaut aufrechterhalten oder wiederaufbauen, um die Migration pathogener Erreger zu verhindern.24 Ein eindeutig protektiver Effekt von Lactobacilli auf die Entwicklung von symptomatischen HWI konnte bisher jedoch nicht nachgewiesen werden. Bei Versagen der nichtantimikrobiellen Prävention kann eine kontinuierliche Langzeitantibiotikaprophylaxe über 3–6 Monate (z. B. Nitrofurantoin 50–100 mg 1-mal pro Tag, Fosfomycin 3 g alle 10 Tage) oder ggf. eine postkoitale Prophylaxe erfolgen.25, 26