Hyperkaliämie – symptomlose Gefahr
Hyperkaliämie ist aufgrund ihrer potenziell lebensbedrohlichen Auswirkung sehr ernst zu nehmen und wird zumeist als Serum-Kalium (sK+) ≥ 5,6 mmol/l (evtl. > 5,0 mmol/l) definiert. Unter den Ursachen für Hyperkaliämie sind chronische Nierenkrankheit (CKD), Diabetes, Herzinsuffizienz und die Verwendung von Hemmern des Renin-Angiotensin-Aldosteron-Systems (RAASi) oder Mineralokortikoid-Rezeptor-Antagonisten (MRA) hervorzuheben. Hyperkaliämie ist ein unabhängiger Risikofaktor für Mortalität jeder Ursache, für kardiovaskuläre Ereignisse und Hospitalisierung, auch auf Intensivstationen.
In der klinischen Aufarbeitung von Patient:innen gilt es zu unterscheiden zwischen echt vermehrtem Kaliumbestand, z. B. durch verminderte K+-Ausscheidung oder exzessive K+-Zufuhr, und von Verteilungsstörungen (K+-Shift nach extrazellulär). Differenzialdiagnostisch ist an Pseudohyperkaliämie zu denken, z. B. durch Hämolyse bei langem Stauen während einer Blutabnahme. Diese kann das K+ um bis zu 2 mmol/l ansteigen lassen. Bei Erhöhung des K+-Bestandes im Organismus um etwa 1–4 mmol/kg Körpergewicht erhöht sich das sK+ um etwa 1 mmol/l.
Klinische Auswirkungen
Die Klinik hängt davon ab, wie schnell sich die Hyperkaliämie entwickelt. Mögliche Symptome sind Muskelschwäche, schlaffe Paralyse oder Ileus. EKG-Veränderungen treten nur bei etwa der Hälfte der Patient:innen mit sK+ > 6,5 mmol/l auf. Charakteristisch ist Bradykardie, terminal kann es zu Kammerflimmern oder Herzstillstand kommen. Geübte Kliniker:innen werden bei Patient:innen mit Risiko für Hyperkaliämie, besonders bei CKD, Diabetes oder Verwendung von RAASi und/oder MRA, immer wieder Kontrollen des sK+ veranlassen.
Therapie akut
Nach Expert:inneneinschätzung ist von schwerwiegender Hyperkaliämie ab einem K+ > 6,0 mmol/l zu sprechen, vor allem, wenn EKG-Veränderungen vorliegen bzw. bei K+ > 6,5 mmol/l ohne EKG-Auffälligkeiten. Charakteristisch im EKG sind hohe spitze T-Wellen, Verbreiterung des PQ-Intervalls und der Kammerkomplexe und zuletzt Verlust der P-Welle und Ausbildung einer Sinuskurve. Die Akuttherapie besteht in der Gabe von Kalziumglukonat i. v. zur Membranstabilisierung. Eine Glukose-Insulin-Infusion bewirkt einen Shift von K+ nach intrazellulär, ähnlich wie ein Azidoseausgleich. Die orale Gabe von K+-Bindern in Korrekturdosis bindet K+ intestinal und verhindert die Resorption. Inhalation von β2-Agonisten wie Salbutamol dürfte ähnlich wirksam sein wie Insulin/Glukose. Potenziell hyperkaliämieinduzierende Medikamente (RAASi, MRA) sind zu pausieren. Eventuell ist eine Dialysebehandlung einzuleiten. Intensivmedizinische Überwachung ist selbstverständlich.
Therapie chronisch
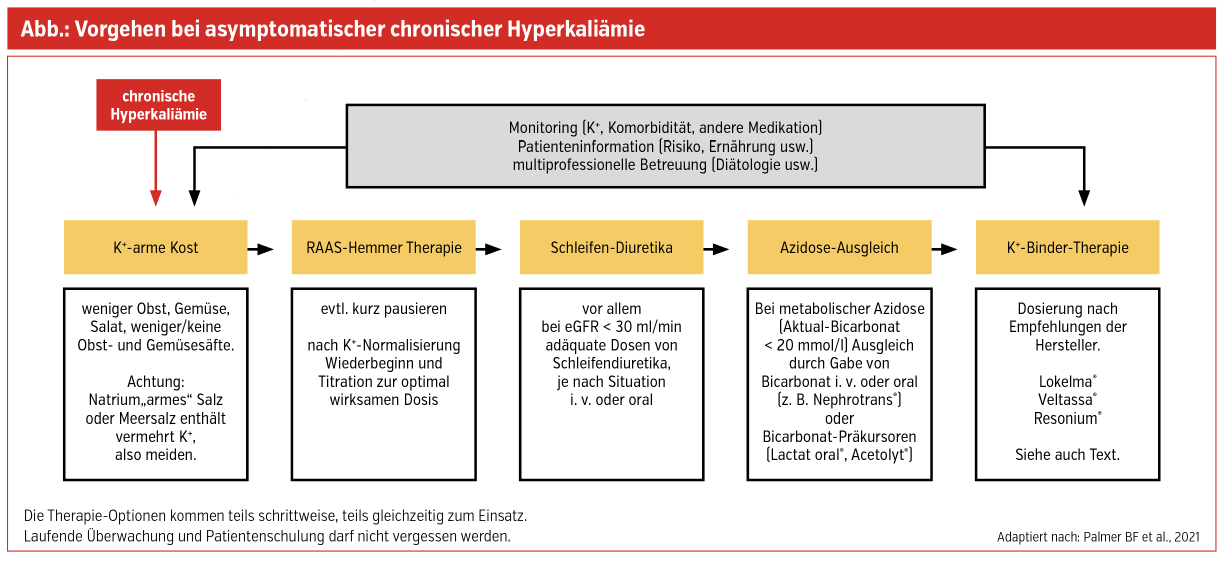
Aufgrund der hohen Mortalität ist jede Hyperkaliämie ernst zu nehmen. Das Risiko steigt mit dem K+-Spiegel. Regelmäßige K+-Kontrollen müssen Standard sein bei CKD, Diabetes, Herzinsuffizienz und Hypertonie sowie bei der Verwendung von potenziell hyperkaliämieauslösenden Medikamenten. Die Therapieschritte sind in der Abbildung angeführt und werden folgend detailliert diskutiert.
Ernährungstherapie: Hyperkaliämie durch exzessive K+-Zufuhr kommt fast nur bei gleichzeitiger höhergradiger CKD vor. Die Ernährungsberatung zielt darauf ab, K+-reiche Nahrungsmittel dosiert zuzuführen („so viel Obst am Tag wie ein mittelgroßer Apfel“). Zum Teil kann K+ durch „Auswässern“ aus den Nahrungsmitteln entfernt werden („Kartoffeln abends schälen, vierteln, in Wasser einlegen, am Folgetag in frischem Wasser kochen“). Obst- und Gemüsesäfte sind zu meiden. Weniger Rohkost und weniger Salat kann mithelfen, das Problem in den Griff zu bekommen. Diesen Empfehlungen steht entgegen, dass vegetarische Ernährung zu weniger Bildung von Säureäquivalenten führt und damit eine metabole Azidose hintanhält.
Hemmer des RAAS: ACE-Hemmer, ARBs und MRA sind je nach Klinik zumindest bei schwerer Hyperkaliämie zu pausieren. Im Zuge akuter Erkrankungen ist zu überlegen, ob die „sick day rules“ anzuwenden sind (Merkwort: SADMANS, d. h. Pausieren von Sulfonylharnstoffen, ACE-Hemmern, Diuretika, Metformin, ARBs, nichtsteroidalen Antirheumatika, SGLT-2-Hemmern, bis normale Nahrungs- und Flüssigkeitszufuhr wieder möglich sind). Hat sich das sK+ normalisiert und ist stabil, so soll die RAASi-Therapie – wie oben diskutiert – wieder begonnen und bis zur höchstmöglichen Dosis gemäß Fachinformationen titriert werden.
Diuretika: Sowohl CKD- als auch Herzinsuffizienz-Patient:innen haben häufig einen Volumenüberschuss, klinisch sichtbar an Ödemen bzw. Gewichtszunahme (> 1 kg/24 h). Schleifendiuretika, hier in höherer Dosis erforderlich, bewirken neben mehr Diurese auch eine K+-Ausschwemmung innerhalb einiger Stunden, weshalb sie als subakut wirksame Maßnahme eingesetzt werden können. Ohne Hypervolämie ist die Gabe von Schleifendiuretika (Furosemid) nicht sinnvoll.
Azidose-Ausgleich: Bei CKD und Hyperkaliämie muss regelhaft eine Blutgas-Analyse erfolgen, da häufig eine metabole Azidose (pH < 7,36, Aktual-Bicarbonat < 20 mmol/l) besteht. Diese bewirkt die Umverteilung von K+ von intra- nach extrazellulär. Insbesondere bei chronischer, asymptomatischer, geringer bis moderater Hyperkaliämie kann die alleinige Azidose-Korrektur die Hyperkaliämie eventuell beheben. Zum Einsatz kommt orales Bikarbonat, wobei der hohe Na+-Gehalt des als Na+-Salz vorliegenden Bikarbonats zu bedenken ist (Hypertonie, Hypervolämie). Weitere Möglichkeit ist die Gabe von Bikarbonat-Präkursoren. Pro 0,1 pH-Anstieg fällt das sK+ um ca. 0,7 mmol/l.
Kaliumbinder: Bei fortgeschrittener CKD sind K+-Binder schon lange zur Hyperkaliämie-Korrektur im Einsatz. In der Therapie kommt modernen K+-Bindern wie Natrium-Zirkonium-Cyclosilikat und Patiromer zunehmende Bedeutung zu, weil damit prognoseverbessernde Therapien mit Blockern des RAAS oder Mineralokortikoid-Rezeptor-Antagonisten kontinuierlich eingesetzt werden können. Im Vergleich der K+-Binder zeigen alle eine wirksame Senkung des sK+, auch wenn die Wirkung mit SZC am raschesten erreicht wird. Bezogen auf schwerwiegende Nebenwirkungen spricht vieles gegen Natrium-Polystyren-Sulfonat, zumal es auch keine prospektiv randomisierten Studien über mehr als 7 Tage aufweisen kann. Für Patiromer spricht, dass es natriumfrei ist. Für SZC spricht die durch Studien gut belegte Vorgangsweise mit Korrektur- und Erhaltungsphase in der Therapie der Hyperkaliämie sowie dass es nahrungsunabhängig und weitgehend ohne Zeitabstand zu anderen Medikamenten verabreicht werden kann.
Die Möglichkeit der Gabe von Fludrocortison 0,1 mg/d als Mineralokortikoid-Agonist zur K+-Senkung wird in Übersichten nur am Rande erwähnt. Zumindest bei Dialysepa-tient:innen könnte dies eine Therapiealternative sein.
Wissenswertes für die Praxis
- Hyperkaliämie kann durch Hemmer des Renin-Angiotensin-Aldosteron-Systems, kaliumsparende Diuretika oder deren Kombination ausgelöst werden und wird durch Nierenfunktionseinschränkung, Diabetes und andere Erkrankungen begünstigt.
- Bedrohlich wird die Hyperkaliämie bei EKG-Veränderungen, ein normales EKG schließt Gefahr aber nicht aus. Verteilungsstörungen des Kaliums von intra- nach extrazellulär sind zu bedenken, z. B. bei Azidose oder gestörter renaler Exkretion. Eine Pseudohyperkaliämie ist auszuschließen.
- Therapeutisch sind Akutmaßnahmen von chronischer Therapie zu unterscheiden. Modernen Kalium-Bindern wie Natrium-Zirkonium-Cyclosilikat oder Patiromer kommt steigende Bedeutung zu.