Lungenkrebs ist nicht gleich Lungenkrebs
Das Bronchialkarzinom geht mit einer hohen Mortalität einher. Laut Statistik Austria wurden im Jahr 2017 4.716 Patienten mit Lungenkrebs diagnostiziert, und insgesamt 3.908 Patienten sind an einem solchen verstorben. Im Vergleich dazu betrug das Inzidenz-Mortalität-Verhältnis beim Mammakarzinom 5.454 zu 1.549 und beim Kolorektalkarzinom 4.567 zu 2.164.
Unterschieden wird zwischen nichtkleinzelligem Bronchialkarzinom (NSCLC – „non small cell lung cancer“), das mit etwa 85 % den Großteil aller Erkrankungsfälle ausmacht, und kleinzelligem Bronchialkarzinom (SCLC – „small cell lung cancer“). Letzteres geht aufgrund der raschen Metastasierung mit einer (noch) schlechteren Prognose einher.
In der Therapie des Bronchialkarzinoms konnten in den vergangenen Jahren große Fortschritte erzielt werden. OA Dr. Maximilian Hochmair leitet die onkologische Ambulanz/Tagesklinik am Krankenhaus Nord und ist im Bereich der Lungenkarzinomforschung mindestens ebenso erfolgreich wie sein älterer Bruder Phillipp Hochmair, der im April mit dem österreichischen Film- und Fernsehpreis „Romy“ in der Kategorie „beliebtester Schauspieler“ ausgezeichnet wurde. „Noch vor 10 Jahren war die therapeutische Situation des Bronchialkarzinoms sehr unbefriedigend. Fast alle Patienten erhielten Chemotherapie, die palliativtherapeutische Begleitung spielte eine zentrale Rolle. Heute gibt es viele verschiedene wirksame Präparate, die uns einem komplexen Therapiealgorithmus folgend zur Verfügung stehen. Früher haben wir gesagt: ‚Krebs ist gleich Krebs‘. Mittlerweise wissen wir, dass es nicht den einen Lungenkrebs, sondern viele verschiedene Subgruppen gibt, die unterschiedlich und in multidisziplinärer Zusammenarbeit mit Pathologen, Radiologen und Chirurgen behandelt werden müssen. Jeder Patient hat eine eigenständige Erkrankung“, führt Maximilian Hochmair aus.
Die zwei Säulen der NSCLC-Therapie
Die Therapie des nichtkleinzelligen Bronchialkarzinoms basiert mittlerweile hauptsächlich auf zwei Säulen: Der zielgerichteten Therapie oder der Immuntherapie plus/minus Chemotherapie.
Das NSCLC lässt sich unterteilen in: Adenokarzinome (60–70 %), Plattenepithelkarzinome (20–30 %) und großzellige Karzinome (circa 5 %), wobei bei Letzteren neuroendokrine von nichtneuroendokrinen Karzinomen zu unterscheiden sind. Neuroendokrine großzellige Karzinome werden wie das kleinzellige Bronchialkarzinom behandelt. Bronchialkarzinome, die sich nicht zuordnen lassen, werden als „NOS“ („not otherwise specified“) bezeichnet.
Liegt ein Adenokarzinom oder ein anderes Nichtplattenepithelkarzinom vor, wird auf die Möglichkeit einer zielgerichteten Therapie getestet, sprich, auf das Vorliegen einer Mutation, für die ein spezifischer Wirkstoff zur Verfügung steht. Dazu zählen unter anderem EGFR, EML4-ALK, ROS 1, BRAF, MET und RET. Patienten, die auf eine dieser Translokationen positiv sind, erhalten primär eine zielgerichtete Therapie, denn, so Hochmair: „Wir wissen, dass die Patienten, die für eine zielgerichtete Therapie in Frage kommen, nicht so stark von der Immuntherapie profitieren.“
Bei Plattenepithelkarzinomen, die wie auch das SCLC fast ausschließlich bei Rauchern auftreten, finden sich nur selten Möglichkeiten einer zielgerichteten Therapie, daher werden diese Patienten auch nur auf eine Mutation getestet, wenn sie nie geraucht haben.
Immuntherapie: Patienten, die keine der getesteten Translokationen für eine zielgerichtete Therapie aufweisen, erhalten eine Immuntherapie ± Chemotherapie. Über
die Blockade des PD-1- beziehungsweise PD-L1-Rezeptors stimuliert diese die körpereigene Fähigkeit, Tumorzellen zu erkennen und auszuschalten. Abhängigkeit vom Ausmaß der PD-L1-Expression erhalten die Patienten eine Immun-Monotherapie oder eine Kombination mit Chemotherapie. „Exprimieren mehr als 50 % der Tumorzellen PD-L1, und das ist bei etwa einem Drittel der Patienten der Fall, besteht auch die Möglichkeit, nur mit Immuntherapie zu verfahren. Viele Patienten entscheiden sich für diese Option. Bei Patienten mit einer PD-L1-Expression kleiner als 50 % hingegen sprechen die Daten klar für eine Immun-Chemo-Therapie in der Erstlinie“, erläutert der Experte.
Auch für die Kombination von Radio- und Immuntherapie gibt es mittlerweile positive Daten: „Patienten mit lokalisierten Erkrankungen, die nach einer Strahlen- oder Radio-Chemo-Therapie eine Immuntherapie erhalten, zeigen ein besseres Überleben“, so Hochmair.
Die Immuntherapie wird abhängig von der Wirksubstanz im Abstand von mehreren Wochen am behandelnden Zentrum infundiert. Neue Daten unterstützen immer größere Abstände zwischen den Behandlungen und ermöglichen dadurch eine patientenfreundlichere Anwendung.
Hoffnungsschimmer beim SCLC
Aufgrund der unspezifischen Symptomatik wird das Bronchialkarzinom oft erst spät erkannt.
Beim SCLC liegt zum Zeitpunkt der Diagnosestellung meistens bereits eine multiple Metastasierung vor. Nur bei einem geringen Prozentsatz der Patienten können lokale Therapiemaßnahmen wie Chemo-Radio-Therapie überhaupt noch zur Anwendung kommen. Auch hinsichtlich der Therapie (Standard: Cisplatin beziehungsweise Carboplatin mit Etoposid) konnten seit Jahrzehnten keine Fortschritte erzielt werden. Vor kurzem wurde endlich wieder eine vielversprechende Studie veröffentlicht, die Anlass zur Hoffnung gibt. Hochmair ist Co-Autor der Studie, die im NEJM publiziert wurde: „Zum ersten Mal nach langer Zeit war dies eine positive Studie in der Erstlinientherapie des SCLC. Die Kombination aus Carboplatin und Etoposid plus Immuntherapie steigerte das Gesamtüberleben von fitten Patienten um 2 Monate.“
Ansprechen und Überleben
Die Frage nach dem Überlebensvorteil der neuen Therapien lässt sich nicht pauschal beantworten, da sie von vielen verschiedenen Faktoren wie zum Beispiel den vorliegenden Mutationen abhängig ist, erläutert Hochmair: „Generell kann gesagt werden, dass durch die neuen Therapien die Ansprech- und Überlebensraten deutlich verbessert werden konnten. Es gibt Patientengruppen, bei denen wir das Überleben im Vergleich zu früher verdrei- bis vervierfachen konnten. Durch Biomarkertests können wir zudem voraussagen, welcher Patient von welcher Therapie profitiert. Dennoch gibt es Typen des Bronchialkarzinoms, bei denen wir nach wie vor machtlos sind.“
Nebenwirkungen erkennen
Prinzipiell sind die Nebenwirkungen der neuen Therapien deutlich harmloser als jene unter Chemotherapie. Bei der Immuntherapie, den PD-1-/PD-L1-Inhibitoren, handelt es sich vor allem um Hautausschläge, Durchfälle und Colitis, Pneumonitis, sowohl Hyper- als auch Hypothyreosen und Hepatitis. „Diese immunassoziierten Nebenwirkungen können auch noch lange nach Beendigung der Immuntherapie auftreten. Mit diesem Wissen wird der Allgemeinmediziner bei einem Patienten mit
aktueller oder vorangegangener Immuntherapie und Durchfall anders vorgehen als bei einem normalen Durchfallpatienten. Es ist wichtig, rasch zu reagieren und mit dem behandelnden Zentrum Kontakt aufzunehmen. Das Mittel der Wahl bei immunmediierten Nebenwirklungen ist Kortison. Bei einer frühzeitigen Gabe sind sowohl lokal als auch systemisch die Nebenwirkungen damit gut in den Griff zu bekommen. Wir versuchen natürlich auch, die Patienten darauf zu schulen, sich bei Nebenwirkungen sofort zu melden oder zumindest ihren Patientenpass beim Arzt herzuzeigen.“
Interessanterweise haben Nebenwirkungen, die im Zusammenhang mit einer Immuntherapie auftreten, nicht nur Nachteile. Patienten, bei denen diese Nebenwirkungen auftreten, haben eine bessere Prognose, so Hochmair: „Offenbar wird bei diesen Patienten das Immunsystem durch die Immuntherapie stärker stimuliert, was in einem besseren Gesamtüberleben resultiert.“
Wechselwirkungen
Relevante Kontraindikationen für die neuen Lungenkrebstherapien gibt es laut Hochmair kaum.
Ältere wie jüngere Patienten profitieren gleichermaßen von der Therapie. „Vorsichtig muss man bei Autoimmunerkrankungen, die mit hohen Kortisondosen behandelt werden, sein. Liegt jedoch beispielsweise eine stabile rheumatische Erkrankung vor, kann die Immuntherapie durchaus gegeben werden. Was wir derzeit nicht empfehlen – da wir noch keine adäquaten Daten dazu haben –, ist, eine Grippeimpfung während laufender Immuntherapie durchzuführen, da dies zu vermehrten Nebenwirkungen führen kann. Auch von Lebendstoffimpfungen während Chemotherapie raten wir ab.“
Wo geht die Reise hin?
Abgesehen von noch mehr Studien zu verschiedenen Kombinationstherapien werden auch neue das Immunsystem inhibierende und stimulierende Rezeptoren untersucht.
Das Mikrobiom zeigt – wie in vielen anderen Bereichen auch – beim Bronchialkarzinom Zukunftspotenzial, verrät Hochmair: „Es gibt Studien, die vermuten lassen, dass eine positive Beeinflussung der Darmflora zu einer besseren Wirksamkeit der Immuntherapie führt. So zeigen etwa Patienten, die Magensäurehemmer während Immuntherapie einnehmen oder häufiger ein Antibiotikum brauchen, ein schlechteres Ansprechen.“
Prävention
Da 85–90 % der Bronchialkarzinome tabakassoziiert sind, ist die beste Prophylaxe der Tabakentzug.
Hochmair nimmt die Politik in die Verantwortung: „Es ist eine Katastrophe! Der logischste Ansatzpunkt wäre, bessere Rauchergesetze zu installieren. Österreich ist in dieser Hinsicht das Schlusslicht Europas – wir sind die ‚Lulus‘ des Nichtraucherschutzes. Es bleibt uns nichts übrig, als weiter darum zu kämpfen, dass sich diese Situation verbessert.“
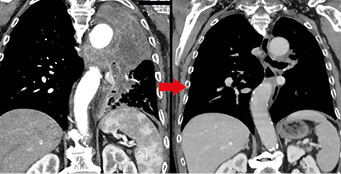
Patient, 71 Jahre mit nichtkleinzelligem Lungenkarzinom
Es handelt sich um ein Adenokarzinom ohne nachweisbare Targets für eine zielgerichtete Therapie und einer PD-L1-Expression von 60 %. Die CT-Bilder zeigen den Verlauf vor und 3 Monate nach Beginn der Erstlinienbehandlung mit Immuntherapie (Pembrolizumab alle 3 Wochen).