Die IgA-Nephropathie (IgAN) ist eine der häufigsten primären Nierenerkrankungen. Trotzdem bleibt sie aufgrund des oftmals oligosymptomatischen Verlaufs wahrscheinlich bei vielen Patient:innen unerkannt. Ein zentraler Aspekt in der Pathogenese ist die Produktion abnormer, galaktosedefizienter IgA1-Moleküle (Gd-IgA1). Der primäre Entstehungsort, die intestinale Mukosa, sowie weitere Beobachtungen deuten auf eine zentrale Rolle des enteralen Immunsystems bei der Pathogenese der IgAN hin. Es bilden sich IgG-Autoantikörper gegen Gd-IgA1 und zirkulierende Immunkomplexe, die sich im Mesangium der Nierenglomeruli ablagern – mit konsekutiver glomerulärer Inflammation, Bildung von mesangialer Matrix und letztlich glomerulärer und interstitieller Fibrose.
Diagnose
Wie schon in der Leitlinie von 2021 betont auch die KDIGO-Leitlinie 2025 zu IgAN und IgAV, dass die Diagnose einer IgA-Nephropathie nur durch eine Nierenbiopsie möglich ist. Es gibt weiterhin keine verlässlichen Blut- oder Urinbiomarker für die Diagnose. Der MEST-C-Score (M = mesangiale Zellvermehrung, E = endokapilläre Zellvermehrung, S = segmentale Sklerose, T = interstitielle Fibrose/tubuläre Atrophie, C = Halbmondbildung) ist ein wichtiger prognostischer Bestandteil und muss beim pathologischen Befund bestimmt werden. Sekundäre Ursachen für eine IgAN müssen ausgeschlossen werden. Neu ist jedoch, dass die Leitlinie 2025 eine großzügigere Haltung zur Durchführung einer Biopsie empfiehlt: Bei allen erwachsenen Personen mit einer Proteinurie ab 0,5 g/Tag (oder einer äquivalenten Urin-Protein-Kreatinin-Ratio [UPCR]) und Verdacht auf IgAN sollte eine Nierenbiopsie in Betracht gezogen werden.
Prognose
Die klinischen Befunde und die histologischen Ergebnisse der Nierenbiopsie sollten genutzt werden, um das Risiko der Patient:innen mithilfe des International IgAN Prediction Tool einzuschätzen. Dieses Tool gibt es in verschiedenen Versionen – je nach Alter (Erwachsene vs. Kinder) und abhängig davon, wie viel Zeit seit der Biopsie vergangen ist.3–5
Zur Abschätzung der Prognose stehen weiterhin im Wesentlichen nur die eGFR und die Proteinurie zur Verfügung.
In der Leitlinie 2025 wird erneut betont, dass weder das International IgAN Prediction Tool noch der MEST-C-Score dafür geeignet sind, die Wirkung einer bestimmten Therapie vorherzusagen. Sie sollten daher aktuell nicht verwendet werden, um konkrete Therapieentscheidungen zu treffen.
Die histologischen Befunde – insbesondere Halbmonde – müssen immer gemeinsam mit den klinischen Informationen bewertet werden. Am wichtigsten ist dabei, wie schnell sich die eGFR verändert.
Zentral: neues duales Therapiekonzept
Das Ziel der Behandlung ist es, den Verlust der Nierenfunktion auf weniger als 1 ml/min pro 1,73 m2 pro Jahr bei den meisten Erwachsenen zu verlangsamen und diesen Zustand langfristig zu erhalten. Der einzige zuverlässige frühe Biomarker, der aktuell zur klinischen Entscheidungsfindung genutzt werden kann, ist die Proteinurie. Nachdem neuere Daten zeigten, dass schon geringere Eiweißmengen als 1 g/Tag im Urin das lebenslange Risiko für ein Nierenversagen deutlich erhöhen6, wurde das Ziel in den aktuellen Richtlinien gesenkt: Proteinurie <0,5g/Tag, möglichst < 0,3 g/Tag (oder adäquater UPCR-Wert), unabhängig davon, ob eine spezifische Therapie läuft oder nicht.
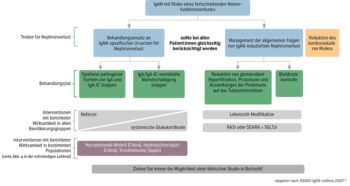
Ausgesprochen neu ist der Fokus auf ein duales Therapiekonzept, das auf Immunologie und CKD-Entwicklung bei IgAN abzielt. Dabei geht es darum:
- die Bildung von IgA-haltigen Immunkomplexen und deren schädigende Wirkung auf die Glomeruli zu verhindern oder zu verringern und
- die Folgen des bereits bestehenden Nephronverlustes durch IgAN zu behandeln und zu kontrollieren; das umfasst neben den ACE-Hemmern bzw. Angiotensin-Rezeptor-Blockern und SGLT2-Hemmern auch nichtmedikamentöse Maßnahmen wie Empfehlungen zum Lebensstil und zu einer Blutdruckeinstellung auf etwa ≤120/70mmHg.
Beide Aspekte sollen gemeinsam berücksichtigt werden, um den Krankheitsverlauf möglichst gut zu beeinflussen (Abb.).
Behandlung der IgAN
Um eine Remission der IgAN zu erreichen, muss auch der immunologische Anteil der Erkrankung behandelt werden. Die neue KDIGO-IgAN-Leitlinie 2025 rät zu einer 9-monatigen Behandlung mit Nefecon bei Patient:innen mit erhöhtem Risiko für einen fortschreitenden Verlust der Nierenfunktion. In der EU ist Nefecon für die Behandlung erwachsener Patient:innen mit primärer IgAN zugelassen, wenn die Eiweißausscheidung im Urin ≥ 1 g/Tag beträgt (bzw. UPCR ≥0,8g/g).7, 8
Alternativ kann eine systemische Glukokortikoidtherapie in reduzierter Dosis, kombiniert mit einer antimikrobiellen Prophylaxe, durchgeführt werden, basierend auf der TESTING-Studie: Methylprednisolon (oder äquivalent) 0,4 mg/kg/Tag, maximal 32 mg/Tag für 2 Monate, danach Dosisreduktion um 4 mg pro Monat, insgesamt über 6–9 Monate.
Behandlung der CKD bei IgAN
Zum Zeitpunkt der Diagnose haben die meisten Patient:innen mit IgAN bereits eine mehr oder weniger fortgeschrittene, aber eindeutig bestehende chronische Nierenkrankheit (CKD). Alle Patient:innen mit IgAN müssen deshalb mit einer maximal zugelassenen oder tolerierten Dosierung eines ACE-Hemmers oder eines Angiotensin-Rezeptor-Blockers behandelt werden.
Neu ist die Empfehlung, Patient:innen mit erhöhtem Risiko für einen fortschreitenden Verlust der Nierenfunktion bei IgAN mit Sparsentan – einem dual wirkenden Endothelin- und Angiotensin-Rezeptor-Antagonisten – zu behandeln.9, 10 In der EU ist Sparsentan zur Behandlung bei einer Proteinurie von ≥ 1,0g/Tag (oder einer UPCR von ≥ 0,75 g/g) zugelassen.Wichtig: Sparsentan ersetzt eine RAS-Blockade und soll nicht gleichzeitig mit einem ACE-Hemmer oder AT1-Rezeptor-Blocker verwendet werden. Die ÖGN hat schon 2023 basierend auf den Daten aus der DAPA-CKD-Studie den Einsatz von SGLT2-Hemmern bei der IgAN empfohlen.11, 12 Mittlerweile sind auch die positiven Subgruppenanalysen zu IgAN-Patient:innen aus der EMPA-KIDNEY-Studie publiziert worden.13 Die KDIGO empfiehlt nun auch erstmals eine Therapie mit einem SGLT2-Hemmer bei Patient:innen, die – allgemein gesprochen – ein erhöhtes Risiko für eine fortschreitende Verschlechterung der Nierenfunktion haben.
Wissenswertes für die Praxis
- Eine Nierenbiopsie wird ab einer Proteinurie > 0,5 g/Tag empfohlen.
- Das International IgAN Prediction Tool wurde sowohl für Erwachsene und für Kinder als auch für unterschiedliche Zeiten seit der Nierenbiopsie validiert.
- RAS-Blockade bis zur maximal zugelassenen oder tolerierten Dosis für alle Patient:innen mit IgAN
- Weitere Therapieoptionen: SGLT2-Hemmer, Sparsentan, Nefecon (und evtl. Steroid)
- Die Therapieziele wurden nachgeschärft: jährlicher eGFR-Abfall < 1 ml/min pro 1,73 m2, Proteinurie < 0,5 g/Tag (ideal < 0,3 g/Tag)