Die Colitis ulcerosa (CU) zählt zusammen mit dem Morbus Crohn zu den chronisch entzündlichen Darmerkrankungen. Im Gegensatz zum Morbus Crohn, der den gesamten Gastrointestinaltrakt segmental betreffen kann, ist die CU als kontinuierliche Entzündung vom Rektum ausgehend auf das Colon beschränkt. Die komplexe Pathogenese ist derzeit nicht vollständig verstanden, es gilt mittlerweile aber als gesichert, dass die Erkrankung durch ein Zusammenspiel von genetischen Faktoren, Umwelteinflüssen, Veränderungen des Mikrobioms und einer fehlregulierten Immunaktivierung entsteht.
Klinik und Diagnose
Die Symptome der CU sind vielfältig und hängen maßgeblich vom Ausmaß und von der Schwere der Entzündung ab. Das typische Leitsymptom ist die blutige Diarrhö mit abdominellen Schmerzen bzw. Tenesmen. Bei einer isolierten Proktitis kann jedoch die Diarrhö fehlen, und es kommt ausschließlich zu blutigem Stuhlgang.
Zusätzlich kann es zu extraintestinalen Manifestationen mit u.a. Beteiligung von Haut, Gelenken und Augen kommen. Die Diagnosestellung erfolgt neben dem Ausschluss einer infektiösen Genese durch die Zusammenschau von Klinik, Biomarkern, Endoskopie, Histologie und Bildgebung.
Therapie: von Steroiden bis Biologika
Die Therapie der CU wurde seit der Erstbeschreibung der Erkrankung stark erweitert und entwickelt sich rasch weiter. Der erste Meilenstein war die Entdeckung der Wirksamkeit von Steroiden bei der akut schweren CU 1955, welche die Mortalität der Erkrankung drastisch reduzierte. Im Laufe der nächsten Jahrzehnte wurden neben Sulfasalazin und Mesalazin auch Immunsuppressiva wie Azathioprin, 6-Mercaptopurin und Methotrexat etabliert.
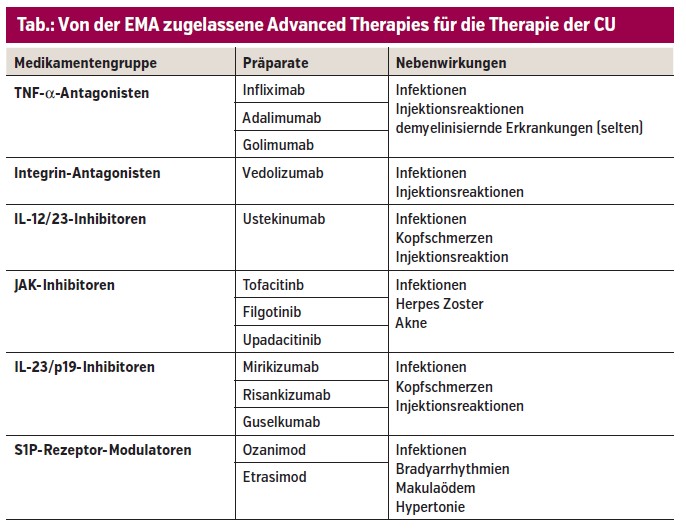
Während Mesalazin weiterhin die Basistherapie der milden bis moderaten CU darstellt, hat die Verwendung der übrigen vorher genannten Medikamente aufgrund neuerer Therapieoptionen mit günstigerem Nebenwirkungsprofil, die unter dem Oberbegriff der „Advanced Therapies“ zusammengefasst werden, stark nachgelassen. Angefangen hat dies mit der Einführung der monoklonalen Antikörper (Biologika) mit den TNF-α-Inhibitoren Infliximab, Adalimumab und Golimumab. Mit dem Integrin-Antagonisten Vedolizumab, dem IL-12/23-Antikörper Ustekinumab, den oralen JAK-Inhibitoren Tofacitinib (unselektiv), Upadacitinib und Filgotinib (selektive JAK-1-Inhibition), den Sphingosin-1-Phosphat-(S1P-)Rezeptor-Modulatoren Ozanimod und Etrasimod sowie den neuen IL-23-Antikörpern Mirikizumab, Risankizumab und Guselkumab steht nun eine Vielzahl an möglichen Therapieformen zur Verfügung (Tab.).
Die Auswahl des jeweiligen Präparates wird in Abhängigkeit vom Ausmaß und Schweregrad der Erkrankung (unter Berücksichtigung extraintestinaler Manifestationen), vom Ansprechverhalten auf Vortherapien, von Vorerkrankungen und dem Alter sowie von individuellen Patientenwünschen (z.B. Kinderwunsch, Wünsche bzgl. der Applikationsform) getroffen. Im Falle eines mehrfachen Therapieversagens steht mit der Kolektomie eine radikale, aber wirksame Therapieoption zur Verfügung. Zunehmend rückt auch die Appendix bei der CU in den Fokus. Die Entfernung dieser kann nach neuester Datenlage das Risiko für das Auftreten eines neuerlichen Schubes deutlich reduzieren.
CU und Schwangerschaft
Ein wichtiger Punkt in der Behandlung ist auch das Thema der Schwangerschaft. So gibt es mittlerweile belastbare Daten, dass eine aktive Erkrankung mit einem erhöhten Risiko für Frühgeburtlichkeit und für ein geringeres Geburtsgewicht einhergeht. Besteht ein Kinderwunsch, sollte frühzeitig ein Therapiekonzept ausgearbeitet werden. Mit Ausnahme von JAK-Inhibitoren und S1P-Rezeptor-Modulatoren kann in den meisten Fällen eine Fortführung der medikamentösen Therapie außerhalb des Labels empfohlen werden, um das Risiko für Schübe während der Schwangerschaft zu verringern.
Konklusion
Trotz moderner Therapieoptionen bleibt die Behandlung der CU eine Herausforderung und erfordert auf Grund der sich rasch entwickelnden therapeutischen Palette eine zunehmende Spezialisierung.