Nierenschädigung als Komplikation eines Diabetes mellitus (DM) ist leider häufig und umfasst chronische, aber auch akute Verlaufsformen. Eingeschränkte Nierenfunktion bei Diabetes kann durch diabetische Nierenschädigung ausgelöst sein oder auch andere Ursachen haben. Niereninsuffizienz hat immer Auswirkungen auf die medikamentöse Therapie, die Patient:innen mit DM einnehmen. Sie erfordert zumindest eine Überprüfung der Dosierungen oder allfälliger Kontraindikationen. Hier wird im Wesentlichen auf die antidiabetische und die antihypertensive Behandlung eingegangen.
Akut könnte gemäß „sickday medication guidance“1 eine Medikamentenpause gerechtfertigt sein. Bei chronischer Nierenschädigung kann eine Dosisadaptierung erforderlich werden. Manche Medikamente sind unabhängig von der Niereninsuffizienz zu dosieren, andere sind kontraindiziert. Das Absetzen mancher Medikamente kann für die Patient:innen auch von Nachteil sein.
Renale Auswirkungen der Diabetestherapie
Eine Auswertung der Auswirkungen von Antidiabetika auf Parameter wie Nephropathieinzidenz, Auftreten einer Albuminurie/Proteinurie, Krankheitsprogression oder Tod renaler Ursache ergibt ein heterogenes Bild.2 Die Studienlage vergleichend zu beurteilen ist schwierig, zumal „Nieren-Endpunkte“ in den Studien nicht einheitlich definiert sind. Auch die Verwendung zusammengesetzter Endpunkte in Studien macht die Einschätzung bestimmter Antidiabetika schwierig. Nicht selten werden signifikante Studienresultate bei Verwendung „zusammengesetzter Endpunkte“ letztlich von einem einzigen Outcome getrieben, beispielsweise Makroalbuminurie3, nicht aber von für Patient:innen unmittelbar relevanten Ereignissen wie notwendigem Dialysebeginn.
Dosisanpassungen je nach Nierenfunktionseinschränkung bzw. Kontraindikationen sind in den jeweiligen Fachinformationen gut dargestellt. Daher soll hier auf Medikamente eingegangen werden, die in „Sickday medication guidance“-Listen1 enthalten sind. Natürlich wird auch auf Besonderheiten der Medikation bei chronischer Niereninsuffizienz eingegangen.
Metformin. In Diabetes-Leitlinien wird Metformin immer noch als erstes zum Einsatz kommendes Medikament genannt.4, 5 Standarddosierungen liegen bei bis zu 2.000 mg/Tag. Es wirkt appetithemmend und weist eine Reihe pleiotroper Wirkungen auf. Bei Nierenfunktionseinschränkung ist eine Dosisreduktion auf 500–1.000 mg/Tag angezeigt, und es ist auf das Risiko einer Laktatazidose zu achten.
SGLT2-Hemmer. Diese Substanzgruppe wird aufgrund ihrer zusätzlich organprotektiven Effekte vor allem auf Nieren und Herz mittlerweile als antidiabetische Option mit Metformin genannt5, neuere Leitlinien empfehlen den parallelen Beginn von Metformin und SGLT2-Hemmern.6 Zu erwähnen ist, dass unter SGLT2-Hemmern das (seltene) Phänomen einer euglykämischen diabetischen Ketoazidose beschrieben wurde.7 Davon abgesehen sind SGLT2-Hemmer aber tatsächlich als protektiv anzusehen, schwere unerwünschte Ereignisse insgesamt und akute Nierenschädigung waren unter SGLT2-Hemmern deutlich seltener zu beobachten.8 Eine ganz aktuelle Praxisleitlinie empfiehlt somit letztlich für fast alle Patient:innen mit chronischer Nierenerkrankung mit und ohne Diabetes die Gabe von SGLT2-Hemmern.9
Inkretinmimetika. GLP-1-Rezeptoragonisten (RA) werden bei bestimmten Kollektiven als Alternative zu SGLT2-Hemmern genannt4,5, sie haben ebenfalls nephroprotektive Wirkung gezeigt.3 Außerdem werden sie als erste zu injizierende Therapie, noch vor Insulin, empfohlen.4 Auch eine Kombination SGLT2-Hemmer/GLP-1-RA ist wegen möglicher additiver organschützender Effekte bereits in Diskussion. Wegen noch geringer Erfahrung ist die Anwendung bei hochgradiger Niereninsuffizienz (noch) nicht generell empfohlen.
Spannend wird die nahe Zukunft in Bezug auf duale GIP/GLP-1-RA. Tirzepatid ist potent blutzuckersenkend und bewirkt eine deutliche Gewichtsreduktion bei niedrigem Hypoglykämierisiko.10 Auch diese Substanz zeigt Nephroprotektion mit Reduktion einer Albuminurie und Verlangsamung des eGFR-Verlustes über die Beobachtungszeit.11 Eine Dosisanpassung ist bei eingeschränkter Nierenfunktion laut Fachinformation nicht erforderlich, es wird zu Vorsicht bei hochgradiger Nierenfunktionsstörung bzw. bei dialysepflichtigen Patient:innen geraten.
Was ist bei der Bluthochdrucktherapie zu beachten?
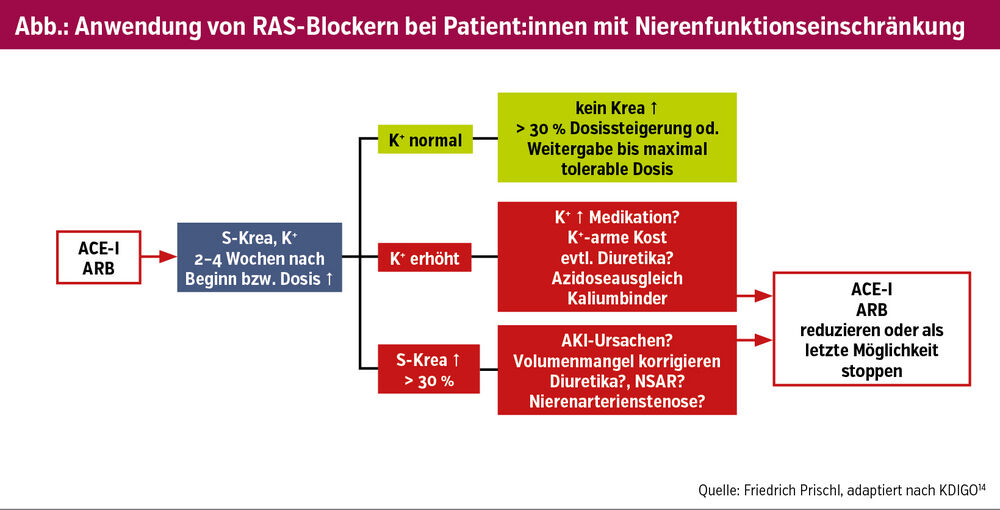
Hypertonie ist ein wichtiger Risikofaktor für die Progression der Niereninsuffizienz und muss therapiert werden. Laut dem Österreichischen Blutdruckkonsens12 und aktuell auch den europäischen Leitlinien13 soll die Behandlung mit ACE-Hemmern oder ARB begonnen werden, typischerweise in Kombination mit einem zweiten Medikament, z. B. Amlodipin. Selbiges gilt für Nierenpatient:innen, besonders auch bei diabetischer Nephropathie.6 Bei Anwendung der Blocker des Renin-Angiotensin-Systems (RAS) ist aber etwas Aufmerksamkeit der Behandler:innen erforderlich (Abb.).
Der Algorithmus ist adaptiert nach den Empfehlungen der KDIGO Working Group14 und soll bei Patient:innen mit Niereninsuffizienz zu deren Sicherheit beachtet werden. Bei Beginn mit RAS-Blockern wie bei Dosissteigerung sollen nach 2–4 Wochen die Nierenfunktion und das Serum-Kalium kontrolliert werden. Die weitere Vorgangsweise folgt dem Algorithmus. Beenden einer RAS-Therapie sollte möglichst vermieden werden, zumal diese eine organprotektive und lebensverlängernde Wirkung gezeigt hat.
Absetzen/Pausieren von Medikation
Aus nephrologischer Sicht konzentriert sich alles auf die Nephroprotektion. Anerkannte Indikatoren sind Rückgang der Albuminurie/Proteinurie, verzögerter Verlust an Nierenfunktion, gemessen an der geschätzten glomerulären Filtrationsrate (eGFR). Harte Endpunkte wie Dialysepflichtigkeit oder Tod aus renalen Ursachen werden teilweise ebenfalls durch moderne Therapien reduziert.
Rezent wurde eine Kohortenstudie über 96.345 Patient:innen mit SGLT2-Hemmern oder GLP-1-RA publiziert, die Therapiepausen/-abbruchsraten, Gründe für die Unterbrechung und ihre Auswirkungen erhob. Bei mehr als einem Drittel der Patient:innen wurde die Therapie pausiert, vor allem aufgrund zerebrovaskulärer, peripher atherosklerotischer oder koronar-ischämischer Ereignisse. Es zeigte sich, dass bei Pausieren von SGLT2-Hemmern ≥ 180 Tage Ereignisse wie Tod um 67 % und Hospitalisierung wegen Herzinsuffizienz um 26 % häufiger beobachtet wurden. Bei Pausieren von GLP-1-RA lagen die Prozentsätze bei 97 % und 48 %. Längeres Pausieren oder Absetzen dieser organprotektiven Medikamente ist also nicht vorteilhaft, sondern sogar schädlich.15
Für die Therapie mit RAS-Blockern gilt Ähnliches. Bei Patient:innen mit einer eGFR <30ml/min/1,73m2 und RAS-Blocker-Therapie wurde analysiert, ob die Fortführung der RAS-Blockade oder ein Absetzen im Stadium G4 und G5 einen Unterschied ausmacht, ob sich RAS-Blocker bei hochgradiger Nierenfunktionseinschränkung nachteilig auswirken. Es zeigte sich, dass kein signifikanter Unterschied nach 3-jähriger Beobachtungszeit besteht. Numerisch lag die eGFR bei RAS-Therapie-Fortsetzung sogar minimal über jener der Patient:innen, welche die RAS-Blockade beendet hatten.16
Diese Studien zeigen, dass bei aller Vorsicht hinsichtlich Medikation und Dosierung bei eingeschränkter Nierenfunktion auch daran zu denken ist, dass Patient:innen durch (gut gemeintes) Absetzen sogar eine organprotektive Wirkung durch SGLT2-Hemmer oder RAS-Blocker vorenthalten wird.