Highlights beim Multiplen Myelom
SHORT CUT
|
Auch heuer wurden am Kongress der European Hematology Association, der dieses Jahr virtuell stattfand, zahlreiche neue Daten und Studien zum Multiplen Myelom vorgestellt. Nicht nur im Setting des neudiagnostizierten Multiplen Myeloms (NDMM), sondern auch im rezidivierten/refraktären Setting (RRMM) gab es einige wichtige Präsentationen. Im Folgenden werden einzelne Studien nach subjektiver Auswahl kurz charakterisiert.
Neudiagnostiziertes Multiples Myelom (NDMM)
Transplant-geeignete und transplant-ungeeignete Patienten
TOURMALINE-MM2, ELOQUENT-1: In den letzten Monaten vor der EHA 2020 haben einige Kongresse und Meetings stattgefunden, wo bereits wichtige Daten und Studien zum Multiplen Myelom präsentiert wurden. Erwähnenswert aus meiner Sicht ist, dass es sich gehäuft um Ergebnisse von großen Phase-3-Studien handelte, die allesamt negativ ausgingen bzw. gescheitert sind. So z. B. die TOURMALINE-MM2-Studie, in der Ixazomib zusätzlich zum Backbone Revlimid/Dexamethason zu keiner Verbesserung des Outcomes im NDMM transplant-ungeeigneten Setting führte, oder auch die ELOQUENT-1-Studie (Backbone Revlimid/Dexamethason mit/ohne Elotuzumab), in der die Zugabe von Elotuzumab ebenfalls zu keinem Benefit im Sinne eines verbesserten PFS/OS führte.
ENDURANCE: Am ASCO wurde in der Late-Breaking-Abstract-Session die viel diskutierte ENDURANCE-Studie vorgestellt, in der zwei Triplets als Induktionstherapie, nämlich KRd (Kyprolis/Revlimid/Dexamethason) vs. VRd (Velcade/Revlimid/Dexamethason), in einem direkten Head-to-Head-Vergleich untersucht wurden. Eingeschlossen wurden hier sowohl transplant-ungeeignete als auch transplant-geeignete Patienten mit Standardrisiko-Zytogenetik. Eine Überlegenheit von Kyprolis in der Dreierkombination (gemessen am PFS nach Induktion und 3-Jahres OS) konnte allerdings nicht gezeigt werden, sodass die Autoren hier die Kombination VRd weiterhin als Standard of Care (SoC) in der Induktionsphase angeben.
GMMG-HD6, SWOG 1211: Am EHA schien sich dann diese Negativserie in einigen Studien fortzusetzen: In einer Studie der deutschen Studiengruppe GMMG-HD6 bei transplant-geeigneten NDMM-Patienten (Abstr. #S203) kam es durch die Zugabe von Elotuzumab zu VRd in der Induktionsphase zu keinem verbesserten Ansprechen, allerdings kann noch keine Aussage zum PFS getroffen werden. Auch in der Phase-2–Studie SWOG-1211 (Abstr. #S201) konnte durch die Zugabe von Elotuzumab zu VRd in der wichtigen Untergruppe des Hochrisiko-transplant-geeigneten-NDMM kein Benefit hinsichtlich PFS/OS nach Induktion und Erhaltungstherapie erzielt werden. Allerdings sind die Outcome-Daten insgesamt besser als erwartet, sodass die Kombination eines Proteasomeninhibitors gemeinsam mit einem IMiD in der Erhaltungstherapie für Patienten mit Hochrisiko-Zytogenetik günstig erscheint.
UNITO-EMN10: Dr. Mina präsentierte eine ebenfalls interessante Phase-2-Studie, in der Ixazomib in verschiedenen Kombinationen als Induktionstherapie über 9 Zyklen bei älteren transplant-ungeeigneten NDMM-Patienten untersucht wurde (Abstr. #S202). Keiner der vier Arme erreichte den vordefinierten Endpunkt eines PFS von mind. 65 % nach 2 Jahren (medianes Follow-up: 18,2 Monate; PFS: 10,5‒23 Monate), auch die VGPR-Raten blieben hinter den Erwartungen zurück.
MASTER: Natürlich gab es aber nicht nur Negativstudien, sondern auch beeindruckende positive Studien, v. a. in Kombinationen mit monoklonalen CD38-Antikörpern. So z. B. das MASTER trial (Abstr. #EP928), in dem Daratumumab mit KRd kombiniert wurde und zu noch nie dagewesenen MRD-Negativitätsraten von bis zu 83 % nach Konsolidierung führte. Dabei ist wichtig zu erwähnen, dass diese Ergebnisse unabhängig davon waren, ob bei den Patienten eine Standardrisiko- oder Hochrisiko-Zytogenetik vorlag.
GMMG-CONCEPT: Die von Dr. Weisel präsentierte Phase-2-Studie, die Isatuximab mit KRd kombinierte und ausschließlich Hochrisiko-Patienten (mit transplant-geeignetem/transplant-ungeeignetem NDMM) inkludierte, zeigte 100 % Ansprechraten (ORR) mit über 90 % VGPR-Raten oder besser sowie ebenfalls beeindruckende 67 % MRD-Negativitätsraten (Abstr. #S204). Diese Daten sind sehr wichtig, da MRD-Negativität derzeit der einzige gute prognostisc he Marker bei Hochrisiko-Patienten ist, der auf ein besseres Outcome schließen lässt.
AGMT-MM2: Ein weiterer wichtiger Beitrag war auch eine Subgruppenanalyse der AGMT-MM2-Studie (KRd vs. KTd bei transplant-ungeeignetem NDMM), präsentiert von Professor Ludwig, in der sehr gute Effektivitätsdaten gezeigt werden konnten, unabhängig vom zytogenetischen Risikoprofil. Diese Ergebnisse sprechen dafür, dass möglicherweise eine Kombinationstherapie mit dem Proteasomeninhibitor Kyprolis den negativen Einfluss einer Hochrisiko-Zytogenetik überwinden kann.
Tourmaline-MM4: Auch die Tourmaline-MM4–Studie (Abstr. #S200) muss erwähnt werden, in der eine Erhaltung mit Ixazomib bei älteren transplant-ungeeigneten NDMM-Patienten nach Standardinduktion untersucht wurde. Es fand sich ein klarer Vorteil einer Ixazomib-Erhaltung vs. Placebo. Festgehalten werden muss allerdings, dass eine Erhaltungstherapie mit Lenalidomid derzeit SoC ist (und auch deutlich bessere Ergebnisse in vorangegangenen Studien erzielte). Für Patienten aber, die kein Revlimid erhalten können, stellt Ixazomib durchaus eine Option/Alternative dar.
Relapsiertes/refraktäres Multiples Myelom (RRMM)
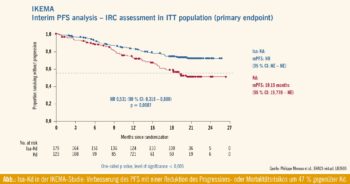
IKEMA: In diesem Setting nehmen sicherlich die Ergebnisse der IKEMA-Studie einen wichtigen Platz ein, die in der Late-Breaking-Session vorgestellt wurden (Abstr. #2603). Der monoklonale Antikörper Isatuximab, welcher gerade unter dem Handelsnamen Sarclisaâ in der EU zugelassen wurde, zeigt hier beeindruckende Ergebnisse in der Kombination mit Carfilzomib/Dexamethason (Isa-Kd) im Vergleich zu Carfilzomib/Dexamethason (Kd) alleine. Im Median hatten die Patienten 2 Vortherapien, das mediane Follow-up war 20,7 Monate und der primäre Endpunkt das PFS.
Es fand sich ein signifikant verbessertes PFS mit Isatuximab-Kd vs. Kd (NR vs. 19,5 Monate; HR = 0,531), das entspricht einer Reduktion des Risikos für eine Progression von 47 % durch die Zugabe von Isatuximab (Abb.). Dieser Vorteil zeigte sich durchgehend für sämtliche untersuchten Subgruppen wie z. B. Patienten ≥ 65 Jahre, Patienten mit Niereninsuffizienz sowie, ganz wichtig, auch für Patienten mit Hochrisiko-Zytogenetik. Weiters ergaben die Daten aus der IKEMA-Studie ein verbessertes tiefes Ansprechen mit hohen MRD-Negativitätsraten (30 % in der ITT-Population) bei akzeptabler Verträglichkeit und gutem Nutzen-Risiko-Profil. Insgesamt kann daraus geschlossen werden, dass Isa-Kd eine wichtige Lenalidomid-freie Therapieoption für Patienten mit RRMM darstellt.
CANDOR: Eine weitere IMID-freie Kombination, welche auch schon am ASH 2019, ebenfalls in der Late-Breaking-Abstract-Session, vorgestellt wurde, ist Daratumumab-Kd im Rahmen der CANDOR-Studie (Abstr. #EP938). Die gute Wirksamkeit und der klare Benefit für die Dreier-Kombination wurden bereits gezeigt (PFS: NR vs. 15,8 Monate; HR = 0,63) und jetzt am EHA 2020 hinsichtlich der Anzahl der Vortherapien ausgewertet und präsentiert. Es zeigten sich in sämtlichen Subgruppen zueinander konsistente Ergebnisse bezüglich der Wirksamkeit und Verträglichkeit. DKd erbrachte einen Benefit für die Patienten unabhängig von der Zahl der vorausgegangenen Rezidive und auch unabhängig von vorheriger Exposition und Ansprechen auf Lenalidomid oder Bortezomib. Auch die MRD-Negativitätsraten konnten durch die Dreier-Kombination verbessert werden.
FAZIT: Aus diesen beiden Studien lässt sich somit ableiten, dass IMID-freie Kombinationen im RRMM-Setting sehr effektiv sein können und eine Kombination eines CD38-Antikörpers mit einem Proteasomeninhibitor wie Kyprolis sinnvoll erscheint.
BELLINI, OPTIMISMM, DREAMM-2: Weiters gab es noch eine Reihe an interessanten Updates und Subgruppen-Analysen von großen Studien, die bereits auf vorherigen Kongressen und Meetings präsentiert wurden, darunter ein Update zur BELLINI–Studie (Abstr. #EP939, Abstr. #EP975; Venetoclax + Bortezomib/Dexamethason) mit hohen MRD-Negativitätsraten (46 %) oder auch ein Update zur OPTIMISMM-Studie (Abstr. #EP957, Abstr. #EP1015; Pomalidomid + Bortezomib/Dexamethason) und DREAMM-2-Studie (Abstr. #EP1037, Abstr. #EP1006; Belantamab mafodotin als Monotherapie), in denen Hochrisiko-Zytogenetik- sowie renal eingeschränkte Patienten ein verbessertes Outcome durch die Dreierkombination bzw. zu testende Substanz hatten.
Innovationen in Phase-1-Studien
Aus meiner Sicht gab es auch einige spannende Daten aus frühen Phase-1-Studien.
Mit TAK-079 (Abstr. #EP931), einem neuen subkutanen CD38-Antikörper, der schon letztes Jahr präsentiert wurde und eine gute Verträglichkeit und niedrige hämatologische Toxizität zeigte, ist bereits eine Phase-2-Studie geplant. Neuartige Substanzen/Konstrukte zeigen vielversprechende Resultate (Interimsanalyse des BCMA/CD3 2+1 T-cell engagers CC-93269) (Abstr. #S205), auch wenn bisher nur wenige Patienten eingeschlossen wurden und die CRS-Raten und infektiösen Komplikationen zu beachten waren (ORR: 89 %; MRD-Negativitätsraten: 78 %). In diesem Zusammenhang interessant war auch die Präsentation zu Teclistamab (humanisierter BCMA-CD3-bispezifischer Antikörper), der ebenfalls hervorragende Effektivitätsdaten (ORR: 78 %) mit vergleichsweise niedrigeren Raten an schweren CRS Grad 3 oder höher zeigte.
Update CAR-T-Zelltherapien
Auch die Updates zu CAR-T-Zelltherapien sollen nicht unerwähnt bleiben.
Neue Effektivitätsdaten zu den drei großen BCMA-CART-Zellstudien KarMMa (Abstr. #S209), CARTITUDE-1 (Abstr. #EP926) und EVOLVE (Abstr. #EP927) wurden präsentiert. Die meisten Patienten wurden bisher in KarMMa eingeschlossen und ausgewertet, besonders gute Daten finden sich bei CARTITUDE. Allen Studien gemeinsam ist, dass stark vorbehandelte und auch penta-refraktäre Patienten (30‒40 %) eingeschlossen werden, das Follow-up aber jeweils noch relativ kurz ist.
RESÜMEE
Zusammenfassend kann man sagen, dass sich auf dem Gebiet des Multiplen Myeloms nach wie vor sehr viel Neues ergibt, und das jetzt schon seit einigen Jahren. Es werden laufend neue Substanzen und Therapiekonzepte entwickelt, die allesamt zum Ziel haben, Patienten langfristig in einen krankheitsfreien Zustand bei sehr guter Lebensqualität zu bringen.
Literatur bei der Verfasserin