Relapsiertes Setting – Highlights in der Behandlung
CANDOR-Studie
Klinisch relevant war die sogenannte CANDOR-Studie, die den additiven Einsatz des Anti-CD38-Antikörpers Daratumumab zu einer Backbone-Therapie mit Carfilzomib in Kombination mit Dexamethason (KdD) in einem randomisierten Setting untersuchte.
Studiendesign: In dieser internationalen, multizentrischen Open-Label-Phase-III-Studie wurden 466 Patienten mit r/r MM eingeschlossen. Einschlusskriterien waren 1–3 vorherige Therapielinien, ein ECOG-Status von 0–2, eine Nierenfunktion mit CrCl > 20 ml/min und eine Herzfunktion mit einer LVEF > 40 %. Die Patienten wurden 2:1 randomisiert: 312 Teilnehmer in Arm A mit Carfilzomib/Dexamethason gemäß dem Endeavor-Protokoll (Carfilzomib-Zyklus I: d 1, 2 20 mg/m² i.v., ab dann immer mit 56 mg/m² i. v. d 8, 9, 15, 16 qw 28; Dexamethason 40 mg p.o. wöchentlich) sowie erste Gabe Daratumumab in Split-Dose mit 2 x 8 mg/kg, gefolgt von 16 mg/kg d 1, 8, 15 qw 28; und 154 Teilnehmer in Arm B mit Carfilzomib-Dexamethason ebenfalls im Endeavor-Schema. Die Patienten sollten die Therapie bis zur Erkrankungsprogression oder intolerabler Toxizität erhalten. Primärer Endpunkt dieser Studie war das progressionsfreie Überleben (PFS). Sekundäre Endpunkte waren die Gesamtansprechrate, das Gesamtüberleben (OS) und das Erreichen eines negativen MRD-Status (minimale Resterkrankung). Beiden Gruppen waren gut ausbalanciert, was Patientencharakteristika angeht. Das mediane Alter lag in beiden Gruppen bei 64–65 Jahren, die mediane Anzahl an Vortherapien betrug 2. Circa 16 % der Patienten wiesen in beiden Gruppen eine Hochrisiko-Zytogenetik auf.
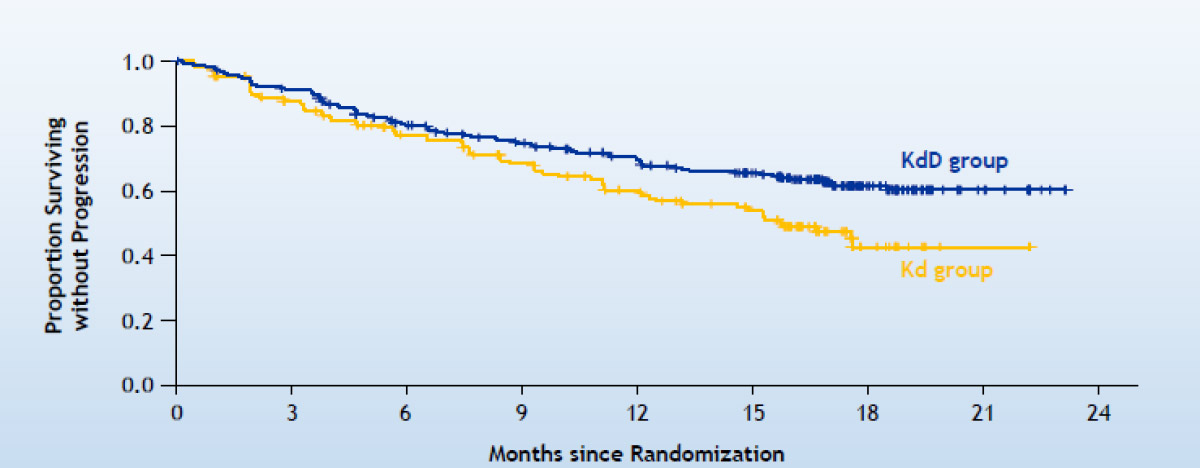
Die Ergebnisse: Das primäre Ziel wurde erreicht: Die Kohorte, die eine Immun-Dreierkombination erhielt, wies ein signifikant verbessertes PFS auf (Abb.). Das mediane PFS im KdD-Arm lag bei einem medianen Follow-up von 17 Monaten bei „nicht erreicht“ gegenüber 15,8 Monaten im Kd-Arm. Was die sekundären Ziele angeht, ist das mediane OS in beiden Armen noch nicht erreicht. Die MRD-Auswertung zeigte nach 12 Monaten eine signifikant tiefere Response mit MRD-negativer CR bei 12,5 % Patienten mit der Dreierkombination im Vergleich zu 1,3 % ohne Daratumumab. Das Nebenwirkungsprofil war in beiden Armen vergleichbar, im Daratumumab-Arm traten jedoch vermehrt Infektionen (insbesondere Pneumonien) auf. Auch hämatologische Nebenwirkungen traten gehäuft im Kombinationsarm mit Daratumumab auf, waren jedoch alle klinisch gut beherrschbar.
Zusammenfassend reduzierte die Zugabe des Anti-CD38-Antikörpers Daratumumab zu einer Backbone-Therapie mit Carfilzomib und Deaxamethason das Risiko einer Progression um 37 %. Die Patienten, die mit KdD therapiert wurden, erreichten im Mittel 10-mal so häufig einen MRD-negativen Status nach 12 Monaten verglichen mit Patienten im Kd-Arm. Das Nebenwirkungsprofil war in beiden Armen vergleichbar und es sind keine neuen, unerwarteten Nebenwirkungen der eingesetzten Medikamente beobachtet worden.
Fazit: KdD ist für Patienten mit refraktärem Multiplem Myelom eine neue, hocheffektive Therapieoption ab der zweiten Therapielinie.