Focus Blase: Demographische Entwicklung bedingt drastischen Anstieg
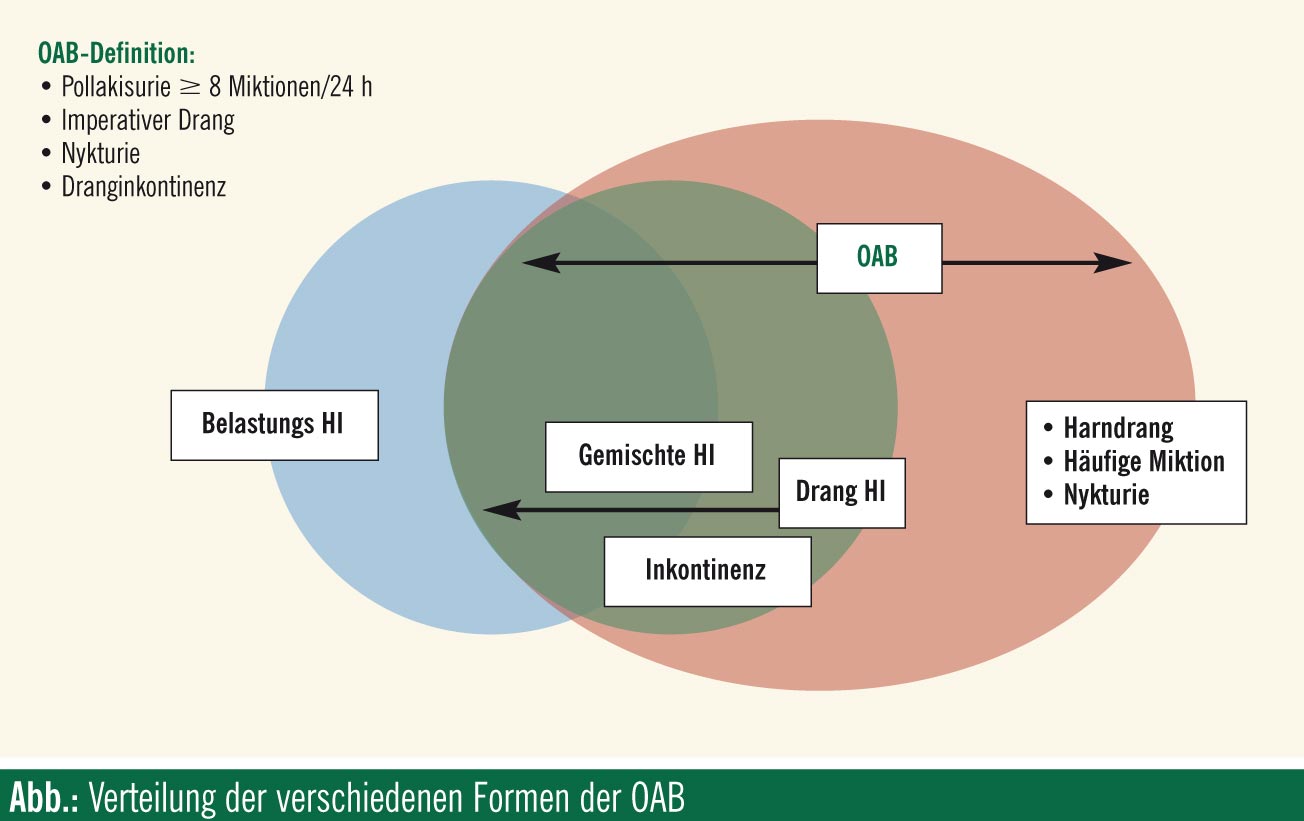
Nach der International Continence Society (ICS) wird die überaktive Harnblase (Overactive Bladder, OAB) als “Drangsymptomatik mit oder ohne Harninkontinenz, mit Pollakisurie (häufiges Wasserlassen) und Nykturie (nächtliches Harnlassen) ohne Vorliegen einer Infektion oder einer anderen augenscheinlichen Pathologie” definiert. Die OAB wird unterteilt in eine OAB trocken (OAB dry): Pollakisurie (> 8-mal/24 Stunden), imperativer Harndrang, Nykturie > 2-mal; und eine OAB nass (OAB wet): umfasst OAB trocken plus Dranginkontinenz. Patienten mit Drang- oder gemischter Belastung/Dranginkontinenz (OAB wet) machen etwa 30% aller OAB-Patienten aus (Abb.).
Die Symptome der OAB sind vor allem im Alter häufig. Bei den > 60-Jährigen sind nahezu gleich viele Männer wie Frauen betroffen, in dieser Altersgruppe gibt jeder Fünfte (unabhängig vom Geschlecht) OAB-Symptome an.
In Österreich leben derzeit etwa 830.000 Menschen mit einer OAB. Bedingt durch die demographische Entwicklung wird diese Zahl in den nächsten 20 Jahren auf fast 1,5 Millionen (!) ansteigen. Eine rezente Studie zum natürlichen Verlauf konnte zeigen, dass es sich bei der OAB um einen dynamischen Prozess mit zum Teil über Jahre stabilen Verläufen, aber auch mit Progressionen und Remissionen handelt.
Pathogenese
Im Wesentlichen können vier Pathomechanismen allein oder in Kombination zu einer überaktiven Harnblase führen 1. vermehrte Afferenzierung, d.h. eine Verstärkung des sensorischen Inputs aus der Harnblase. 2. Mangel an zentralnervöser Kontrolle bzw. bei Defekten der kortikalen Hemmung des Detrusorreflexes: Mb. Parkinson, St. p. Insult, Mb. Alzheimer, Encephalitis disseminata etc. 3. Degenerative Veränderungen der Harnblase (“Aging Bladder”): relativ schlecht charakterisierte Veränderungen des Detrusors der alternden Harnblase. 4. Störungen im Urothel: die erhöhte Durchlässigkeit der Glukosamin-Glycan-Schicht der Schleimhaut vor allem im Alter ermöglicht die vermehrte Reizung der in der Blasenwand liegenden Nervenendigungen.
Diagnostik
Die Basisabklärung von Patienten mit den Symptomen der überaktiven Harnblase entspricht im Wesentlichen der von Patienten mit Miktionsbeschwerden im Allgemeinen. Miktionsfrequenz und Miktionsvolumina werden am besten mittels eines Miktionsprotokolls über 48 Stunden quantifiziert. Eine rezente Untersuchung konnte zeigen, dass Frauen die Tagesmiktionsfrequenz (im Gegensatz zur Nykturie) zum Teil deutlich überschätzen, dies unterstreicht die diagnostische Wertigkeit des Miktionsprotokolls. Eine sonographische Restharnkontrolle ist obligat. Die Messung der Blasenwanddicke erlaubt keine zusätzliche Aussage. Eine weitergehende funktionelle Abklärung inkl. Uroflowmetrie, Flow-EMG, Urodynamik ist in der Regel nur bei Patienten nach frustraner Ersttherapie angezeigt.
Therapie
Die Eckpfeiler der Therapie der OAB sind die Verhaltensmodifikation und die medikamentöse Therapie (Tab.). Bei Therapieversagen oder Kontraindikationen für Anticholinergika stehen nichtinvasive Verfahren der Neuromodulation invasive Verfahren (sakrale Neuromodulation, Botox-Injektion, Blasenaugmentation, Harnableitung) zur Verfügung (Tab.).
|
Tab.: Therapieoptionen bei OAB |
||
|---|---|---|
|
Konservative Therapie |
Nicht invasive Neuromodulation |
|
|
|
|
|
Medikamentöse Therapie |
Invasive Therapie |
|
|
|
|
Verhaltensmodifikation
Auf der Basis des Miktionsprotokolls sollte mit dem Patienten primär eine Modifikation des Trinkverhaltens besprochen werden: exzessive Flüssigkeitszufuhren sollten vermieden werden, eine Flüssigkeitszufuhr von 1.500-2.000 ml/24 Stunden ist in der Regel ausreichend; steht die Nykturie im Vordergrund, sollten größere abendliche Trinkmengen vermieden werden. Eine Umstellung der Medikation (z.B. Diuretika) sollte in Betracht gezogen werden.
Beim Toiletten- bzw. Blasentraining sollten zunächst die Miktionsintervalle verkürzt werden (Miktion nach der Uhr), damit der Zeitpunkt der terminalen, nicht mehr kontrollierbaren Detrusorüberaktivität (die zur Dranginkontinenz führt) nicht erreicht wird. Im nächsten Schritt sollten dann die Miktionsintervalle schrittweise wieder verlängert und damit die Blasenkapazität erhöht werden kann.
Medikamentöse Therapie
Anticholinergika: Seit über 20 Jahren sind Anticholinergika der Eckpfeiler der medikamentösen Therapie bei überaktiver Harnblase. Anticholinergika führen bei 50-70% der Patienten zu einer Besserung der Symptome (cave: deutlicher Placeboeffekt). Grundsätzlich unterscheiden sich Anticholinergika in ihrer Wirkung nur marginal, der tatsächliche Erfolg kann aber erst nach 4-6 Wochen kontinuierlicher Therapie abgeschätzt werden.
Hinsichtlich der Nebenwirkungsrate bestehen deutlich Unterschiede, diese betreffen vor allem Mundtrockenheit (20-30%) und Obstipation (15-20%).
Diese relativ hohe Nebenwirkungsrate ist eine wesentliche Ursache für die schlechte Compliance (über 50% der Patienten brechen die Therapie innerhalb von 12 Monaten ab). Im Vergleich zum Klassiker Oxybutynin zeigen neuere Präparate wie Tolterodin, Trospiumchlorid und M3-selektive Präparate (Solifenacin) eine bessere Verträglichkeit. Retardpräparate zeichnen sich ebenfalls durch eine bessere Verträglichkeit aus. Das Oxybutyninpflaster bietet auf Grund der langsamen Wirkstoffabgabe ebenfalls eine gute Verträglichkeit.
Vor allem in der geriatrischen Bevölkerung können ZNS-Nebenwirkungen (Schläfrigkeit, Konzentrationsschwäche, Halluzinationen, delirante Zustände) unter Anticholinergika auftreten. Die Passage von Anticholinergika durch die Blut-Hirn-Schranke ist nicht einheitlich. Auf Grund der ZNS-Nebenwirkungen gilt das orale Oxybutynin in der geriatrischen Population heute als obsolet.
Die bessere Verträglichkeit moderner Anticholinergika ermöglicht eine flexible Dosierung, d.h. bei Nichtansprechen sollte zunächst – bei tolerablen Nebenwirkungen – eine Dosissteigerung durchgeführt werden.
Topische Östrogentherapie: Bei Frauen in der Menopause ist eine topische Östrogentherapie (E2-haltige Vaginalsuppositorien, 1 täglich für 2-3 Wochen, dann als Erhaltungstherapie 2/Woche) angezeigt. Über die gesteigerte Proliferation des urethralen Epithels, die venöse Kongestion in der Lamina propria der Harnröhre und eine erhöhte β-adrenerge Sensitivität kommt es zu einer (moderaten) Besserung der Symptomatik, urodynamische Veränderungen wurden keine nachgewiesen.
Alternative medikamentöse Ansätze: Werden Anticholinergika nicht vertragen oder bestehen Kontraindikationen (Engwinkelglaukom), können als medikamentöse Alternativen auch trizyklische Antidepressiva (Imipramin), Spasmolytika, Baclofen, Tetrazepam oder Tizanidin versucht werden. Die diesbezügliche Datenlage ist aber dürftig.
Ein weiterer, derzeit intensiv untersuchter, alternativer Ansatz ist die intravesikale Applikation von Chondroitinsulfat, da ein Defekt der Glykokalix des Urothels als pathogenetischer Co-Faktor für eine OAB angesehen wird.
Die intravesikale Instillation der Neurotoxine Capsaicin und Resiniferatoxin (RTX) führt nach etwa zwei Wochen zu einer Besserung der Symptome, die Wirkung hält für 3-4 Monate an. Beide Präparate sind in Österreich nicht zugelassen, Langzeitdaten fehlen.
Botulinumtoxin
Die intravesikale Applikation von Botulinumtoxin A hat sich in den letzten Jahren zu einer Standardtherapie der neurogenbedingten Detrusorüberaktivität entwi ckelt. Seit 2-3 Jahren wird dieser Ansatz zunehmend auch bei der therapierefraktären, nicht neurogenbedingten OAB eingesetzt. Der Wirkung tritt in etwa 14 Tagen ein, die Wirkdauer beträgt zwischen 6 und 12 Monate, danach ist eine neuerliche Behandlung notwendig. Die wichtigste Nebenwirkung ist eine passagere Harnretention mit der Notwendigkeit einer Harnableitung (intermittierender Katheter, Dauerkatheter), über die alle Patienten aufgeklärt werden müssen. Systemische Nebenwirkungen (allgemeine Muskelschwäche) treten nur ganz selten auf.
Periphere Neuromodulation
Die nichtinvasive, periphere Elektrostimulation mittels Vaginal-, Rektal-, Penisoder Klitoriselektroden führt über eine Erregung des Nervus hypogastricus zu einer direkten Hemmung des Nervus pelvicus und damit zu einer Beruhigung der Blasenaktivität. Diese periphere Neuromodulation wird in der Regel als Heimbehandlung zweimal täglich für 20 Minuten durchgeführt und hat sich seit vielen Jahren bewährt. Eine alternative semiinvasive Methode stellt die Stimulation des Nervus tibialis posterior dar.
Invasive Neuromodulation
Bei dieser Technik werden perkutan von dorsal unter Röntgenkontrolle Elektroden in die Foramina sacralia eingelegt und damit eine sakrale Nervenwurzelstimulation im Bereich S3 durchgeführt. Im Rahmen einer Teststimulation kann bei über 50% der therapierefraktären Fälle eine Besserung der Symptomatik erreicht werden. Die vorgelegten Elektroden werden über einen externen Stimulator für 1-3 Wochen probestimuliert. Spricht der Patient auf diese Probestimulation an, wird in einem zweiten Schritt subkutan ein Schrittmachergenerator implantiert.
Dieser Generator kann perkutan über ein Programmiergerät gesteuert werden.
Blasenersatz/Blasenaugmentation/ Dauerharnableitung
Als Ultima Ratio bietet sich eine Blasenaugmentation mit einem isolierten Dünnoder Dickdarmsegment – in der Regel kombiniert mit einem intermittierenden Selbstkatheterismus – an. Kommt diese Option nicht in Frage, ist die Anlage einer supravesikalen kontinenten (d.h. katheterisierbarer Pouch) oder inkontinenten (d.h. IIeum-Conduit, Transversum-Conduit) Harnableitung möglich.
Take-Home-Message
|
Univ.-Doz. Dr. Stephan Madersbacher, FEBU
Abteilung für Urologie und Andrologie, Sozialmedizinisches Zentrum Ost – Donauspital, Wien























































































