Ästhetische Dermatologie: Hormonelle Effluvien
Androgenetisches Effluvium
Das androgenetische Effluvium (AE) hat mit Abstand die höchste Prävalenz vor allen anderen Effluvien. Sie beträgt für die Alopezie bei Männern altersabhängig 40% bei 40-Jährigen bis zu 65% bei 60-Jährigen. Bei Frauen ist die Inzidenz wesentlich geringer, sie liegt bei 3% im 2. Lebensjahrzehnt und 23-28% zwischen 5. und 7. Jahrzehnt.
Ätiopathogenetisch liegt dem Haarausfall ein genetisch geprägter, androgen induzierter Prozess zu Grunde, der durch eine zunehmende Verkürzung der Haarwuchszyklen in den betroffenen Arealen charakterisiert ist, die über eine regressive Metamorphose von Terminalhaarfollikeln zu Vellushaarfollikeln führen.
Pathogenetisch sind in den Haarfollikeln das Konversionsenzym 5-α-Reduktase und damit sekundär der terminale Androgenmetabolit DHT erhöht. Dieser bindet an den Androgenrezeptor (AR). Der aktivierte AR-Komplex beeinflusst die Transkription und Prozessierung einer Reihe von Proteinen durch Interaktion mit der DNA. Geschlechtsspezifische Unterschiede in der Aktivität dieser Enzyme erklären zum Teil die geschlechtsgebundenen, phänotypischen Unterschiede.
Der Vererbungsmodus ist polygen, die Hauptrolle spielt ein X-chromosomal vererbter AR. Das AR-Gen wird rezessiv vererbt. 2007 wurde ein anderes Gen am X-Chromosom nahe dem AR gefunden – das EDA-2-R-Gen, das am häufigsten mit dem AE assoziiert ist. Genetische Polymorphismen scheinen mit einer vermehrten Wirkung der Sexualhormone einherzugehen. Die geschlechtsspezifischen phänotypischen Unterschiede des AE sind vermutlich durch die geschlechtsspezifischen Unterschiede in den Aktivitäten der Konversionsenzyme (5-α-Reduktase I und II, Aromatase) zu erklären.
Varianten des androgenetischen Effluviums bei Frau und Mann
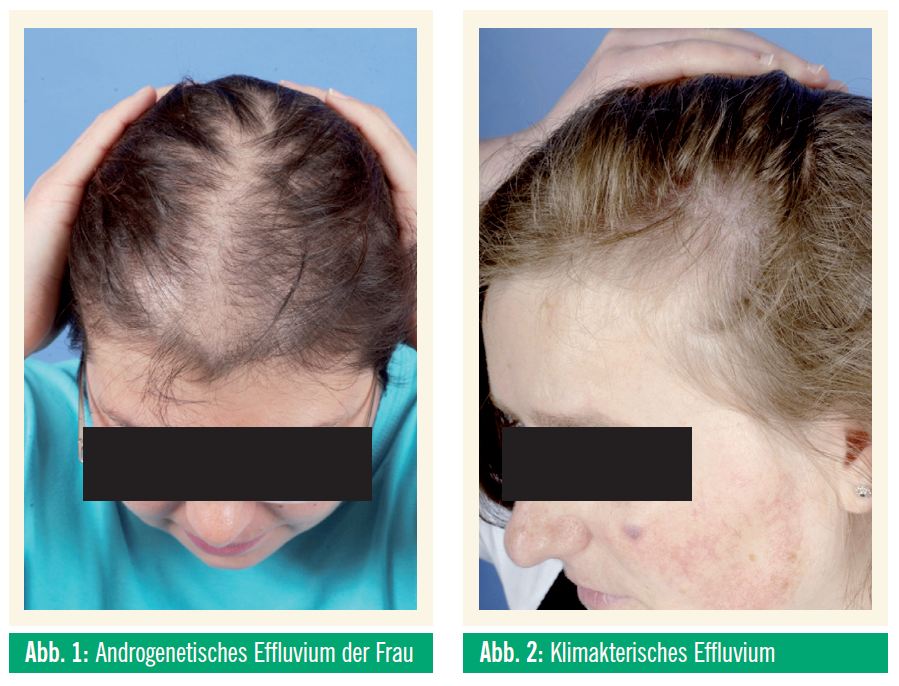
Beim maskulinen Typ (male pattern) wird nach der Hamilton-Norwood-Skala, beim femininen Typ (female pattern) nach dem Ludwig-Schema skaliert (Abb. 1).
Alopecia praecox (praematura): Selten beobachtet man eine Alopecia praecox (praematura) zwischen dem 10. und 20. Lebensjahr. Falls diese bereits vor der Adrenarche auftritt, weist sie ein ausschließlich feminines Muster auf. Das Verhältnis von männlichen zu weiblichen Jugendlichen beträgt 2:1.
Das postpartale Effluvium tritt etwa ab dem 3. Monat post partum auf. Die Geburt bewirkt eine Normalisierung der zuvor erhöhten Östrogenwerte, welche im letzten Trimenon eine Synchronisierung der Haarwuchszyklen in der Anagenphase bewirkt haben. Die Folge ist eine Wiederherstellung der normalen Haarzyklen und damit ein diffuser Haarausfall.
Die Alopecia climacterica (Abb. 2) kann zusätzlich zum gewohnten Bild auch eine Ausdünnung der Haare im Temporalbereich zeigen. Kausal ist ein für die ersten beiden Jahre des Klimakteriums charakteristisches hormonelles Ungleichgewicht zu Gunsten der Androgene. Aber auch eine ungünstige Hormonsubstitution (HRT) mit einer Gestagen-Monotherapie – in welcher Form auch immer – oder eine Kombinationstherapie mit partial androgenen Nebenwirkungen – fördert das hormonelle Effluvium in dieser Lebensphase. In diesem Fall sollen die Gestagenkomponenten im Hinblick auf androgenisierende Partialwirkungen recherchiert werden (Tab.).
Das Hinterfragen der HRT, ggf. deren Absetzen oder Umstellen auf ein z. B. Cyproteronacetat- oder Spironolacton-haltiges Präparat ist hier eine Kausaltherapie (Tab.).
| Tab.: Gestagene/Partialwirkungen | |
|---|---|
| Androgen oder Partialandrogen | Norethisteron (-acetat) NETA Norgestrel Levonorgestrel Desogestrel Norgestimat Tibolon |
| Antiandrogen | Cyproteronacetat Chlormadinonacetat Spironolacton |
Diagnostik: Hormonstatus
Im pillenfreien Intervall werden in der zweiten Zyklushälfte neben den Androgenen (T, A, DHEAS) Kortisol, die Hypophysenhormone LH, FSH und vor allem Prolaktin sowie die Schilddrüsenhormone erfasst. Auf diese Weise sollen ein Prolaktinom, das polyzystische Ovarsyndrom, ein spätmanifestes adrenogenitales Syndrom sowie androgenproduzierende Ovarial- oder Nebennierentumoren ausgeschlossen bzw. verifiziert werden. Zur klinischen Diagnostik ist der Zupftest ausreichend.
Therapie bei Männern
Als allgemeine Maßnahme, die zur Verlängerung der Anagenphase führt, kommt Minoxidil 2-5% zum Einsatz.
Kausaltherapie: Falls mit topischem Minoxidil kein Therapieerfolg erzielt wird, wird Finasterid 1 mg/d gegeben, welches durch eine Blockade der 5-α-Reduktase II kausal wirksam ist. Die fotografisch dokumentierten Unterschiede in den Zuwachsraten betrugen zwischen Finasterid- und Placebo-Gruppe nach 12 Monaten 14%, nach 24 Monaten 16%. Das globale Erscheinungsbild war in der Verum-Gruppe nach 12 Monaten um 48%, nach 48 Monaten um 66% verbessert. Eigenhaartransplantationen durch Spezialisten können in speziellen Fällen von hohem Leidensdruck eine durchaus wertvolle Therapiealternative darstellen.
Therapie bei Frauen
Die Therapie bei Frauen erfolgt durch topische Applikation von 0,025-0,03%igem 17-α-Östradiol. Bei dieser Konzentration kommt es zu keinen systemischen Nebenwirkungen, wenn die tägliche Applikationsmenge rund 3 ml nicht überschreitet. An der Universitätsklinik für Dermatologie Wien empfehlen wir gerne eine magistrale Rezeptur in Kombination mit 3% Minoxidil. Empirisch zeigen sich hier sehr gute Ergebnisse.
Finasterid: In zwei kontrollierten klinischen Studien zeigte Finasterid 1 mg/d (Propecia®) bei Frauen keinen Benefit gegenüber Placebo oder keiner Behandlung. Die Majorität der Studien zeigt keinen Vorteil einer Finasterid-Therapie (die bei Frauen in der fertilen Phase obligat eine Kontrazeption erfordert) gegenüber keiner Therapie.
Antiandrogene: Cyproteronacetat führt in der niedrigen Dosis (2 mg CPA/35 μg Ethinylestradiol – z.B. in Diane® mite) bei über 80% der Patientinnen zu einer Besserung des Effluviums. Auch Spironolacton in Kombination mit EE ist als orale Kontrazeption bei Frauen im gebärfähigen Alter sinnvoll (Yasmin®). Außerdem können Chlormadinonacetat-haltige Präparate zum Einsatz kommen (Belara®). Im Klimakterium oder in der Postmenopause können ebenfalls CPA (Climen®) oder Spironolacton (Angeliq®) verordnet werden.
Effluvien bei Schilddrüsenfunktionsstörungen
Haarfollikeln exprimieren Thyroxinrezeptor-β-1, darüber hinaus zeigen experimentelle Hinweise den Einfluss einer Inkubation mit Schilddrüsenhormon auf die Haarwuchsgeschwindigkeit und die Überlebensdauer von Haarfollikelzellen.
Hypothyreose: Das diffuse Telogeneffluvium ist oft ein initiales Zeichen einer Hypothyreose. Am Kopf tritt das Effluvium bei 25-50% bei Myxödem auf, darüber hinaus kommt es häufig zum Verlust von Körperhaaren sowie von Pubes und Achselhaaren; in 25% findet sich ein positives Hertoghe-Zeichen.
Hyperthyreose: Die Zusammenhänge sind weniger gut belegt, in 60% besteht aber eine deutliche Reduktion der Axillarbehaarung. Auch Thyreostatika können zu Haarausfall führen.
Diagnostik: Die Anamnese nimmt einen wichtigen Stellenwert ein (Körpergewicht, Kälteintoleranz, Obstipation oder Diarrhoe, Nervosität, Depression oder Affektlabilität). Labor: basales TSH, freies T4, Gesamt-T3
Therapie: Eine Substitution der Hypothyreose mit L-Thyroxin führt innerhalb weniger Monate zum Sistieren des Effluviums, während eine bereits länger bestehende Alopezie weiter bestehen kann. Vor allem die Kombination mit einer androgenetischen Alopezie hat eine ungünstige Prognose.
Literatur bei der Verfasserin