Die individualisierte Lipidsenker-Therapie
Die Dyslipidämie stellt einen der Hauptrisikofaktoren für kardiovaskuläre Erkrankungen dar. Eine Reihe großer Interventionsstudien konnte aufzeigen, dass eine effektive Therapie der Dyslipidämie in einer signifikanten Reduktion der kardiovaskulären Ereignisrate resultiert. LDL-Cholesterin (LDL-C) gilt dabei als vorrangiges Therapietarget.
Die Therapiewahl erfolgt in der klinischen Praxis unter Bezugnahme auf den Lipoproteinphänotyp der Patienten und die in den aktuellen Leitlinienempfehlungen dargelegten Zielwerte entsprechend Risikoprofil (Tab. 1).1, 2 Ein sehr hohes Risiko besteht dementsprechend bei Patienten nach einem dokumentierten kardiovaskulären Ereignis (Myokardinfarkt, Bypass und andere Revaskularisationsverfahren, Schlaganfall, PAVK, signifikante Plaques), bei Diabetes mit weiteren Risikofaktoren (Rauchen, Hypertonie, Dyslipidämie, Endorganschäden), bei einer schweren chronischen Nierenerkrankung (GFR < 30 ml/min/1,73 m2) oder einem Risikoscore (europäischer SCORE zur Einschätzung des Risikos für einen kardiovaskulären Todesfall in den folgenden 10 Jahren) ≥10 % . Ein hohes kardiovaskuläres Risiko besteht bei deutlich erhöhten einzelnen Risikofaktoren (wie familiäre Hypercholesterinämie), chronischer Niereninsuffizienz (GFR 30–69 ml/min/1,73 m2) oder einem Risikoscore von ≥ 5 % bis < 10 %.
Der Lipoproteinphänotyp in Folge einer Insulinresistenz führt zur Entwicklung kleiner dichter atherogener LDL-Partikel, einer Hypertriglyzeridämie und einer Reduktion von HDL-Cholesterin. Non-HDL-Cholesterin als Bezugswert für alle triglyzeridhältigen Lipoproteine wird deshalb als weiteres Therapieziel in Leitlinienempfehlungen für Patienten mit Typ-2-Diabetes berücksichtigt.2
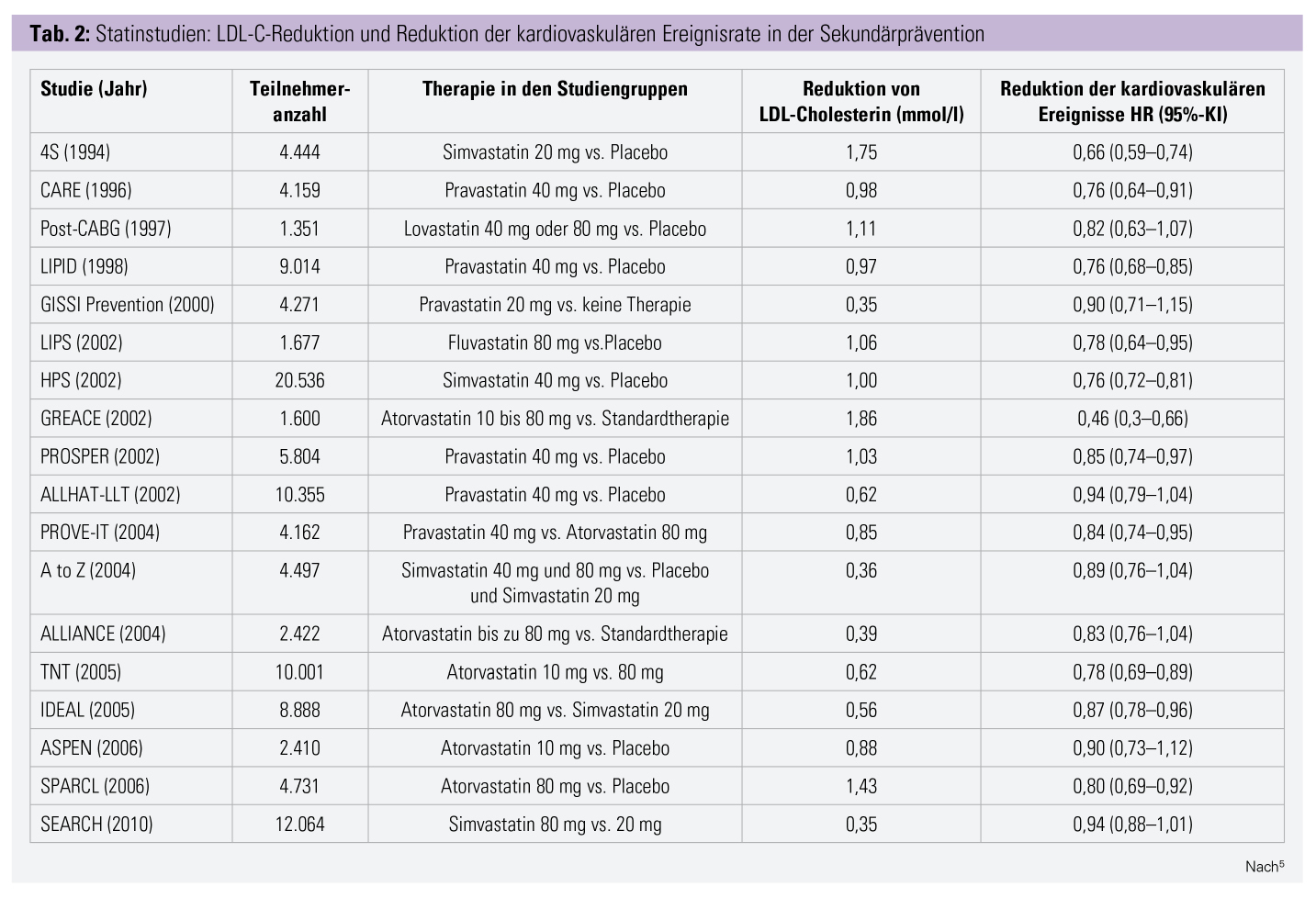
Aus Meta-Analysen der großen Statininterventionsstudien geht hervor, dass eine LDL-C-Reduktion um 40 mg/dl eine 21%ige Senkung des kardiovaskulären Risikos bewirkt (Tab. 2).3–5 Die neue Substanzklasse der PCSK9-Inhibitoren (Evolocumab, Alirocumab) ermöglicht – neben einer besonders ausgeprägten Reduktion von LDL-C – auch eine Reduktion von Lipoprotein (Lp) (a).6, 7
Medikamentöse Therapieformen
Statine inhibieren Schlüsselenzyme der zellulären Cholesterinsynthese und bewirken über eine verstärkte zelluläre LDL-Rezeptorexpression eine Verminderung der LDL-C-Plasmakonzentration. In Abhängigkeit von der Wirkintensität des Statins und der Dosierung kann eine LDL-C-Reduktion um bis zu 60 % erreicht werden. Die Triglyzeridwerte nehmen unter Statinen um 10–20 % ab, HDL-Cholesterin steigt um rund 5–10 % an. Große klinische Studien zeigen auf, dass durch die Statintherapie eine signifikante Reduktion der kardiovaskulären Ereignisrate, der kardiovaskulären Mortalität und der Gesamtmortalität erfolgt (Tab. 2).3–5
Eine weitere Intensivierung des lipidsenkenden Effektes der Statine kann durch Kombination mit Ezetimib, das die intestinale Cholesterinabsorption verringert, erzielt werden. Die zusätzliche LDL-C-Reduktion beträgt rund 15–20 %. In der IMPROVE-IT-Studie wurde unter der Kombination von Simvastatin mit Ezetimib bei Patienten nach einem akuten Koronarereignis eine weitere LDL-C-Senkung um 17 mg/dl und eine Reduktion des kardiovaskulären Risikos um 7,6 % gegenüber einer Simvastatinmonotherapie beschrieben.8
Die PCSK9-Inhibitoren Evolocumab und Alirocumab stehen seit rund 4 Jahren für den klinischen Einsatz zur Verfügung. Diese Substanzklasse verringert die lysosomale Degradation des LDL-Rezeptors und bewirkt eine hocheffektive rund 60%ige Senkung von LDL-C.9 Bei einem Großteil der klinischen Studien erfolgte die PCSK9-Inhibitortherapie zusätzlich zu einer laufenden und optimierten Statintherapie.6, 7
An der FOURIER-Studie nahmen über 25.000 Patienten mit Zustand nach einem kardiovaskulären Ereignis teil.6 Davon wiesen 36,7 % einen Diabetes mellitus auf, 13,5 % eine PAVK.6 Die Therapie mit Evolocumab resultierte in einer signifikanten LDL-C-Senkung, die LDL-C-Mittelwerte betrugen 30 mg/dl. Während des Beobachtungszeitraumes von 2,2 Jahren konnte eine Reduktion des primären Endpunkts (5-MACE) um 15 % erreicht werden.
An der ODYSSEY-Studie nahmen rund 18.000 Hochrisikopatienten nach einem akuten Koronarsyndrom teil.7 Unter Alirocumab wurden LDL-C-Mittelwerte von 42 mg/dl sowie eine Reduktion des kombinierten kardiovaskulären Endpunkts (4-MACE) um 15 % erreicht. Für diese Hochrisikopopulation nach einem akuten Koronarsyndrom konnte auch eine Reduktion der Gesamtmortalität um 15 % beobachtet werden.
Die Verordnung von PCSK9-Inhibitoren erfolgt derzeit für ausgewählte Hochrisikopatienten an definierten Stoffwechselzentren.
Komorbiditäten
Das Vorliegen eines Diabetes mellitus ist mit einem deutlich erhöhten kardiovaskulären Risiko assoziiert. Die Effektivität von Statinen und PCSK9-Inhibitoren hinsichtlich einer Reduktion des kardiovaskulären Risikos wurde in Subanalysen der großen Interventionsstudien auch für Diabetiker belegt. Gegenüber einer Vergleichsmedikationen mit Fenofibrat fand sich in der ODYSSEY DM-DYSLIPIDEMIA-Studie unter Alirocumab auch eine um rund 30 % stärkere Reduktion von Non-HDL-Cholesterin.10
Das hohe kardiovaskuläre Risiko ist insbesondere bei PAVK-Patienten zu beachten. Statine zeigen günstige Effekte hinsichtlich der PAVK selbst, wie auch in Bezug auf die kardiovaskuläre Komplikationsrate. Zur PAVK liegen aus der FOURIER-Studie Daten über die Vorteile einer Therapie mit Evolocumab vor.6 Dies betrifft sowohl den Verlauf und die Komplikationsrate der PAVK als auch das kardiovaskuläre Risiko.
In klinischen Studien wurde der günstige Effekt einer LDL-Cholesterinsenkung durch Statine und PCSK9-Inhibitoren auf das Risiko für einen ischämischen (Re-)Insult sowie kardiovaskuläre Komplikationen auch bei Schlaganfallpatienten aufgezeigt.4
Lipidzielwerte
Die Ergebnisse der Statininterventionsstudien, einschließlich der IMPROVE-IT-Studie, zeigen auf, dass bei einer strikteren Senkung des LDL-C eine ausgeprägtere Reduktion des kardiovaskulären Risikos erreicht wird („the lower, the better“). Der Vorteil, aber auch die Sicherheit einer intensiven LDL-C-Senkung, wird durch die Ergebnisse der PCSK9-Inhibitor-Studien bestätigt. In aktuellen Leitlinienempfehlungen, wie jenen der AACE für Patienten mit Diabetes mellitus und einer manifesten kardiovaskulären Erkrankung, erfolgte bereits eine Anpassung des LDL-C-Zielwert auf < 55 mg/dl anstelle von bislang < 70 mg/dl.6
Resümee
Für die klinische Praxis stehen mit Statinen (in Kombination mit Ezetimib) und PCSK9-Inhibitoren hocheffektive Medikamente zur Therapie der Dyslipidämie zur Verfügung. Klinische Studien belegen die Vorteile einer intensiven LDL-C-Senkung hinsichtlich der Reduktion des kardiovaskulären Risikos.