Highlights in der Hepatologie
Auf der diesjährigen „United European Gastroenterology Week“ (UEGW) wurden zum einen neue Forschungsergebnisse präsentiert und zum anderen exzellente Übersichts- und „State-of-the-Art“-Vorträge gehalten. Auf der amerikanische Lebertagung (Meeting der „American Association for the Study of Liver Diseases“; [AASLD]) in San Francisco wurden interessante internationale epidemiologische Trends von Lebererkrankungen und faszinierende Resultate von Phase-II-Studien präsentiert. Folgend möchte ich einen Überblick über praxisrelevante Beiträge von der UEGW und der AASLD geben und dabei auf folgende Themengebiete eingehen:
- Hepatitis B und Hepatitis C
- cholestatische Lebererkrankungen
- Lebererkrankungen in der Schwangerschaft
- Fettlebererkrankungen
Unter 3.705 zur Auswahl stehenden wissenschaftlichen Beiträgen wurden letztendlich 2.392 Originalbeiträge (64,6 % Annahmequote) auf der UEGW präsentiert.
Unter den Teilnehmern aus insgesamt 111 Ländern waren auch 437 Mitglieder der ESGENA (European Society of Gastroenterology and Endoscopy Nurses and Associates) und erfreulicherweise kamen 16,9 % aus Asien, 5,6 % aus Südamerika und 5,3 % aus Nordamerika. Großbritannien, Italien und Deutschland stellten die meisten Teilnehmer auf der UEGW.
Hepatitis B
Zur Hepatitis-B-Therapie wurden Daten zu neuen Substanzklassen vorgestellt, die in Zukunft neben oder zusammen mit den aktuell verwendeten Nukleosid-Analoga Tenofovir und Entecavir zum Einsatz kommen könnten:
„Core-Inhibitoren“: ABI-H0731 zeigte in einer 28-tägigen Phase-Ib-Studie an 12 nichtzirrhotischen Hepatitis-B-Patienten dosisabhängige antivirale Effekte mit bis zu einem 4-log-Stufen-Abfall in der Viruslast (HBV-DNA) (Man-Fung Yuen, AASLD 2018 abstr 73).
„Capsid-Assembly-Modulatoren“ (CAMs): JNJ-6379 erreichte bei nichtzirrhotischen Hepatitis-B-Patienten eine Viruslastabfall (HBV-DNA) von knapp 3-log-Stufen (Zoulim F, AASLD 2018, abstr 74).
„Nukleinsäuren-Polymere“ (NAPs): REP 2139 blockiert den Zusammenbau und die Freisetzung von Hepatitis-B-Viruspartikeln und induzierte damit effektive Immunantworten. Interessanterweise kam es zu einem Abfall der HBsAg-Spiegeln und damit verbunden oftmals zur Anti-HBs-Serokonversion, die allerdings mit Transaminasen-Flares assoziiert war. Eine Phase-II-Studie wird geplant (Bazinet et al., AASLD 2018, abstr 393).
„RIG-Modulatoren“: In einer randomisiert kontrollierten Studie über 12 Wochen erreichte Inarigivir bei HBeAg-negativen Patienten eine 3-log-Stufenreduktion und bei HBeAg-positiven Hepatitis-B-Patienten einen 1-log-Stufenabfall in der Viruslast (HBV-DNA) (Man-Fung Yuen, AASLD 2018, abstr 75).
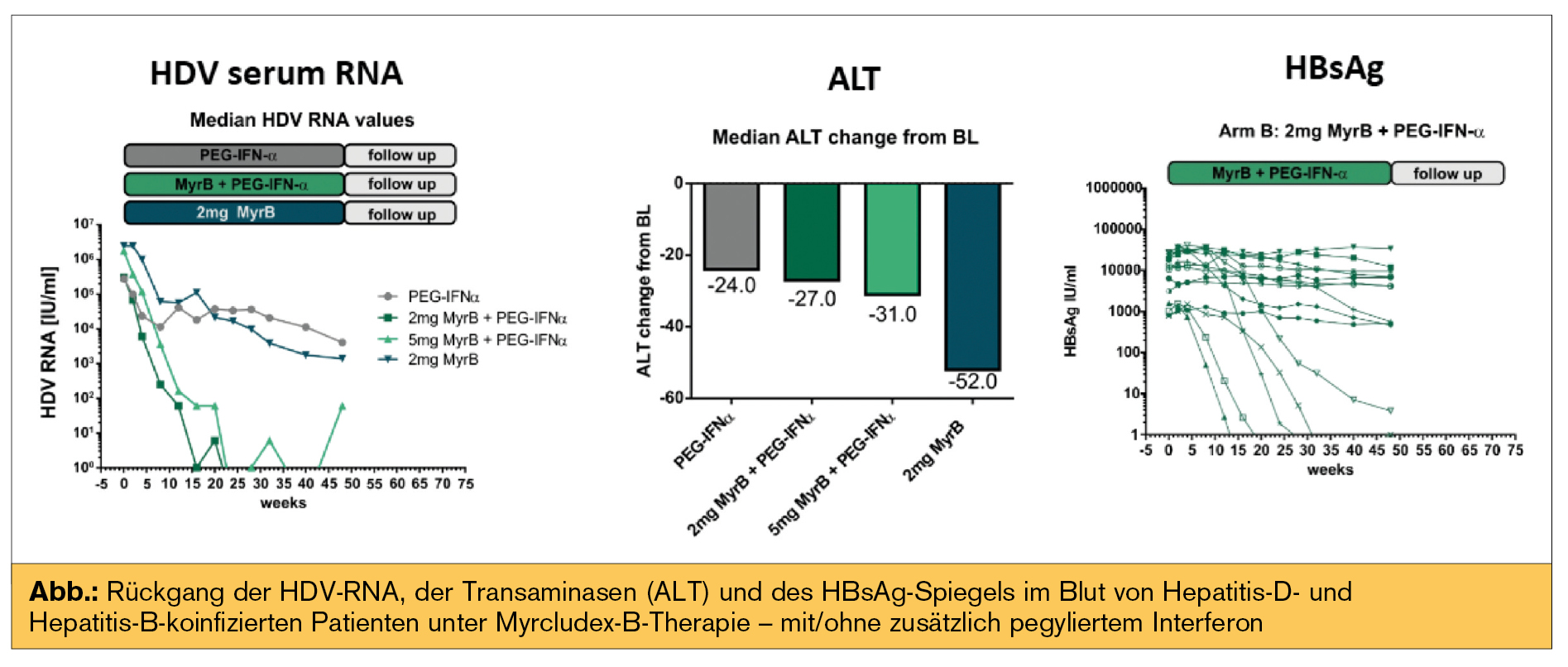
„Entry-Inhibitoren“: Myrcludex B (MyrB, NTCP-Rezeptor-Blocker, über ein Jahr täglich subkutan appliziert) zeigte bei 60 Hepatitis-D- und Hepatitis-B-koinfizierten Patienten in einer 4-armigen randomisierten Studie mit und ohne pegyliertem Interferon antivirale Effekte (Rückgang der HDV-RNA) und Abfall des HBsAg sowie einen Rückgang der Transaminasen (Wedemeyer H, AASLD 2018, abstr 16) (Abb.).
Hepatitis C
In der von Dr. Bianca Magro aus Palermo (Italien) präsentierten RESIST-HCV-Studie wurde gezeigt, dass „direkt antiviral wirkende Substanzen“ (DAAs) die Mortalität von Hepatitis-C-Patienten – egal, in welchem Krankheitsstadium sich die Patienten befinden – signifikant reduzieren. So war das Erreichen einer virologischen Heilung (Sustained virologic Response, SVR) mit einem reduzierten Risiko sowohl für leberbezogene als auch für nichtleberbezogene Todesursachen erhöht. Die Studie schloss 5.166 Teilnehmer ein, die zwischen März 2015 und Dezember 2016 mit DAAs therapiert wurden. 4.668 dieser Teilnehmer wurden dann in der RESIST-HCV-Studie für im Mittel 72 Wochen nachverfolgt, und der Großteil dieser Patienten (4.236, 90,7 %) erreichte eine Heilung/SVR. Das Nichterreichen eines SVR (18,5-fache Risikosteigerung) und ein niedriges Serum-Albumin < 35 g/l (6,1-fache Risikosteigerung) wurden als unabhängige Risikofaktoren für leberbezogene Mortalität identifiziert. Interessanterweise wird auch das Risiko für kardiovaskuläre Ereignisse und für das Entstehen eines Diabetes durch eine SVR deutlich reduziert.
Eine weitere auf der AASLD vorgestellte Studie (Dr. Sarah Kattakuzhy und Dr. Elena Rosenthal, AASLD 2018, abstr 18) untersuche die Effektivität von DAAs (hier Sofosbuvir/Velpatasvir für 12 Wochen) in der Problempopulation der Hepatitis-C-Patienten mit aktivem und „rezentem“ (also innerhalb der letzten 3 Monate) intravenösem Drogenkonsum. Die Therapieadhärenz (1-mal 1 Tablette pro Tag) wurde durch die eingenommenen bzw. noch übrigen Tabletten zum geplanten Therapieende überprüft. Während nur 14/43 Patienten (32,6 %) der Patienten die Therapie-Vorschreibung genau einhielten, hatten die 29/43 (67,4 %) Patienten, die einzelne oder mehrere Dosen nicht einnahmen und erst später mit der Therapie fertig wurden, gleich hohe SVR-Raten. Insgesamt lag die SVR-Rate im Problemkollektiv der Hepatitis-C-Patienten mit aktivem oder rezentem Drogenabusus bei 90 %.
In der EXPEDITION-8-Studie wurde die SVR von Hepatitis-C-Patienten mit kompensierter Leberzirrhose (Child-Pugh Score A5/A6) auf eine 8-wöchige Therapie mit Glecaprevir/Pibrentasvir (G/P) untersucht. Insgesamt wurden 280 zirrhotische (aber kompensierte) Patienten mit Non-Genotyp3-Infektion für 8 Wochen mit G/P behandelt, und obwohl 48 Patienten (17 %) eine Thrombopenie < 100 G/l als Zeichen einer portalen Hypertension aufwiesen, lag die SVR-Rate bei 98 % (274/280), bei Patienten, welche die Therapie laut Protokoll durchgeführt haben, sogar bei 100 % (273/273). Eine Extension der EXPEDITION-8-Studie auf kompensierte, zirrhotische Patienten mit HCV-Genotyp3-Infektion rekrutiert gerade.
Primäre biliäre Cholangitis (PBC)
Eine neue Therapieoption stellt Seladelpar, ein Agonist des nukleären PPAR-Delta-Rezeptors dar: In einer Open-Label-Phase-II-Studie erhielten 34 Patienten mit Ursodeoxycholsäure-(UDCA-)Non-Response oder Intoleranz den PPAR-Delta-Agonisten Seladelpar für 52 Wochen. 64,7 % (22/34) der Patienten zeigten ein Ansprechen (definiert durch ein Absinken der alkalischen Phosphatase [AP] auf das < 1,67-Fache des oberen Normwerts und zeitgleiche Normalisierung des Bilirubins). Die Einnahme von Seladelpar über 52 Wochen war generell sicher und verursachte keinen Pruritus. Zusätzlich kam es zu einem Absinken der ALT um 31–33 % vom Ausgangswert (Bowlus C et al., AASLD 2018, abstr LB3).
Die prognostische Wertigkeit des Serum-Bilirubins wurde in einer großen PBC-Kohorte von 4.238 Patienten gezeigt. Interessanterweise waren bei PBC-Patienten bereits Bilirubin-Werte im hoch normalen oder auch im mittleren Normbereich im Vergleich zu niedrig normalen Werten mit einer erhöhten Mortalität verbunden (Gordon SC et al., AASLD, abstr 47).
Primär sklerosierende Cholangitis (PSC)
Mit dem nichtsteroidalen FXR-Rezeptoragonisten GS-9674 wurde eine interessante Therapieoption für PSC-Patienten in einer doppelblinden, placebokontrollierten Phase-II-Studie an 52 nichtzirrhotischen Patienten mit Large-duct-PSC untersucht. 20 Patienten erhielten den FXR-Agonisten GS-9674 in einer 100-mg-Dosierung und 19 Patienten in einer 30-mg-Dosierung für 12 Wochen einmal täglich. Es kam zu einem dosisabhängigen Abfall der AP um –6,1 % (30 mg/Tag) und –20,5 % (100 mg/Tag). Diese Effekte wurden auch bei gleichzeitiger UDCA-Einnahme beobachtet. Wichtigerweise kam es unter dem nichtsteroidalen FXR-Agonisten GS-9674 sogar zu einer Besserung der Juckreizsymptomatik. Weiters erfolgte eine Reduktion der ALT- und GGT-Werte sowie der TIMP-1-Spiegel als indirektes Zeichen einer Fibrosereduktion (Trauner M et al., AASLD 2018, Abstract 43).
Die Relevanz der MR-Diagnostik für die Prognose-Abschätzung der PSC wurde in zwei unabhängigen PSC-Kohorten unterstrichen: Zwei simple MR-Scores – basierend auf semiquantitativer Beurteilung von Gallengangsdilatationen, Dysmorphie, Zeichen der portalen Hypertension sowie der parenchymalen Kontrastmittelanflutungsinhomogenitäten – konnten ein komplikationsfreies Überleben bei PSC vorhersagen (Cazzagon N et al., AASLD 2018, abstr 44).
Lebererkrankungen in der Schwangerschaft
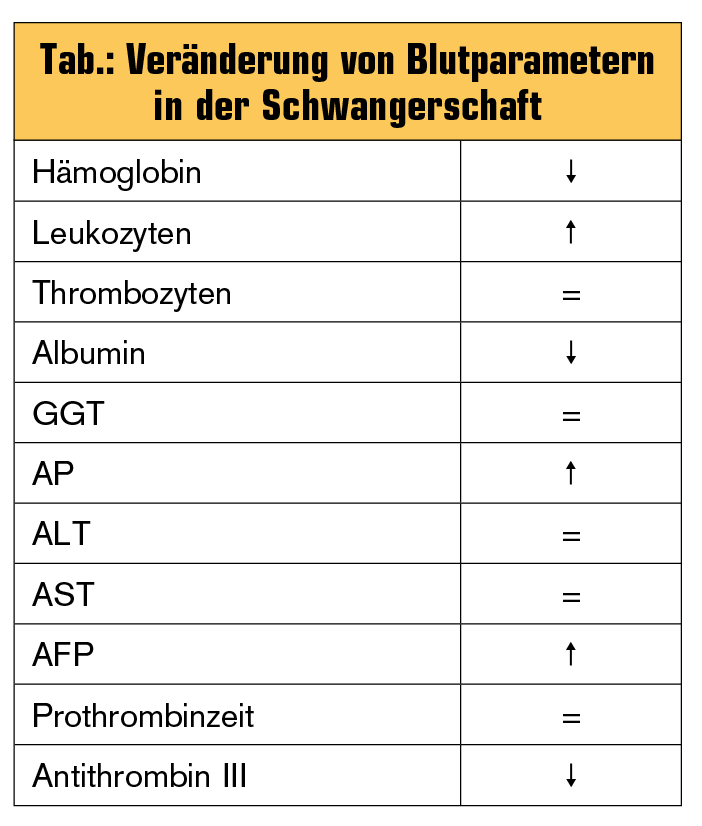
Eine sehr gut besuchte Session auf der UEGW beschäftige sich mit dem komplexen Thema der Lebererkrankungen in der Schwangerschaft (SS). Durch Fallbeispiele wurden die Pathophysiologie, typische Klinik und Laborveränderungen veranschaulicht sowie Therapieempfehlungen für fünf häufige Krankheitsbilder mit Leberbeteiligung in der Schwangerschaft erläutert. Es sei vorangestellt, dass einige „physiologische“ Laborabweichungen von der Norm in der Schwangerschaft zu beobachten sind, die es im Rahmen von hepatologischen Konsilen zu beachten gilt (Tab.). Während einer isolierten AP-Erhöhung zumeist kein Krankheitswert zukommt, sind Erhöhungen von anderen Cholestase-Parametern oder von Gallensäuren in der Differenzialdiagnostik zu beachten:
Hyperemesis gravidarum: Prävalenz von 0,3 bis 2 % aller SS, tritt im ersten Trimester auf und endet typischerweise vor der 18. SSW. Morgendliche Übelkeit und unberechenbares Erbrechen bis zu Dehydration, Elektrolytentgleisungen, Ketose und Gewichtsverlust können vorkommen. Cave: die AST/ALT-Werte können bis auf das 20-Fache der Norm ansteigen! Als Risikofaktoren gelten hoher BMI, psychiatrische Komorbiditäten, Diabetes und Mehrlingsschwangerschaft. Die Therapieoptionen inkludieren ausreichende Flüssigkeitszufuhr (evtl. Infusionstherapie), Korrektur von Elektrolytstörungen und antiemetische Therapie (hier ist Metoclopramid und Domperidon erlaubt) sowie evtl. Vitamin-B1-Supplementation.
Intrahepatische SS-Cholestase (ICP): tritt bei 0,5–1,8 % aller SS auf, und ist mit AST/ALT-Erhöhungen verbunden, AP ist immer erhöht, Bilirubin-Werte liegen zumeist im Normbereich. Erhöhte Gallensäurespiegel und Pruritus sind die laborchemischen und klinischen Leitsymptome der intrahepatischen SS-Cholestase. Gallensäurespiegel > 40 µmol/l sind mit häufigeren Komplikationen für das Kind assoziiert, korrelieren aber nicht unbedingt mit den Symptomen der Mutter. Die Entbindung sollte ab der 36. SSW angestrebt werden. Ursodeoxycholsäure (UDCA) in einer Dosis von 15 mg/kg Körpergewicht pro Tag stellt die Erstlinientherapie der ICP dar.
(Prä-)Eklampsie: Bei der Eklampsie handelt es sich um eine Multisystem-Erkrankung, die recht häufig (5–10 % aller SS) ab der 20. SSW zu beobachten ist. Die Symptome reichen von arterieller Hypertonie (> 140/90 mmHg) und Proteinurie (> 300 mg/24 h) bis zu Krampfanfällen (eigentliche Eklampsie). Als Risikofaktoren gelten junges Alter < 16 Jahre und höheres Alter > 45 Jahre, Erst-SS, präexistente Hypertonie, Eklampsie bei früheren SS und eine positive Familienanamnese auf Eklampsie. Die Symptomatik der Eklampsie umfasst: Übelkeit, Erbrechen, Oberbauchschmerzen, Kopfschmerzen, Visus-Veränderungen, Ödeme, verringerte Nierenfunktion und ALT-Erhöhungen bis zum 10-Fachen des oberen Normwerts. Als Therapie sollte eine möglichst strikte Blutdruckeinstellung erfolgen.
HELLP-Syndrom: 10–20 % der Eklampsie-SS können bis zum HELLP voranschreiten. Pathophysiologisch handelt es sich um eine mikroangiopathische hämolytische Anämie, die bei 6/1.000 SS ausschließlich im 2. und 3. Trimester auftritt. Laut Tennessee-Kriterien definiert sich die Hämolyse über eine LDH > 600 IU/l, die „ELevated Transaminasen über ALT/AST > 70 IU/ml und die Low Platelets über Thrombozyten < 100 G/l. Bei 2/3 Kriterien besteht ein partielles HELLP, bei 3/3 Kriterien ein komplettes HELLP-Syndrom. Als weitere diagnostische Maßnahmen sollte ein vermindertes Haptoglobin als Hämolysezeichen sowie Schistozyten im peripheren Blutausstrich erkennbar sein, die Prothrombinzeit/die INR sind zumeist nicht deutlich verlängert. Differenzialdiagnostisch sollte die akute SS-Fettleber (siehe unten), die thrombotische thrombozytopene Purpura (TTP: ADAMTS-13-Bestimmung!) und das hämolytische Urämie-Syndrom (HUS: Blutkultur, Fragmentozyten) beachtet werden. Als Therapiemaßnahmen sollte umgehend eine Kreislaufstabilisierung angestrebt werden, Magnesiumsulfat kann verabreicht werden, und es sollte mit Dexamethason therapiert werden. Eine Geburt ab der 34. SSW ist anzustreben.
Akute SS-Fettleber: Die akute SS-Fettleber ist eine seltene (1 : 7.000–16.000 SS) aber sehr schwere Erkrankung, die mit einem 20%igen Mortalitätsrisiko der Mutter und des Kindes einhergeht. Sie tritt im 3. Trimester oder auch früh post partum auf und ist histologisch durch eine mikrovesikuläre Verfettung gekennzeichnet. Die akute SS-Fettleber ist mit einem Gendefekt im Sinn einer Defizienz der Long-Chain-3-Hydroxyacyl-Koenzym-A-Dehydrogenase (LCHAD, fetale Mutation: Glu47G1n oder G1528C), der zu einem Defekt in der mitochondrialen Beta-Oxidation führt, assoziiert. Die Swansea-Kriterien umfassen Erbrechen, Bauchschmerzen, Polydipsie, Enzephalopathie, Bilirubin-Erhöhung, Hypoglykämie, Urämie, Leukozytose > 11 G/l, Aszites, erhöhte Echogenität der Leber im US, AST/ALT-Erhöhungen > 42 IU/ml, Hyperammonämie, Kreatininanstieg, Koagulopathie (Prothrombinzeit > 14 s, APTT > 34 s) und mikrovesikuläre Steatose in der Leberbiopsie. Wenn 6 oder mehr Kriterien (in Abwesenheit von anderen Gründen für die Symptome) erfüllt sind, ist die Diagnose einer akuten SS-Fettleber getroffen. Als Therapie wird eine ehestmögliche Entbindung empfohlen. Nach Geburt sollte auf eine LCHAD-Mutation getestet werden.
Fettlebererkrankungen – nichtalkoholische Steatohepatitis (NASH)
In Zusammenschau der Beiträge zur NASH auf der UEGW und auf der AASLD wurde klar, dass einerseits die Definition/Diagnostik in Abwesenheit eines idealen Biomarkers und der geringen Akzeptanz für eine Leberbiopsie (die ihrerseits jedoch auch durch „Sampling Error“ und „Interobserver Variability“ fehleranfällig ist) zu sehr heterogenen Studienpopulation von NASH-Patienten führen. Andererseits ist die NASH eine sehr dynamische Erkrankung, und schon geringe Änderungen im Lebensstil (wie Kalorienreduktion), körperliche Aktivität und Gewichtsabnahme können zu beachtlichen Veränderungen in der NASH-Krankheitsaktivität führen. Diese Phänomene erklären auch die teilweise beträchtlichen Unterschiede in den Placebo-Gruppen der präsentierten NASH-Studien. Zusätzlich können die pathophysiologischen Therapieansätze bei NASH auf verschiedenste Aspekte der Krankheit abzielen. So gibt es primär metabolische Ansätze, die vor allem auf die hepatische Steatose und das Plasmalipidprofil bzw. die Insulinresistenz abzielen, weiters gibt es antiinflammatorische Therapieansätze, die auf die hepatische Nekroinflammation und Ballonierung der Hepatozyten abzielen, und es existieren direkt antifibrotische Substanzen, die vor allem die Kollagen- und andere Matrixbestandteile im Vernarbungsprozess reduzieren sollen. Daher kommen dem Studiendesign besonders im NASH-Setting besondere Bedeutung zu. Typische NASH-Studiendesigns der aktuellsten Studien verwenden MR-basierte Steatose-Messungen, kombiniert mit nichtinvasiven Serum-Biomarkern zur Baseline und zum Studienende (zumeist um die 12 Wochen). Eine klinisch relevante Steatosereduktion wird dabei entweder als Reduktion im Leberfettgehalt (gemessen als Proton Density Fat Fractrion, PDFF) um entweder –5 % absolut oder –30 % relativer Gehalt definiert. Nachdem die Reduktion der ALT-Werte mit histologischer Nekroinflammation assoziiert ist, wird in Phase-II-Studien ohne Leberbiopsien eine ALT-Abfall um &re;= 17 IU/ml als klinisch relevant gewertet. Wichtig erscheint auch die Wirksamkeit einer Substanz als relativen Benefit im Vergleich zur Placebo-Gruppe (nachdem hier sehr unterschiedliche Ansprechraten beobachtet wurden) zu betrachten. Hierzu wurde der Begriff „margin over placebo“ definiert, also ein „relativer Placebo-Benefit“. Nun aber zu den vorgestellten Studien zu neuen Therapieansätzen bei NASH:
FXR-Agonismus: Der nichtsteroidale FXR-Agonist GS9674 führte bei nichtzirrhotischen NASH-Patienten (Definition entweder über MR-PDFF &re;= 8 % + MRE &re;= 2,5 kPa oder histologisch NAS &re;= 4) in einer randomisierten Studie (56 Patienten mit 30 mg 1-mal täglich, 56 Patienten mit 100 mg 1-mal täglich, 26 Patienten Placebo) über 24 Wochen zu keiner relevanten FGF19-Induktion, zu einer moderaten Reduktion der Gallensäurespiegel und zu einer dosisabhängigen Reduktion der hepatischen Steatose (–1,8 % PDFF bei 30 mg, –22,7 % bei 100 mg). Eine klinisch relevante Steatosereduktion zur Woche 24 um &re;= 30 % PDFF wurde bei 14,0 % (30 mg) und bei 38,9 % (100 mg) erreicht. Bei ALT und AST war ein nichtsignifikanter Abfall unter GS9674-Therapie zu verzeichnen, während es zu einem signifikanten Abfall der GGT (–19 % bei 30 mg, –37 % bei 100 mg), aber zu einem signifikanten Anstieg in der AP (+5 % 30 mg, +18 % 100 mg) kam. Wichtigerweise kam es zu keinen signifikanten Änderungen im Lipidprofil (Cholesterol, LDL-C, HDL-C, Triglyzeride) (Patel K et al., AASLD 2018, abstr 736).
FXR-Agonismus: In der FLIGHT-FXR-Studie wurde der nichtsteroidale FXR-Agonist Tropifexor (LJN) 91 nichtzirrhotischen NASH-Patienten (Definition entweder über NAS &re;= 4 in der Histologie + ALT-Erhöhung 40 %) oder adipösen Diabetikern (BMI &re;= 27 kg/m2) mit „phänotypischer“ NASH (erhöhtes ALT, 60 %) über 12 Wochen verabreicht, 30 Patienten waren im Placebo-Arm. Dosisabhängig kam es zu einer Induktion von FGF19 und zu einer Reduktion der ALT-Werte. Knapp 3 % der mit Tropifexor behandelten Patienten erzielten eine klinisch relevante Fettreduktion in der Leber (absoluter MR-PDFF Abfall &re;= 5 %). Nebenwirkungen (insbesondere Pruritus) traten nicht gehäuft auf, es kam jedoch zu einem milden Anstieg von LDL und mildem Abfall von HDL unter Tropifexor (Sanyal A et al., AASLD 2018, abstr LB23).
Rekombinantes FGF19: Eine 12-Wochen-Therapie mit NGM282 reduzierte den histologischen NAS-Score bei biopsiegesicherten NASH-Patienten. In dieser Studie war der zusätzliche Einsatz von Rosuvastatin erlaubt. Die endogene Gallensäuresynthese wurde durch NGM282 unterdrückt (90 % Reduktion der C4-Spiegel und Serum-Gallensäuren). Der primäre Endpunkt einer 5%igen Reduktion im absoluten Leberfettgehalt (MR-PDFF) wurde von 92 % (1-mg-Dosis, n = 24) und von 100 % (3-mg-Dosis, n = 19) erreicht, die absolute ALT-Reduktion betrug –62 IU/ml und –53 IU/ml. Histologisch zeigte sich bei 75 % und bei 84 % eine Verbesserung im NAS-Score, und 25 % zeigten eine Reduktion der Fibrose. Wichtig ist zu erwähnen, dass sich dennoch 17 % der Patienten in der Fibrose verschlechterten (Harrison SA et al., AASLD 2018, abstr 104).
Thyroidrezeptor-Beta-Agonismus: Die MGL3196-Gabe über 36 Wochen bei biopsiegesicherter NASH führte bereits nach 12 Wochen, aber auch nach 36 Wochen zu einem deutlichen Abfall des Leberfettgehalts (–36,3 % W12 und –37,3 % zur W36), und somit erreichten 27,4 % aller Patienten eine histologische NASH-Remission (Biopsie ohne Ballonierung, ohne relevante Inflammation und ein Rückgang im NAS &re;= 2 Punkte) – versus nur 6,4 % im Placebo-Arm. Es kam auch zu einer signifikanten Reduktion bei den ALT-Werten (–40 %) und zu einer Reduktion der nichtinvasiven Fibrosemarker (ELF, CK18, ProC3) und der histologischen Fibrose (32 % mit Abfall um zumindest ein Fibrosestadium) (Harrison SA et al., AASLD 2018, abstr 14).
Thyroidrezeptor-Beta-Agonismus: VK2809 führe bei 32 Patienten mit Steatose (NAFLD) und Hypercholesterinämie (LDL > 110 mg/dl) über 12 Wochen zu einer signifikanten Reduktion der LDL-Cholesterol-Spiegel um –21,8 %, der Lp(a) um –30,4 % und Apolipoprotein B (ApoB) um –20,4 %. Der relative Abfall im Leberfettgehalt betrug mittels MR-PDFF –58,1 %. Interessant war hier der Ansatz, die Studienpopulation über Steatose und Hyperlipidämie zu identifizieren. Limitierend sind die fehlende Leberbiopsie, die relativ kurze Studiendauer und fehlende Daten zu hepatischer Inflammation und Fibrose.
Resümee
Rezente epidemiologische Daten lassen in der westlichen Welt einen deutlichen Trend Richtung Rückgang von Hepatitis-C-Infektionen, aber einer Zunahme von Fettlebererkrankungen erkennen. In der Grundlagenforschung identifizierte Therapieansätze bei der nichtalkoholischen Fettleberhepatitis (NASH) haben in klinischen Phase-II-Studien beachtliche Erfolge erzielt. Während eine Reduktion des Fettgehalts in der Leber, Rückgang der Transaminasen und auch Hemmung der Fibrose – zumeist anhand nichtinvasiver Surrogatparameter in der multimodalen MR-Bildgebung oder Serum-Markern – erzielt wurden, fehlt aktuell noch die Evidenz für einen Benefit dieser Substanzen in Bezug auf harte Endpunkte wie leberbezogene Komplikationen (Dekompensation) und Mortalität. Bei fortgeschrittenen Lebererkrankungen, wie der Leberzirrhose und dem Akut-auf-chronischem Leberversagen (ACLF), wurden in Studien zu Regeneration mittels Stammzellmobilisierung und Plasmaaustausch vielversprechende Ergebnisse präsentiert.