Update zum Lungenkarzinom – Neues zu Diagnostik und Therapie aus 2011
Dass Diagnostik und Therapie des Lungenkarzinoms weiterhin eine Herausforderung für die Pneumologie bleiben, ist leicht auf der Homepage der Statistik Austria zu erkennen. So bleibt die Inzidenz mit ca. 30/100.000 Einwohnern und Jahr zwar gleich, die absoluten Zahlen nehmen aber kontinuierlich zu. In der Geschlechtsverteilung zeigt sich eine Zunahme der Häufigkeit bei den Frauen.1 In der Lungenkrebsmortalität findet man einen Rückgang von 25,4 auf 23,9/100.000/Jahr.
Diagnostik
Frühdiagnostik: Im NEJM erschienen im August 2011 die Ergebnisse der National Lung Cancer Screening Trial2. In diese Studie wurden 53.454 Risikopersonen zwischen 2002 und 2004 eingeschlossen und bis 2009 nachbeobachtet. Die eingeschlossenen TeilnehmerInnen waren zwischen 55 und 74 Jahre alt und hatten eine Raucheranamnese von mindestens 30 Packyears. Die Randomisierung erfolgte 1:1 in Screening mit Low- Dose-CT oder konventionellem Thoraxröntgen. Die erste Untersuchung erfolgte bald nach der Randomisierung, weitere 2 Tests folgten im Jahresabstand. Erstmals konnte eine Reduktion der Lungenkrebsmortalität um 20 % in der Low-Dose-CT-Gruppe im Vergleich zur Thoraxröntgen-Gruppe nachgewiesen werden. Allerdings ergeben sich beim Screening mit CT auch 3-mal mehr positive Befunde (39 % vs. 16 %) im Vergleich zum Thoraxröntgen, die weiter abgeklärt werden müssen. Es müssen jedenfalls 320 Personen gescreent werden, um einen Krebstodesfall verhindern zu können.
Bronchoskopie:Die Etablierung der transbronchialen Nadelaspiration mittels 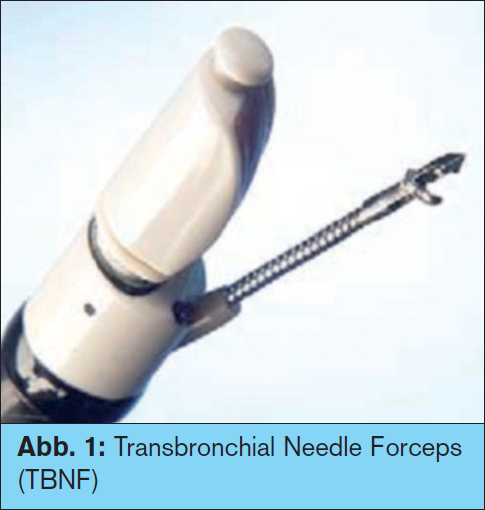 endobronchialem Ultraschall (EBUS-TBNA) in der bronchoskopischen Diagnostik des Lungenkrebses hat in den letzten Jahren zu einer deutlichen Qualitätsverbesserung des Stagings einerseits, aber auch der Diagnostik andererseits geführt. Die Verwendung einer Zange, die für die Penetration durch die Bronchialwand eine spitze Branche hat (> Abb. 1), scheint vielversprechend und wurde von F. Herth im ERJ beschrieben.3 Der Vorteil von histologischen Proben aus vergrößerten paratrachealen und aortopulmonalen Lymphknoten liegt auf der Hand. So sind immunhistochemische Färbungen und auch molekularpathologische Untersuchungen (z. B. EGFR-Mutationsstatus) aus solchen Proben leichter möglich, wie auch die Diagnostik von Lymphomen, Sarkoidose oder Tuberkulose.
endobronchialem Ultraschall (EBUS-TBNA) in der bronchoskopischen Diagnostik des Lungenkrebses hat in den letzten Jahren zu einer deutlichen Qualitätsverbesserung des Stagings einerseits, aber auch der Diagnostik andererseits geführt. Die Verwendung einer Zange, die für die Penetration durch die Bronchialwand eine spitze Branche hat (> Abb. 1), scheint vielversprechend und wurde von F. Herth im ERJ beschrieben.3 Der Vorteil von histologischen Proben aus vergrößerten paratrachealen und aortopulmonalen Lymphknoten liegt auf der Hand. So sind immunhistochemische Färbungen und auch molekularpathologische Untersuchungen (z. B. EGFR-Mutationsstatus) aus solchen Proben leichter möglich, wie auch die Diagnostik von Lymphomen, Sarkoidose oder Tuberkulose.
Therapie
Metastasiertes nicht-kleinzelliges Lungenkarzinom, NSCLC: Mehrere Phase-III-Studien (IPASS [Gefitinib], CALBG-30406 [Erlotinib]) haben bewiesen, dass bei aktivierender EGFR-Mutation ein EGFR-Tyrosinkinaseinhibitoren in der First-Line-Therapie des metas – tasierten NSCLC als Standard anzusehen ist. So wurde erstmals auch bei Kaukasiern in der EURTAC4-Studie dieses Konzept für Erlotinib untermauert. Im Mai 2011 ist dazu bereits ein Konsensusbericht in der „Wiener Klinischen Wochenschrift“ erschienen, der einen Histologie-basierten Algorithmus zur Bestimmung von Mutationen im EGFR-Gen empfiehlt5 (> Abb. 2). 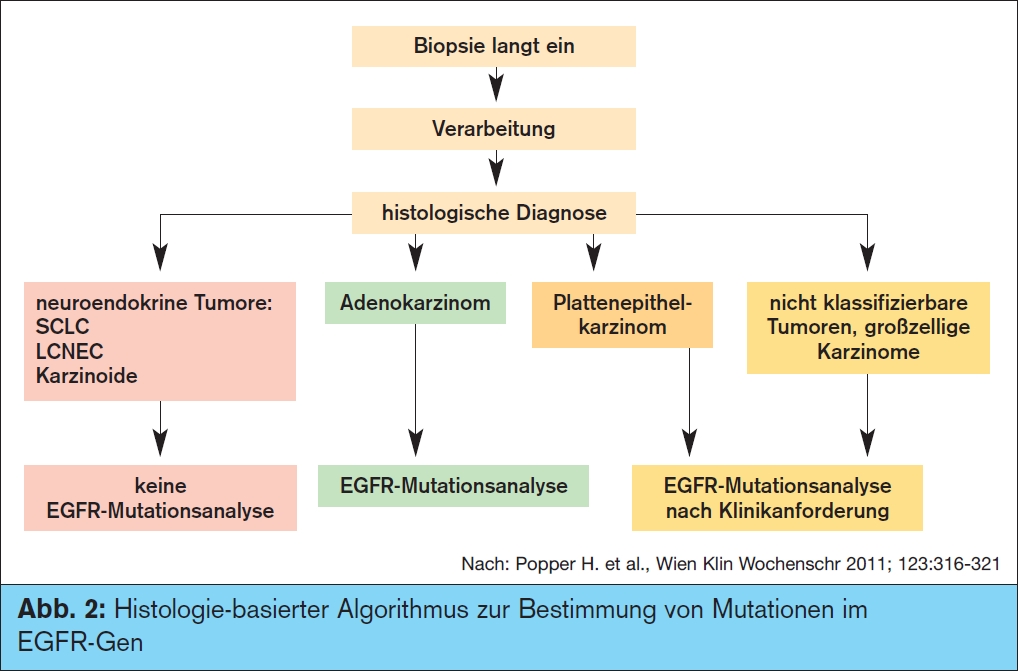 In unserem Patientengut sind bei den Adenokarzinomen 12–14 % Mutationen zu erwarten.
In unserem Patientengut sind bei den Adenokarzinomen 12–14 % Mutationen zu erwarten.
Der Einfluss von Crizotinib, einem ALK-Inhibitor (Anaplastic Lymphoma Kinase), auf das Überleben von Patienten mit ALK-positivem NSCLC wurde mit historischen Kontrollen verglichen.6 82 Patienten mit ALK-positivem FISH wurden mit Crizotinib behandelt. Bei diesen Patienten war die mediane Überlebenszeit nach 2,5 Jahren nicht erreicht, die 1-Jahres-Überlebensrate betrug 74 %. Aufgrund dieser Ergebnisse hat die FDA in einem abgekürzten Verfahren Crizotinib für die Therapie von NSCLC im Stadium IV mit ALK-positivem FISH zugelassen. Die EML4- ALK-Translokation kommt bei jüngeren Männern mit Adenokarzinom gehäuft vor. Insgesamt ist eine Häufigkeit von 4 % in allen NSCLCs zu erwarten.
Im Hinblick auf die Heterogenität der Adenokarzinome wurden vom amerikanischen Lung Cancer Mutation Consortium (LCMC) beim heurigen ASCO sogenannte „driver mutations“ vorgestellt. Es wurden bereits mehr als 1.000 Adenokarzinom-Proben untersucht und in 54 % der Fälle konnten Mutationen nachgewiesen werden. Die wichtigsten sind KRAS-, EGFR- und EML4-ALK-Mutationen. Bezüglich der VEGFR-Inhibitoren ist festzuhalten, dass bis dato nur Bevacizumab (ECOG 4599, AVAIL) in der First-Line-Therapie in Kombination mit Chemotherapie einen Überlebensvorteil belegen konnte.
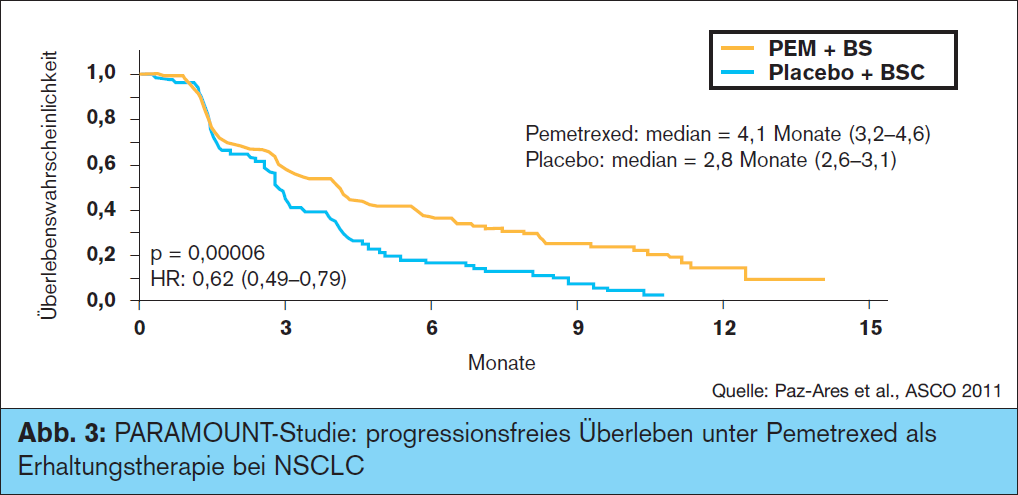
Das in letzter Zeit viel diskutierte Konzept der Erhaltungstherapie wird mit den Ergebnissen der PARAMOUNT-Studie komplettiert. Eine Pemetrexed-Continuation, nach Induktion mit Cisplatin/Pemetrexed, wurde gegen Placebo verglichen. Es zeigte sich ein signifikanter Vorteil hinsichtlich des medianen PFS für die Maintenance-Gruppe (3,9 Monate vs. 2,6 Monate) (> Abb. 3). Dies führte auch zur Zulassung von Pemetrexed als Erhaltungstherapie nach Chemotherapie mit Pemetrexed und Platin, obwohl die OSDaten noch nicht vollständig sind.
Neue Substanzklassen mit ersten Studien – ergebnissen sind unter anderem der Heat- Shock-Protein-90-Inhibitor Ganetespib (Hsp90) und der Toll-like-Rezeptor-Agonist (Mycobacterium w/CADI-05) als Immunotherapie. Bei kleinen Patientenzahlen lassen sich Wirkungen in Subgruppen erkennen, welche weiterer Forschung bedürfen.
Kleinzelliges Lungenkarzinom, SCLC: In der Zweitlinientherapie des SCLC ist Topotecan seit Jahren etabliert. In der Phase-III-Studie ACT-19 wurde Amrubicin, ein Drittgeneration- Anthrazyklin und Topoisomerase-2-Hemmer, gegen Topotecan in der Second-Line- Therapie des SCLC getestet. Die Ansprechraten sind bei Amrubicin besser, im OS sind die Ergebnisse nicht signifikant.
Adjuvante Therapien: TREAT10 ist eine randomisierte Machbarkeitsstudie zur Verbesserung der adjuvanten Chemotherapie des NSCLC (Cisplatin/Vinorelbin vs. Cisplatin/Pemetrexed). Die Studienziele – eine Reduktion der Toxizitäten, Erhöhung der Compliance und der Gesamtdosis – konnten erreicht werden. Überlebensdaten liegen noch nicht vor. Es wurden allerdings alle NSCLCs eingeschlossen mit beinahe der Hälfte plattenepithelialer Histologie.
Strahlentherapie: Seit März 2009 ist in München ein Protonen-Therapiezentrum in Betrieb. Im Unterschied zur Photonen-Therapie gelingt es mit diesem Therapieansatz hohe Zielvolumendosen unter maximaler Schonung des gesunden Gewebes zu erreichen. Aufgrund der physikalischen Eigenschaften der Protonen reduziert sich die Integraldosis im gesunden Gewebe auf 1/6 im Vergleich zu Photonen. Eine breite Anwendung ist derzeit aufgrund der limitierten Kapazitäten und der hohen Einzelfallkosten noch nicht möglich. In Wiener Neustadt ist ein ähnliches Therapiezentrum in Bau, das 2015 in Betrieb gehen soll.
FACT-BOX
- In Risikogruppen bringt Screening mit Low-Dose-CT einen Überlebensvorteil.
- Bei bekanntem positivem Mutationsstatus (EGFR, EML4-ALK) ist die zielgerichtete Therapie mit EGFR-TKIs bzw. Crizotinib im Stadium IV des NSCLC die beste Therapieoption.
- Die Erhaltungstherapie bleibt weiter aktuell, sowohl als „Continuation“- als auch als „Switch-Maintenance“, der routinemäßige Einsatz ist noch nicht etabliert.
- Die Rolle der Molekularbiologie wird immer bedeutender für die Patientenselektion, aber auch für die Prognose.
1 Statistik Austria, Österreichisches Krebsregister (Stand 13. 9. 2011)
2 Reduced Lung-Cancer Mortality with Low-Dose Computed Tomographic Screening; NEJM 2011; 365:5
3 Herth F. et al.: EBUS-guided lymph node biopsy (EBUS-TBNB) with a transbronchial needle forceps (TBNF) – a pilot study; ERJ Express 2011, June 23
4 Rosell R.: Erlotinib versus chemotherapy (CT) in advanced non-small cell lung cancer (NSCLC) patients (p) with epidermal growth factor receptor (EGFR) mutations: Interim results of the European Erlotinib Versus Chemotherapy (EURTAC) phase III randomized trial. ASCO 2011; #7503
5 Popper H. et al.: Histologie-basierter Algorithmus der molekularen Diagnostik des epidermalen Wachstumsfaktor- Rezeptorgens (Epidermal Growth Factor Receptor, EGFR) beim nicht-kleinzelligen Lungen – kar zinom (non-small cell lung cancer, NSCLC); Wien Klin Wochenschr 2011; 123:316-321
6 Shaw A. T.: Impact of crizotinib on survival in patients with advanced, ALK-positive NSCLC compared with historical controls. ASCO 2011; #7507
7 Identification of driver mutations in tumor specimens from 1,000 patients with lung adenocarcinoma: The NCI’s Lung Cancer Mutation Consortium (LCMC). ASCO 2011; Abstract CRA7506
8 Paz-Ares L.G.: Phase III study of maintenance peme – trexed (pem) plus best supportive care (BSC) versus placebo plus BSC immediately following induction treatment with pem plus cisplatin for advanced nonsquamous non-small cell lung cancer (NSCLC). ASCO 2011; Abstract CRA7511
9 Jotte R.: Randomized phase III trial of amrubicin versus topotecan (Topo) as second-line treatment for small cell lung cancer (SCLC). ASCO 2011; #7000
10 M. Kreuter: Randomized phase II trial on refinement of early-stage NSCLC adjuvant chemotherapy with cisplatin and pemetrexed (CPx) versus cisplatin and vinorelbine (CVb): TREAT. ASCO 2011#7002