Asthma bronchiale ist eine der häufigsten Atemwegserkrankungen. Laut Daten der österreichischen LEAD-(„Lung – hEart – sociAl – boDy“-)Studie (www.leadstudy.at) gibt es in Österreich rund 500.000 Betroffene, wovon rund 5 % unkontrolliert sind und das Asthma somit als schwer definiert wird. Schweres Asthma ist mit einem hohen Risiko für schwere Exazerbationen, akute Verschlechterung mit/ohne Hospitalisation und einer damit verbundenen erhöhten Mortalität sowie einer Beeinträchtigung der Lebensqualität und der Verrichtung von Alltagsaktivitäten verbunden, wodurch der Bedarf an (Früh-)Erkennung und personalisierter Therapie besteht.
Therapie des schweren Asthmas
Gemäß der Empfehlung der „Global Initiative for Asthma“ (GINA) basiert die Therapie des Asthmas auf einem Stufenschema, wobei die Gabe eines inhalativen Kortikosteroids (ICS) immer die Basis darstellt. Im Rahmen der Inhalationstherapie werden Kortikosteroide häufig mit einem schnell, aber lang wirksamen b2-Agonisten (LABA) kombiniert und können so sowohl die Basis- als auch die Bedarfsmedikation bilden (SMART = Single Maintenance and Reliever Therapy). Systemische Kortisontherapie soll – außer bei Notfällen – vermieden werden.
Das Risiko von Exazerbationen sowie die Mortalität sind unter alleiniger Therapie mit einem kurzwirksamen b2-Agonisten (SABA) gegenüber einer Therapie mit einem ICS erhöht. In einer Langzeitstudie zeigte sich außerdem eine schlechtere Entwicklung der Lungenfunktion sowie erhöhte Exazerbationsgefahr bei alleiniger Therapie mit SABA. Dementsprechend ist von einer Monotherapie mit einem inhalativen SABA generell abzuraten!
Als schweres Asthma gelten Verlaufsformen, die nur unter einer optimierten hochdosierten Kombination aus ICS, LABA und gegebenenfalls einem Anticholinergikum zu kontrollieren sind oder sogar hierunter unkontrolliert bleiben. Dies bedeutet, dass diese Patient:innen trotz maximaler, korrekt inhalierter Dauertherapie entsprechend den neuesten Leitlinien und trotz der Reduktion von Triggern (= Auslösern, wie z. B. Allergene) weiterhin von respiratorischen Symptomen (> 2/Woche), Bedarf an zusätzlicher Therapie (> 2/Woche Bedarfsmedikation) bzw. Aktivitätseinschränkungen berichten. Hierbei stellt die Gabe von Biologika eine sehr gute zusätzliche Option dar. Insbesondere soll auch der Einsatz von systemisch verabreichten Kortikosteroiden reduziert und im besten Fall völlig verhindert werden.
Phänotypisierung des schweren Asthmas
Zunächst muss dabei eine umfangreiche Phänotypisierung erfolgen. Von der pathophysiologischen Seite her lassen sich 4 verschiedene Phänotypen skizzieren:
Beim eosinophilen Asthma sind eosinophile Granulozyten eine treibende Kraft der Krankheitsaktivität. Hier lassen sich vermehrt Eosinophile im Blut (≥ 300/mcl) und im Sputum nachweisen. Zusätzlich ist der Anteil an exhaliertem Stickstoffmonoxid (FeNO) erhöht. Diese Biomarker sind Ausdruck der sogenannten Typ-2-Inflammation, also einer durch einen spezifischen Schenkel des Immunsystems vermittelten chronischen Entzündung. Diese Form ist vor allem durch assoziierte Typ-2-Erkrankungen, die begleitend adäquat diagnostiziert und therapiert werden müssen, gekennzeichnet. Dazu zählen u. a. die eosinophile Ösophagitis/GERD, chronische Rhinosinusitis mit Nasenpolypen (CRSwNP) und atopische Dermatitis.
Ebenfalls in die Kategorie des Typ-2-vermittelten Asthmas fällt das allergische Asthma. Hierbei steht die Sensitivierung gegenüber einem oder auch mehreren Allergenen im Vordergrund. Es kommt zu einer Ausschüttung spezifischer IgE, die zur Aufrechterhaltung der chronischen Entzündung beitragen. Dementsprechend ist die allergologische Austestung und der Nachweis spezifischer Antikörper zentral in der Typisierung dieser Asthmaform. Der nachgewiesene Erfolg der Desensibilisierung zur Prophylaxe einer Verschlechterung ist hier zu betonen.
Neben diesen – als Typ-2-high-Varianten bezeichneten – Asthmatypen gibt es noch das neutrophile Asthma, wobei primär neutrophile Granulozyten für die Inflammation verantwortlich sind und nachgewiesen werden können. Diese Variante ist therapeutisch insofern herausfordernd, als sie oftmals schlechter auf Kortikosteroide anspricht und mit anderen Formen (begleitend COPD/Emphysem, Adipositas) einhergeht. Schließlich gelingt es bei maximal 5 % der Patient:innen mit schwerem Asthma nicht, sie einem spezifischen Phänotyp zuzuordnen.
Auswahl des Biologikums
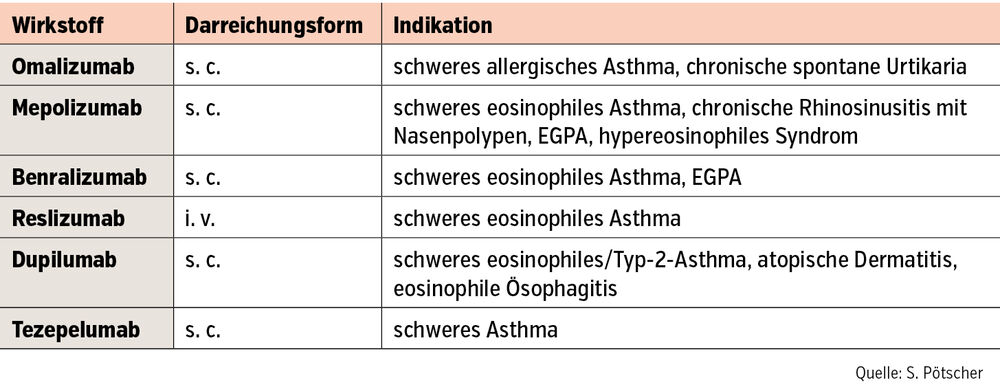
Die Wahl des Biologikums hängt nun von dem zugrunde liegenden Phänotyp ab. In Österreich sind bisher 6 Antikörper (Tab.) zugelassen:
- Der Anti-IgE-Antikörper Omalizumab bindet IgE und reduziert somit die Aktivität der spezifischen IgE beim schweren allergischen Asthma und kommt auch nur bei diesem Phänotyp zum Einsatz.
- Die Anti-Interleukin-5-Antikörper bzw. Anti-Interleukin-5-Rezeptor-Antikörper Mepolizumab, Benralizumab und Reslizumab hemmen die Aktivität von IL-5, das sowohl auf Wachstum als auch Differenzierung von eosinophilen Granulozyten wirkt. Somit werden diese Präparate primär beim schweren eosinophilen Asthma angewendet. Mepolizumab ist insbesondere auch bei konkomitant auftretenden Nasenpolypen zugelassen.
- Der Anti-IL-4-Rezeptor-Antikörper Dupilumab hemmt die Aktivität von IL-4 und IL-13, die Teil der Signalkaskade der Typ-2-Inflammation sind, und kann somit bei jedem schweren eosinophilen Asthma eingesetzt werden.
- Schließlich gibt es mit dem Anti-TSLP-Antikörper Tezepelumab einen Wirkstoff, der das vom Epithel sezernierte Alarmin „thymic stromal lymphopoietin“ (TSLP) hemmt und somit einen Ansatzpunkt hat, der weit stromaufwärts entlang der Signalkaskade liegt. Tezepelumab kann bei jedem schweren eosinophilen Asthma angewendet werden.
Die Auswahl des Biologikums sollte in Zusammenschau aller verfügbaren Befunde erfolgen. Zumindest die Erstgabe sollte immer unter fachärztlicher Aufsicht erfolgen, in weiterer Folge können die Patient:innen dann auf eine selbstständige Applikation geschult werden. Der Therapieerfolg sollte nach 4–6 Monaten abschließend beurteilt werden, wobei sich oftmals schon früher eine deutliche und vor allem spürbare Verbesserung der Symptomatik zeigt. Dank dieser Therapien kann ein weit größeres Therapieziel definiert werden, die Remission. Dazu gehört der nachweisbare Erfolg, typischerweise definiert als die Abwesenheit von Asthma-Symptomen über einen Zeitraum von mindestens 12 Monaten (= klinische Remission).
Impfprävention
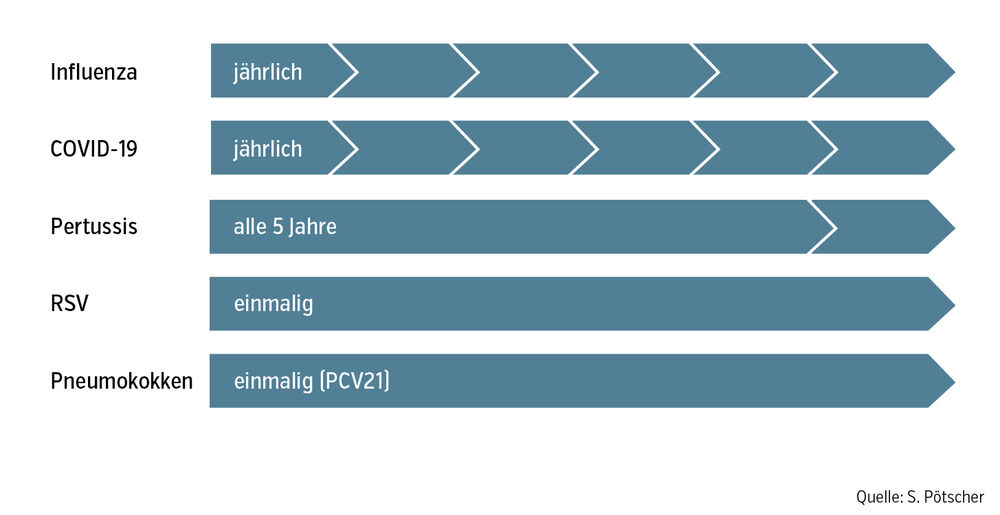
Zuletzt gilt es zu betonen, dass unabhängig vom gewählten Therapieschema die Prävention von Exazerbationen zentral ist. Insbesondere die Impfprävention ist hierbei von großer Wichtigkeit. Patient:innen mit Asthma bronchiale gehören a priori zu einer vulnerablen Gruppe hinsichtlich respiratorischer Infektionserkrankungen, und Impfungen gegen etwa Influenza, Sars-CoV-2, Pneumokokken, RSV und Pertussis sollten durchgeführt bzw. je nach Impfung (Abb.) regelmäßig aufgefrischt werden.