Blinde Flecken beseitigen
Angeblich stehen wir auf der Schwelle in ein neues medizinisches Zeitalter; dem Zeitalter der personalisierten Medizin. Therapien sollen in Zukunft auf einzelne Patienten maßgeschneidert und damit verbessert werden. Doch wie weit stehen wir tatsächlich beim Einlösen dieses seit Jahren erbrachten Versprechens? Was können sich Ärztinnen und Ärzten und Patientinnen und Patienten in den nächsten Jahren erwarten? Die Antworten auf diese Fragen werden je nach medizinischem Fachbereich höchst unterschiedlich ausfallen. Es steht etwa außer Zweifel, dass künstliche Intelligenz enorme Fortschritte für die bildgebende Diagnostik erbrachte – und noch bringen wird. Wesentlich ernüchternder fällt die Bilanz jedoch für die vermutlich größte Herausforderung für unser Gesundheitssystem aus: die Versorgung einer alternden Bevölkerung mitsamt einem rasanten Anstieg von chronisch kranken und multimorbiden Patienten. In diesem Bereich verstehen wir noch nicht einmal die vermutlich einfachste „Personalisierung“ hinreichend, nämlich geschlechtsspezifische Unterschiede.
Das Big-Data-Prinzip
Bei der Entwicklung personalisierter Therapien nimmt der Einsatz großer Datenmengen (Big Data) aus unterschiedlichsten Bereichen eine zentrale Rolle ein: von genomischen über metabolomische und soziodemografische bis hin zu medizinischen Daten. Die „klassische“ medizinische Forschung arbeitet bekannterweise mit kontrollierten Vergleichen. Dabei wird etwa eine bestimmte Bevölkerungsgruppe in zwei Kohorten aufgeteilt: Eine Kohorte bekommt eine neue Therapie, die andere wird nach bisherigen Standards behandelt. So kann man bewerten, ob die neue Therapie einen Nutzen bringt.
In personalisierten Big-Data-Analysen geht man im Grunde ähnlich vor, stellt aber den Anspruch, jeden einzelnen Patienten in seiner Ganzheit datenmäßig erfassen zu können. Sind ausreichend Daten vorhanden, kann man im Prinzip für jeden noch so komplizierten Fall (Alter, Geschlecht, Vorerkrankungen, soziale Faktoren et cetera) eine hinreichend große Menge vergleichbarer Patienten finden und bewerten, welche Behandlungen Erfolg hatten und welche nicht. Jedem Patienten/jeder Patientin eine eigene kontrollierte Fallstudie, um zu sehen, was hilft − so das Prinzip.
Als wir in meiner Forschungsgruppe an der MedUni Wien vor circa 10 Jahren zum ersten Mal mit bevölkerungsweiten Gesundheitsdaten der Sozialversicherungen arbeiten konnten, war die Zuversicht daher enorm, mithilfe solcher Daten neue spannende Wege in der personalisierten Medizin gehen zu können. Jedoch mussten wir sehr schnell feststellen, dass wir bereits bei der einfachsten Personalisierung an die Grenzen des Bekannten stießen – nämlich im Verstehen der gesundheitlichen Unterschiede zwischen Mann und Frau. Diese Unzulänglichkeiten sind nicht neu. Es ist bekannt, dass das weibliche Geschlecht in Studien – von der tierexperimentellen Studie bis hin zu fortgeschrittenen klinischen Phasen – im Vergleich zum männlichen unterrepräsentiert ist. Das hat gravierende Folgen für die Frauengesundheit. Wenn etwa Medikamente aufgrund unerwünschter Nebenwirkungen wieder vom Markt genommen werden, treten diese Nebenwirkungen häufiger bei Frauen als bei Männern auf.
Österreichische Gesundheitsdaten
Big Data bietet hier die große Chance. Das Arbeiten mit bevölkerungsweiten Daten ermöglicht es, blinde Flecken zu beseitigen. Anstatt von einer kleinen und statistisch verzerrten Patientenpopulation auf mögliche Charakteristika der gesamten österreichischen Bevölkerung hochrechnen zu müssen, können aus elektronischen Gesundheitsdaten sämtliche Medikamente und Spitalsdiagnosen aller Österreicher direkt ausgewertet werden.
Was wir beim Abtauchen in diese Daten fanden, erstaunte uns als Nichtmediziner dann doch. Mehr als 10 % der ÖsterreicherInnen im Alter von 50 Jahren oder darüber sammelten innerhalb von zwei Jahren mehr als zehn unterschiedliche medizinische Diagnosen an; manche bis zu 30 oder 40. Diese Erkrankungen verteilten sich über das gesamte diagnostische Spektrum. Um solch komplexe Patientenbilder zu verstehen, bedarf es interdisziplinärer Ansätze – über medizinische Fachrichtungen und sozial- und naturwissenschaftliche Grenzen hinweg.
Geschlechterspezifische Krankheitsnetzwerke
Die Komplexität dieser bevölkerungsweiten Multimorbidität sprengt das menschliche Vorstellungsvermögen. Wenn wir etwa zwei der PatientInnen mit zehn Diagnosen betrachten, wird kaum ein Paar die exakt gleichen Erkrankungen haben, aber viele werden sich zumindest teilweise überlappen.
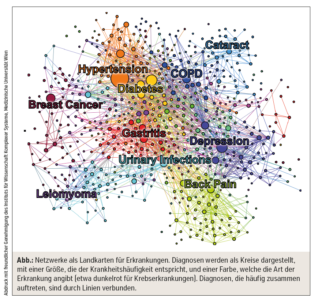
Das metabolische Syndrom kombiniert sich in dem einen Fall etwa mit Depressionen und Alkoholismus, im anderen Fall mit Nieren- und Herz-Kreislauf-Erkrankungen (HKE). Unsere wissenschaftliche Herausforderung bestand daher im Zeichnen einer Landkarte für diesen komplexen Krankheitsraum, um einzelne PatientInnen darin verorten zu können. Das kann mit Hilfe sogenannter „Krankheitsnetzwerke“ gemacht werden, darin werden Diagnosen als Kreise dargestellt (Abb.).
Zwei Kreise werden mit einer Linie verbunden, wenn die Krankheiten statistisch überzufällig häufig gemeinsam auftreten. Sobald man diese Landkarte kennt, werden personalisierte Vorhersagen möglich. Dazu wertet man aus, wo ein Patient/eine Patientin gerade „im Netzwerk ist“ − welche Diagnosen den Gesundheitszustand charakterisieren − und kann dann aus den Verbindungslinien ablesen, in welche Netzwerkregionen mit welchen Erkrankungen sich der Patient in den nächsten Jahren vermutlich bewegen wird.
Männer und Frauen zeigen höchst unterschiedliche Landkarten. Das zeigt sich beispielsweise deutlich beim Geschlechtervergleich der Krankheitsnetzwerke für Menschen mit HKE. Obwohl Männer im Allgemeinen ein höheres Risiko für HKE haben als Frauen, dreht sich dieses Bild oft komplett um, wenn man multimorbide PatientInnen betrachtet. Diabetes, Übergewicht, Nikotinabhängigkeit, Pneumonie, COPD oder Nierenerkrankungen sind allesamt bei Frauen stärker mit HKE assoziiert als bei Männern. Ärztinnen und Ärzten müssen sich dieser geschlechtsspezifischen Unterschiede bewusst sein, um ein effektiveres Screening für kardiovaskuläre Erkrankungen bei älteren Frauen zu erreichen.
So paradox es klingen mag, mit dem Einsatz großer Datenmengen, künstlicher Intelligenz und mittels maschinellen Lernens können wir die Medizin näher zum Patienten/zur Patientin bringen. Inwiefern wir damit einen Beitrag zum gesunden Altern der Bevölkerung liefern können, wird gerade intensiv beforscht. Bislang zeigt sich, dass sich Multimorbidität von chronischen Erkrankungen stark geschlechtsspezifisch entwickelt. Um dieses Geschehen besser zu verstehen und geeignete Interventionen entwerfen zu können, bedarf es eines multidisziplinären Ansatzes und eines besseren Zuganges zu Daten für Forschungszwecke, um diese Entwicklungen weiter vorantreiben zu können.
KOMMENTAR | Big Data als Brücke zur personalisierten und Gendermedizin
 Univ.-Prof. Dr. Alexandra Kautzky-Willer
Univ.-Prof. Dr. Alexandra Kautzky-Willer
Leiterin der Gender Medicine Unit der Medizinischen Universität Wien und des Gender Instituts Gars am Kamp
Der Big-Data-Ansatz ermöglicht einen völlig neuen Zugang zur individuellen geschlechtsspezifischen Medizin. Aus Real-World-Daten können Cluster von klinischen Charakteristika oder Komorbiditäten erkannt werden, die eine Zuordnung einzelner Individuen in eine bestimmte Risikokategorie ermöglichen. Das wiederum kann dann eine Entscheidungshilfe für bestimmte Präventions- oder Therapieoptionen darstellen. Geschlecht und Alter stellen hierbei wichtige Merkmale dar. Neben dem biologischen Geschlecht spielen auch soziale und Umweltfaktoren, die in „Gender“ einfließen, eine wichtige Rolle.
So konnten wir zum Beispiel anhand von Daten der Sozialversicherungsträger erkennen, dass bei Diabetes unterschiedliche Zusammenhänge zwischen der antidiabetischen Therapie und dem Risiko für verschiedene Krebserkrankungen zwischen Männern und Frauen vorliegen. Ebenso fand sich dosisabhängig ein höheres Risiko für Osteoporose unter Statintherapie, das vor allem bei postmenopausalen Frauen bedeutsam ist. Im Alter von 50 bis 60 Jahren hatten Frauen mit metabolischem Syndrom ein dreifach höheres Risiko für kardiovaskuläre Komplikationen, wohingegen Männer ein zweifach höheres Risiko aufwiesen.
Der Gender-Gap ist bei Depression unter Diabetes-Erkrankten noch größer als in der nichtdiabetischen Bevölkerung. Big Data können dabei helfen, das individuelle geschlechtsspezifische Krankheitsrisiko besser einzuschätzen.