Die venöse Thromboembolie (VTE) setzt sich aus der tiefen Beinvenenthrombose (TVT) sowie, als deren mögliche Komplikation, der Pulmonalarterienembolie (Lungenembolie, PAE) zusammen.
Diagnostik der VTE
Die Diagnostik der TVT erfolgt heute meist mittels Kompressionssonografie. Mit Hilfe der Vortestwahrscheinlichkeit, die anhand von thromboseförderlichen Erkrankungsbildern und klinischen Zeichen einer Thrombose in einem Punkteverfahren die Wahrscheinlichkeit für ein VTE angibt, und dem Laborwert D-Dimer kann man gemeinsam mit der Kompressionssonografie eine Beinvenenthrombose sicher diagnostizieren bzw. bei niedriger Vortestwahrscheinlichkeit und negativem D-Dimer auch sicher ausschließen. Sollte aufgrund mangelnder Erfahrung die Sonografie nicht in den gesamten Abschnitten möglich sein, ist auch eine Reduktion der Sonografie auf eine Zwei-Punkt-Sonografie (Leiste und Kniekehle) möglich, wobei jedoch eine zeitnahe Kontrolle der Bildgebung nach einigen Tagen zum sicheren Ausschluss einer progredienten venösen Thrombose empfohlen wird. Auch wenn dieses Vorgehen in den rezenten deutschen AWMF-Leitlinien so vorgesehen ist, scheint bei entsprechender Expertise eine sonografische Abklärung des gesamten tiefen Leitvenensystems empfehlenswert zu sein.
Die Diagnostik der PAE wird meist mittels CT-Angiografie mit Kontrastmittel durchgeführt. Nur im Einzelfall (wie bei ausgeprägter Kontrastmittelallergie) ist eine Lungenszintigrafie anzudenken, da diese häufig falsch positive Befunde liefert. Weiters ist die Darstellung möglicher anderer Pathologien im Brustraum und somit die Abklärung der Differenzialdiagnosen der Atemnot/des Thoraxschmerzes in der CT-Untersuchung besser möglich (z. B. Darstellung einer möglichen Aortendissektion etc.).
Therapie der VTE
Die Therapie der VTE umfasst die Akuttherapie sowie die Dauersekundärprophylaxe. Diese Therapie besteht in der Hemmung des plasmatischen Gerinnungssystems (Antikoagulation).
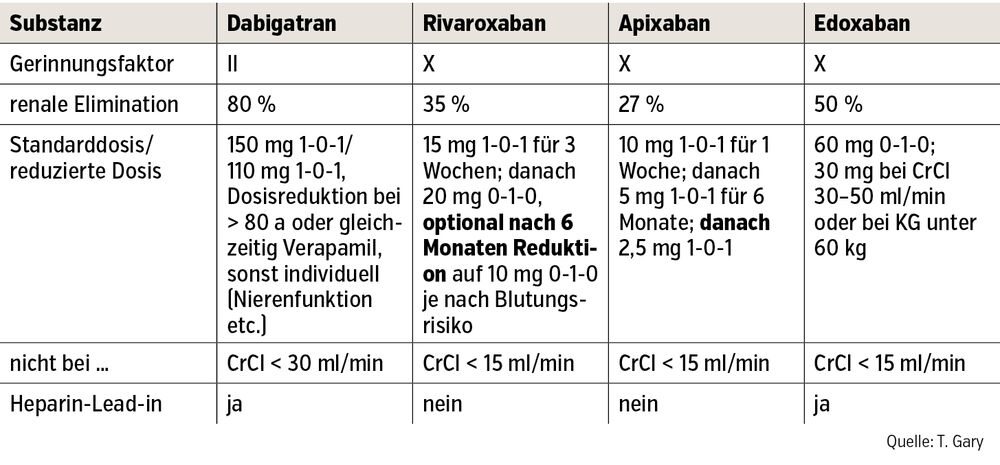
Akuttherapie. In der Akutsituation, in der ein Präparat mit sofortigem Wirkungseintritt benötigt wird, erfolgt die Antikoagulation mit einem Heparinpräparat, dem Pentasaccharid Fondaparinux oder auch Rivaroxaban bzw. Apixaban. In der Praxis ist es wichtig, darauf hinzuweisen, dass aufgrund der unterschiedlichen Studiendesigns bei 2 Substanzen (Dabigatran, Edoxaban) vor Start mit der oralen Therapie zumindest eine 5-tägige Heparintherapie indiziert ist (der sogenannte „Heparin-Lead-in“).
Dauersekundärprophylaxe. Die Dauersekundärprophylaxe erfolgt vorzugsweise mit einem Non-Vitamin-K-Antikoagulans (NOAK, Tab.) oder im Einzelfall mit einem Vitamin-K-Antagonisten (VKA, z. B. beim sehr seltenen Antiphospholipidsyndrom [APS]). Im Falle einer paraneoplastischen VTE hat sich über die Jahre die Dauersekundärprophylaxe mit niedermolekularem Heparin (NMH) als Goldstandard etabliert. Eine Studie aus 2017 hat jedoch gezeigt, dass auch in der Therapie der tumorassoziierten VTE Edoxaban als Alternative verwendet werden kann, da dieses NMH nicht unterlegen ist und auch bei Patient:innen mit Chemotherapie bis zu einer Thrombozytenzahl von 50.000 G/l untersucht und sicher ist. In den darauffolgenden Jahren wurden auch sehr gute Studienergebnisse mit den Faktor-X-Hemmern Rivaroxaban und Apixaban publiziert, sodass derzeit die Therapie mit einem Faktor-X-Hemmer bei den meisten Tumorpatient:innen mit VTE der Heparintherapie vorgezogen wird. Speziell die Therapie mit Apixaban hat bei onkologischen Patient:innen ein äußerst positives Nutzen-Risiko-Profil.
Definition unterschiedlicher VTE-Risikosituationen
Bei der Beurteilung der Dauer der Antikoagulation gilt es, das Re-VTE-Risiko dem Blutungsrisiko gegenüberzustellen. Während früher die VTE in Risikosituation den spontanen VTE-Ereignissen gegenübergestellt wurden, hat sich in den letzten Jahren eine exaktere Aufschlüsselung der Risikosituationen etabliert. Nun werden in der aktuellen Literatur große transiente Risikofaktoren (z. B. Polytrauma, große Operation unter Allgemeinnarkose), große persistierende Risikofaktoren (z. B. aktive Krebserkrankung, APS), kleine persistierende Risikofaktoren (z. B. chronisch entzündliche Darmerkrankung, Übergewicht) und kleine transiente Risikofaktoren (z. B. Schwangerschaft, Pilleneinnahme, Gipsbein) differenziert. In den Gruppen ist das Rezidivrisiko ohne Antikoagulation unterschiedlich und bei großen transienten Risikofaktoren am niedrigsten.
Blutungsrisiko und Rezidivrisiko
Dem Rezidivrisiko muss nun bei der Entscheidung für oder gegen ein Fortsetzen der Antikoagulationstherapie nach den initialen 3 bis 6 Monaten das Blutungsrisiko gegenübergestellt werden. Hier wurde z. B. mit dem VTE-BLEED-Score ein Rechenmodell entwickelt, das mit den Faktoren aktive Krebserkrankung, hoher Blutdruck bei männlichem Geschlecht, Anämie, Blutungsvorgeschichte, Alter > 60 Jahre und eingeschränkte Nierenfunktion die wichtigsten Blutungsrisiken zusammenfasst. Bei den Modellen zur Errechnung des Rezidivrisikos haben sich das Vienna Prediction Model, der DASH-Score und der HERDOO2-Score etabliert. Bei diesen Modellen wird anhand unterschiedlicher Parameter (D-Dimer-Wert nach Absetzen der Antikoagulation, Alter, Geschlecht etc.) versucht, das Rezidivrisiko zu beurteilen.Insgesamt erfordert die Entscheidung über Dauer und Intensität der Antikoagulation (Kasten) stets ein individualisiertes Vorgehen unter Berücksichtigung von Blutungs- und Rezidivrisiko sowie patientenspezifischen Lebensumständen.