Seltene genetische Ursache für Nierensteine
Ungefähr 10 % der Bevölkerung leiden unter Nierensteinen, mit zunehmender Prävalenz insbesondere in Industrieländern.1 Zu den metabolischen Risikofaktoren für Nierensteine zählen vor allem Adipositas und Diabetes.2 Bei einer kleinen Anzahl der Patient:innen mit Nephrolithiasis oder Nephrokalzinose ist jedoch eine monogenetische Variante die Ursache.
Fallbericht
Vorgeschichte und Anamnese. Ein 38-jähriger Mann soll an der Nephrologie Innsbruck wegen einer progredienten Verschlechterung seiner Nierenfunktion vorgestellt werden. Aufgrund eines Arbeitsunfalls mit multiplen Frakturen und Operationen nahm der Patient lange Zeit in höheren Dosen NSAR ein. Des Weiteren hatte er Oxalat-Nierensteine. Die Familienanamnese war negativ für Dialyse, Nierentransplantation und Nierensteine. Also lauteten unsere Differenzialdiagnosen: Analgetika-Nephropathie, CKD-assoziiert mit einer Nierensteinkrankheit, oder eine Oxalat-Nephropathie. Der Patient kam nicht zum Kontrolltermin, wurde aber notfallmäßig in seinem Heimatkrankenhaus mit einem akuten Nierenversagen und Anurie aufgenommen. Nach Beginn der Hämofiltration erfolgte umgehend eine Nierenbiopsie, und der Patient wurde nach Innsbruck überstellt.
Nierenbiopsie und Diagnose. Die Nierenbiopsie ergab die Diagnose einer renalen Oxalose mit Akkumulation von doppelbrechenden Kalziumoxalat-Kristallen in den Tubuli. Des Weiteren zeigten sich eine weit fortgeschrittene interstitielle Fibrose und Tubulusatrophie sowie eine interstitielle Nephritis, passend zur höchstwahrscheinlich terminalen Nierenerkrankung des Patienten (Abb.).
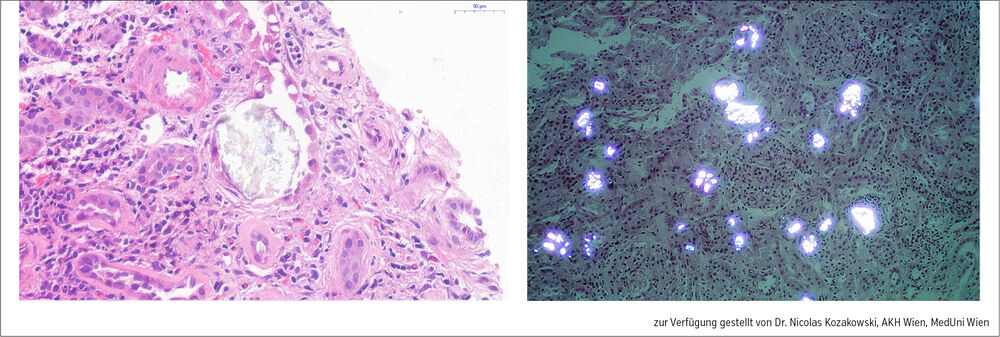
Abb.: Nierenbiopsie bei primärer Hyperoxalurie: linkes Bild: PAS-Färbung mit Kristallen im Tubulus; rechtes Bild: doppelbrechende Oxalat-Kristalle im polarisierten Licht
In der genetischen Analyse fand sich eine homozygote pathogene Mutation des AGXT-Gens, somit war die Diagnose gesichert: primäre Hyperoxalurie Typ 1 (PH1, siehe Kasten). In den weiteren Wochen wurden verschiedene Organbeteiligungen beim Patienten zusätzlich gesichert: Es zeigte sich eine kardiale Beteiligung, nachgewiesen mit kardialem MRT und einer Endomyokardbiopsie (Myokardbiopsat mit subendokardial akzentuierter interstitieller Oxalose), ein klinisch hochgradiger Verdacht auf eine Oxalat-Arthritis und eine sensomotorische, axonale Polyneuropathie.
Therapie. Unser Patient hatte eine homozygote AGT-Variante, die nicht responsibel auf Pyridoxin war. Einer Steigerung der Hämodialysefrequenz auf 6-mal/Woche wollte der Patient nicht zustimmen, immerhin konnten wir diese auf 4-mal 4 h/Woche erhöhen. Die stark erhöhten Plasmaoxalat-Werte (120–160µmol/l) sanken durch die Hämodialyse auf ca. 40 µmol/l ab (–67 bis –75 %), kehrten aber vor der nächsten Hämodialyse wieder auf den Ausgangswert zurück. Wir stellten die Indikation für eine Therapie mit Lumasiran und listeten den Patienten zur kombinierten Leber- und Nierentransplantation (LNTX). Das Ziel der Lumasiran-Therapie war eine Senkung der systemischen Oxalat-Last vor der geplanten Transplantation, um das Risiko einer Oxalat-Nephropathie im Nierentransplantat so niedrig wie möglich zu halten. Ebenso sollten die kardiale Oxalat-Belastung sowie die (vermutliche) Oxalat-Arthritis behandelt werden. Durch die Therapie mit Lumasiran konnte der Oxalat-Rebound um ca. 40–50 % reduziert werden, nach der Dialyse konnten Oxalat-Werte im Normalbereich (< 30 µmol/l) dokumentiert werden.
Als der Patient schließlich ein Organangebot bekam, erfolgten Hämodialysen unmittelbar vor der LNTX und täglich danach. Bei primärer Nichtfunktion des Nierentransplantates erfolgte eine Biopsie, die jedoch einen akuten Tubulusschaden mit unspezifischer Histomorphologie ohne Hinweise auf Abstoßung oder auf ein Rezidiv der Oxalose zeigte. In weiterer Folge erholte sich die Transplantatfunktion, das Serum-Kreatinin ca. 10 Monate nach der LNTX beträgt 1,0 mg/dl, der klinische Verlauf ist erfreulich unauffällig. Wir kontrollierten in unregelmäßigen Abständen die Harnoxalat-Ausscheidung, die sukzessive abnahm und sich nach ca. 6 Monaten im Normalbereich bewegte.
Fazit
PH1 ist eine sehr seltene autosomal-rezessive Erkrankung, die sich vor allem im Kindesalter mit Nierensteinen manifestieren kann. Eine LNTX und/oder eine Therapie mit Lumasiran (evtl. mit einer NTX) stellen therapeutische Möglichkeiten dar, die man mit den Betroffenen und der zuständigen Sozialversicherung diskutieren sollte.























































































