Venöse Thromboembolien bei Diabetes mellitus
Venöse Thromboembolien (VTE), bestehend aus tiefer Beinvenenthrombose (TVT) und Pulmonalarterienembolie (PAE), gehören mit global ca. 10 Millionen Fällen pro Jahr zu den häufigsten Gefäßerkrankungen.1 In den vergangenen Jahren wurde daher auf die Prävention dieser Erkrankung ein besonderes Augenmerk gelegt, wobei nicht nur krankenhausassoziierte Risikofaktoren (z.B. Operationen, Tumoren) untersucht wurden, sondern auch kardiovaskuläre Risikofaktoren.2 Dies hat dazu geführt, dass venöse und arterielle Thromboembolien als unterschiedliche Entitäten wahrgenommen wurden und auch in der Prävention und der Behandlung unterschiedliche Strategien verfolgt werden.2,3
Kardiovaskuläre Risikofaktoren: Trotz allem ist es nicht gänzlich geklärt, welche kardiovaskulären Risikofaktoren venöse wie auch arterielle Thromboembolien betreffen, und verschiedene Studien lieferten gegensätzliche Ergebnisse.4–14
In einer über 1,1 Millionen Patient:innen einschließenden prospektiven Studie wurde die Assoziation verschiedener etablierter kardiovaskulärer Risikofaktoren und VTE untersucht. Kardiovaskuläre Risikofaktoren, die in dieser Studie gefunden wurden, sind höheres Alter (HR pro Lebensdekade 2,67; 95%-KI 2,45–2,91), aktiver Nikotinkonsum (HR 1,38; 95%-KI: 1,20–1,58) sowie höherer BMI (HR per 1-SD höherer BMI 1,43; 95%-KI 1,35–1,50). Außer bei Adipositas, die eine stärkere Assoziation mit PAE aufweist, waren die HR einzelner Risikofaktoren für TVT und PAE vergleichbar. Inkonsistente Ergebnisse zeigten sich jedoch für Diabetes wie auch für die arterielle Hypertonie, weshalb von dieser Studie keine weiteren Aussagen dazu extrapoliert werden können.15
Antikoagulation bei Adipositas
Obwohl Fachgesellschaften direkte orale Antikoagulanzien (DOAK) als Erstlinientherapie zur Therapie und Prävention der VTE empfehlen, gab es weiterhin Unsicherheiten bezüglich der Effektivität und Sicherheit bei deren Anwendung bei Patient:innen mit Adipositas. Da die Prävalenz der Adipositas stetig steigt, müssen öfter auch Therapieentscheidungen in diesem Patientenkollektiv getroffen werden. Vor wenigen Jahren wurde auch von der International Society of Thrombosis and Haemostasis (ISTH) empfohlen, DOAK bei Patient:innen mit extremer Adipositas nicht anzuwenden und Tal- und Spitzenspiegelbestimmungen durchzuführen, sollten sie trotzdem zur Anwendung kommen.16 Für die aktuellen Empfehlungen der ISTH bezüglich der Anwendung von DOAK bei Patient:innen mit Adipositas konnten jedoch nun vorliegende Ergebnisse aus Phase-III- und Phase-IV-Studien und Metaanalysen herangezogen werden. Prinzipiell wurden 2 Ansätze dahingehend betrachtet: 1.DOAK versus Vitamin-K-Antagonisten in unterschiedlichen Gewichtsklassen und 2. DOAK in unterschiedlichen Gewichtsklassen je nach DOAK-Präparat bzw. gepoolt (Tab.).17
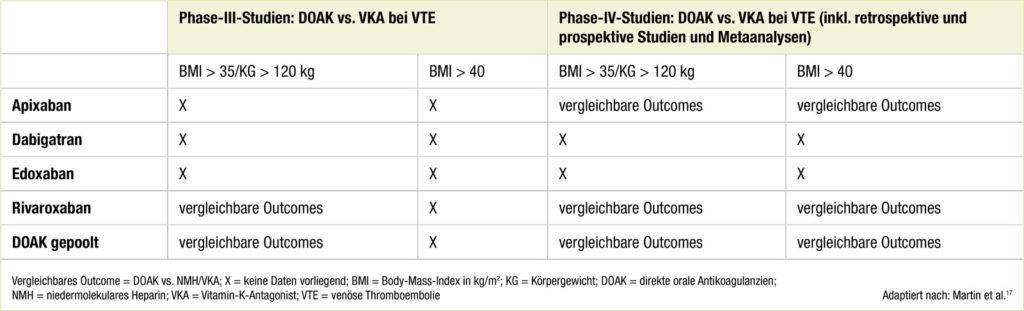
Tab.: Zusammenfassung von klinischen Studien bezüglich Effektivität und Sicherheit in der Behandlung von VTE: DOAK und VKA vergleichend bei Patient:innen mit Adipositas
In Zusammenschau der vorliegenden Daten wurden 2021 folgende Empfehlungen zur Anwendung von DOAK bei Patient:innen vonseiten der ISTH abgegeben17:
- Für die Therapie der VTE wird eine Standarddosis von Rivaroxaban oder Apixaban unabhängig von BMI-Kategorie und Körpergewicht empfohlen (weniger supportive Daten für Apixaban als für Rivaroxaban). Vitamin-K-Antagonisten, eine körpergewichtsadaptierte Dosis von niedermolekularem Heparin (je nach Fachinformation) und Fondaparinux stellen weitere Optionen dar.
- Als VTE-Prophylaxe wird ebenfalls die Standarddosis von Apixaban oder Rivaroxaban für die jeweiligen Zulassungen (nach Hüft-/Kniegelenkersatz) empfohlen.
- Die Anwendung von Dabigatran und Edoxaban für die Therapie und Prophylaxe der VTE bei Patient:innen mit BMI > 40 kg/m2 oder Körpergewicht > 120 kg wird aufgrund der fehlenden Datenlage weiterhin nicht empfohlen.
- Eine regelmäßige Bestimmung von Tal- und Spitzenspiegelwerten wird aufgrund unzureichender Daten, wie diese das weitere Management beeinflussen sollen, nicht empfohlen.
- Im Akutsetting von bariatrischen Operationen sollen DOAK für die Therapie und Prävention der VTE aufgrund einer möglichen herabgesetzten Absorption nicht angewendet werden. Stattdessen sollte in der Akutphase eine parenterale Antikoagulation verwendet werden. Eine Umstellung auf ein DOAK oder einen Vitamin-K-Antagonisten sollte nach frühestens 4 Wochen unter Monitoring der Talspiegel zur Abschätzung einer möglichen Absorptionsstörung oder herabgesetzter Bioverfügbarkeit erfolgen.
Am diesjährigen Kongress der Gesellschaft für Thrombose- und Hämostaseforschung wurde eine Pilotstudie präsentiert, in der bei Patient:innen in unterschiedlichen Gewichtsklassen einschließlich Adipositas und unter laufender Antikoagulation mit Edoxaban oder Rivaroxaban Gerinnungsparameter inklusive Anti-Xa-Spiegel und Plasmakonzentrationslevels bestimmt wurden. Es zeigte sich, dass die bestimmten Gerinnungsparameter unabhängig von der Körpermasse wie auch Körperzusammensetzung sind, was auch in der Anwendung bei Patient:innen mit Adipositas auf eine ausreichende Effektivität von Edoxaban und Rivaroxaban schließen lässt. Weitere Daten in größeren Populationen, vor allem bei Patient:innen mit Adipositas, werden notwendig sein, um diese Resultate zu bestätigen und somit auch mehr Sicherheit für die Anwendung dieser Substanzen in der klinischen Praxis geben zu können.18
VTE und Diabetes mellitus
Wie bereits eingangs dargestellt, konnte in den vorliegenden Studien keine klare Assoziation zwischen Diabetes mellitus und VTE gefunden werden.5–7 Jedoch wurde in diesen Studien nicht zwischen Typ-1- und Typ-2-Diabetes unterschieden; zudem wurde nur sehr spärlich untersucht, ob das Risiko für VTE bei Patient:innen mit Typ-1-Diabetes erhöht ist. In einer Studie konnte gezeigt werden, dass bei Patient:innen mit Typ-1-Diabetes unter Berücksichtigung von Dyslipidämie, arterieller Hypertonie, Insult, Fraktur einer unteren Extremität oder stattgehabter Operation sowie Adipositas das Risiko im Vergleich zur Gruppe der Patient:innen ohne Typ-1-Patienten erhöht ist (adjustierte HR 5,33; 95%-KI: 3,57–7,96).19
Die Assoziation zwischen Typ-1-Diabetes und VTE-Risiko konnte auch in einer weiteren Studie von Hinton et al. gezeigt werden. Die publizierten Daten zeigen, dass Patient:innen mit Typ-1-Diabetes – adjustiert für Alter, Geschlecht, Body-Mass-Index, Nikotinkonsum, chronische Nierenerkrankung, Begleitmedikation mit Aspirin, Metformin und Statinen sowie Vorhofflimmern – ein erhöhtes Risiko für VTE haben (HR 1,46; 95%-KI: 1,11–1,92).20
Auch wenn bis dato eine klare Assoziation nur für Typ-1-, jedoch nicht für Typ-2-Diabetes gezeigt werden konnte, stellte sich häufig die Frage, ob antidiabetische Therapien, die bei Patient:innen mit Typ-2-Diabetes verschrieben werden, zu einem erhöhten VTE-Risiko führen könnten.
Dipeptidylpeptidase-4-Inhibitoren (DPP-4i) werden regelmäßig als antidiabetische Zweitlinientherapie bei Patient:innen mit Typ-2-Diabetes verschrieben. Eine rezent durchgeführte Pharmakovigilanzstudie, die anhand der Datenbank der Weltgesundheitsorganisation (WHO) durchgeführt wurde, zeigte ein konsistentes Signal, dass DPP-4i mit VTE-Ereignissen (PPR: 2; 95%-KI: 1,7–2,3) und insbesondere mit viszeraler VTE (PPR 13,4; 95%-KI: 9,2–19,6) assoziiert sind.21 Jedoch muss an diesem Punkt auf einige Schwächen von Meldedatenbanken hingewiesen werden, wie z. B. Meldungsbias und Meldungsdaten. Eine Metaanalyse von 5 großen kardiovaskulären Endpunktstudien, welche die Assoziation zwischen DPP-4i und VTE-Risiko analysiert, zeigte keine signifikante Assoziation (OR 1,12; 95%-KI: 0,81–1,55). Zwischen den unterschiedlichen DPP-4i wurde ebenfalls kein Unterschied gefunden (p = 0,50). Das zuvor gefundene Signal zwischen DPP-4i und viszeraler VTE konnte in dieser Metaanalyse ebenfalls nicht bestätigt werden.22
Durch den diuretischen Effekt der SGLT2-Inhibitoren (i) wurde der Verdacht geweckt, dass dies zu einer Hämokonzentration führen könnte und somit ein erhöhtes VTE-Risiko besteht. Eine skandinavische Studie, die SGLT2i und GLP-1-Rezeptor-Antagonisten (RA) in Hinblick auf das VTE-Risiko untersuchte, zeigte hier eine neutrale Assoziation in der gesamten Studienpopulation wie auch in allen Subgruppen.23 Diese Ergebnisse wurden auch in einer populationsbasierten Studie bestätigt, die knapp 220.000 Patient:innen einschloss. Auch hier zeigte sich, dass VTE-Ereignisse bei Patient:innen unter einer Medikation mit SGLT2i seltener auftreten als bei Patient:innen unter einer Medikation mit DPP-4i (RR 0,75; 95%-KI: 0,59–0,94).24
Interessanterweise haben Patient:innen mit Diabetes mellitus und VTE häufiger einen komplizierten Verlauf als Patient:innen ohne Diabetes mellitus. Dies ergab eine populationsbasierte Studie von Piazza et al. Unter anderem wurde gezeigt, dass Patient:innen mit Diabetes mellitus häufiger rezidivierende VTE-Ereignisse (14,9% vs. 10,7%; p = 0,01) sowie mehr schwere Blutungen unter der Antikoagulation erleiden (16,4% vs. 11,7%; p = 0,01).25
Resümee
Typ-1-Diabetes mellitus wie auch Adipositas gehen mit einem erhöhten Risiko für venöse Thromboembolien bei diesem Patientenkollektiv einher. Für die Therapie der venösen Thromboembolien können bei Patient:innen mit Adipositas nach jetzigem Wissensstand Apixaban wie auch Rivaroxaban bezüglich Effektivität und Sicherheit angewendet werden. In Studien, in denen DOAK mit Vitamin-K-Antagonisten bei nichtvalvulärem Vorhofflimmern untersucht wurden, wurden auch zu circa 30% Patient:innen mit Diabetes mellitus inkludiert, die ähnliche Risikoreduktionsraten im Vergleich zu Patient:innen ohne Diabetes mellitus zeigten.26
Für Patient:innen mit Diabetes mellitus, die eine orale Antikoagulation benötigen, werden außer bei einer absoluten Indikation für einen Vitamin-K-Antagonisten (z.B. mechanische Herzklappen) prinzipiell DOAK aufgrund geringerer Blutungsraten und geringeren Monitoringaufwands bevorzugt.27, 28



























































































