Kinder und Jugendliche mit Diabetes mellitus Typ 1
Technologische Innovationen haben das Management des Typ-1-Diabetes (T1D) in den letzten zwei Jahrzehnten grundlegend verändert. Insulinpumpen, kontinuierliche Glukosemessung (CGM) und automatisierte Insulinabgabesysteme (Automated Insulin Delivery, AID) gelten heute als State-of-the-Art-Therapie und haben die herkömmliche Basis-Bolus-Therapie mit Insulin-Pens und kapillären Messungen, insbesondere bei Kindern, weitgehend abgelöst.1 Durch den breiten Einsatz dieser Technologien konnten Kinder und Jugendliche mit T1D ihre glykämische Kontrolle deutlich verbessern. Das spiegelt sich auch in den Therapiezielen internationaler Diabetes-Fachgesellschaften wie der American Diabetes Association (ADA) oder der International Society for Pediatric and Adolescent Diabetes (ISPAD) wider. Noch vor knapp 20 Jahren empfahl die ADA altersabhängige HbA1c-Ziele von bis zu 8,5 %, und noch 2019 galt ein einheitliches Ziel von < 7,5 % (< 58 mmol/mol) für alle Kinder. Aktuell werden dagegen < 7 % (< 53 mmol/mol) bzw. bei Einsatz moderner Technologien sogar < 6,5 % angestrebt.2, 3
Kontinuierliche Glukosemessung und Insulinpumpen
Heute verfügbare CGM-Systeme sind klein, präzise und einfach anzuwenden – eine Kalibrierung per Blutzuckermessung ist nicht mehr nötig. Via alle 7–14 Tage subkutan platzierte Sensoren findet eine kontinuierliche Glukosemessung statt, die Daten werden dabei in Echtzeit auf kleine Auslesegeräte bzw. Apps auf Mobiltelefon/Smartwatch oder direkt auf die Pumpe übertragen. CGM-Systeme haben die kapilläre Messung im Bereich des T1D weitgehend ersetzt, mit Ausnahme spezieller Situationen wie der Bestätigung von Hypoglykämien oder zur Kalibrierung ungenauer Sensorwerte (sofern möglich).1 Die CGM-Technologie ist heute ein zentraler Bestandteil des Diabetesmanagements. CGM-spezifische Parameter, insbesondere die „Zeit im Zielbereich“ (Time in Range, TiR), also der Prozentsatz der Zeit, in der die Glukosewerte zwischen 70 mg/dl und 180 mg/dl liegen, haben sich sowohl in der Klinik als auch in der Forschung als nützliche Parameter etabliert.4 Im Bereich des T1D könnte TiR zunehmend den HbA1c als Hauptindikator der glykämischen Kontrolle ersetzen.5 Aktuell wird neben der mittlerweile etablierten TiR zunehmend auch die Time in normal Glycemia (TiNG), d. h. Werte im normalen Bereich (70–140 mg/dl), als mögliches Therapieziel diskutiert.
Registerdaten: Daten aus dem deutsch-österreichischen Register Diabetes-Patienten-Verlaufsdokumentation (DPV) und dem US-amerikanischen T1D Exchange (T1DX) zeigen einen deutlichen Anstieg der CGM-Nutzung bei Kindern (DPV: 40 % 2017 auf 76 % 2020; T1DX: 25 % auf 49 %).6, 7 In Australien liegt die Nutzungsrate bei unter 21-Jährigen bei 79 %.8 Grund dafür ist neben technologischem Fortschritt vor allem die Kostenübernahme durch Kassen. Auch Insulinpumpen sind weit verbreitet, mit Nutzungsraten bis zu 90 %.9 Die Nutzung von Diabetestechnologien variiert dabei deutlich zwischen verschiedenen Altersgruppen und Ländern auch in westlichen Gesundheitssystemen.10
Automated Insulin Delivery System
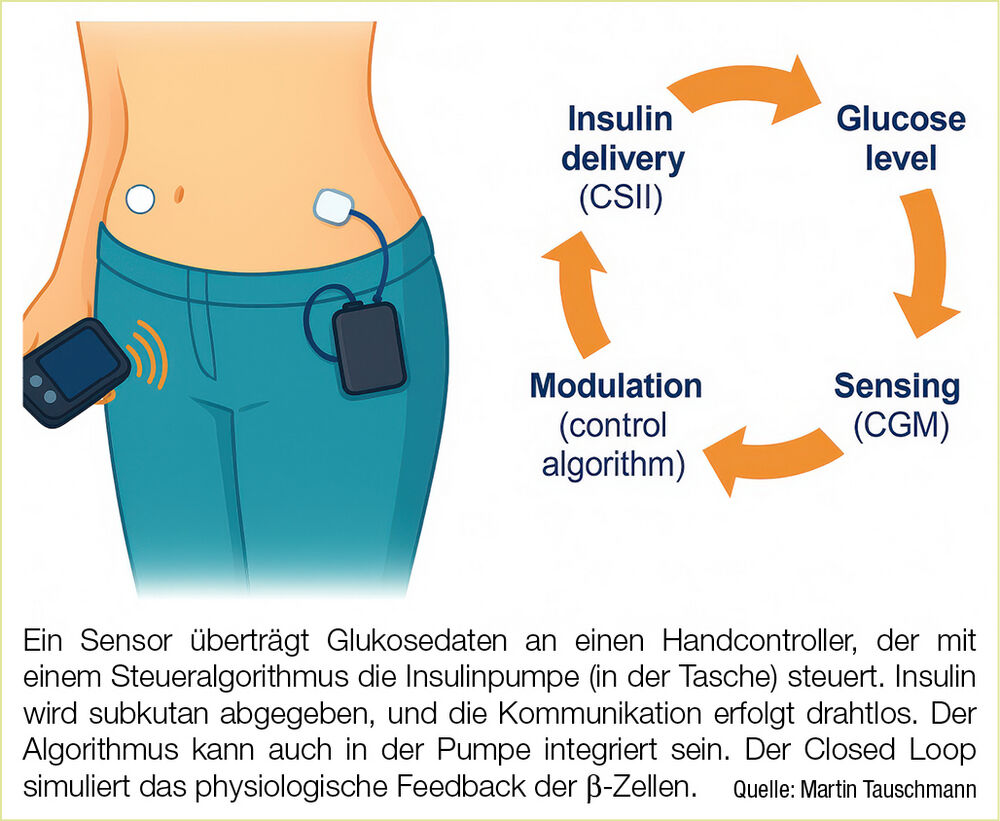
Neben der Kombination von Pumpe und CGM im Rahmen der sensorunterstützten Pumpentherapie (SuP) hat sich vor allem die automatisierte, glukoseabhängige Insulinabgabe bewährt. Frühere Systeme mit (vorausschauender) Hypoglykämieabschaltung zeigten dabei klare Vorteile in der Reduktion von Häufigkeit und Dauer von Hypoglykämien.1 AID-Systeme (Closed Loop oder Artificial Pancreas) sind komplexer als einfache Systeme zur Hypoglykämieabschaltung. Sie regulieren die Insulinabgabe automatisch in kurzen Intervallen, wobei Algorithmen sowohl aktuelle als auch vergangene Sensorglukosewerte berücksichtigen. Eine schematische Darstellung eines AID-Systems und seines Regelkreises ist in der Abbildung zu sehen.
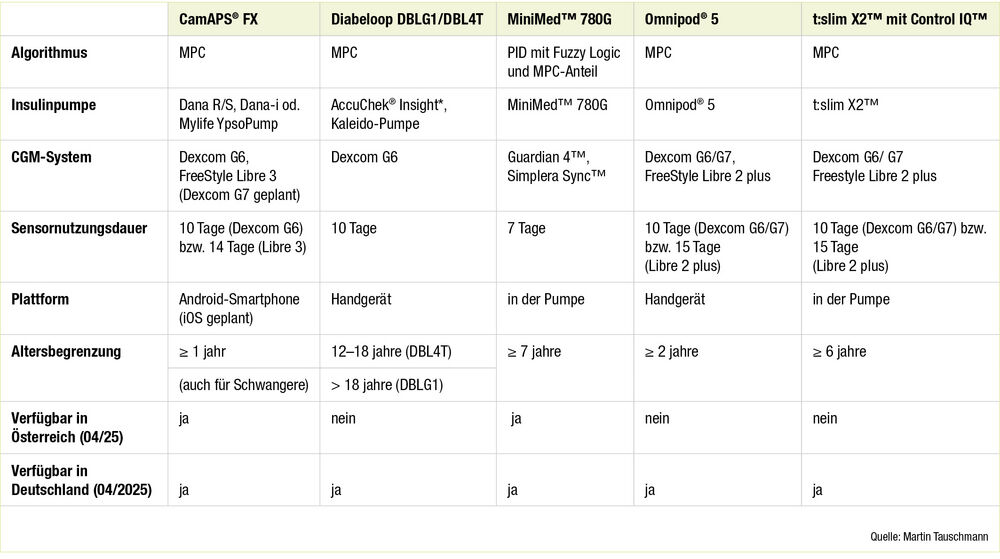
Einsatz in der Praxis: Der AID-Bereich war lange akademisch geprägt. Seit der FDA-Zulassung des ersten kommerziellen AID-Systems (MiniMed™ 670G, Medtronic) im Jahr 2016 wurden mehrere weitere Systeme eingeführt. AID-Systeme gelten in vielen Ländern mittlerweile als Goldstandard für die Versorgung von Kindern und Jugendlichen mit T1D. Die Nutzungsraten sind deutlich ansteigend.11 In den ISPAD-Richtlinien 2024 wird ihr Einsatz, sofern verfügbar, dringend empfohlen.12 Die Tabelle zeigt aktuell CE-zertifizierte AID-Systeme, die in Österreich und Deutschland derzeit kommerziell verfügbar sind. Daneben gibt es noch sogenannte Do-it-yourself- (DIY-) oder Open-Source-Systeme (z. B. OpenAPS, AndroidAPS, LOOP). Durch die langsame Entwicklung und ungleiche Verfügbarkeit von AID-Systemen weltweit entstand unter dem Motto #wearenotwaiting eine Community, deren Mitglieder ihre AID-Systeme eigenständig und in Eigenverantwortung mit online verfügbaren Anleitungen zusammenbauen. 2022 wurde eine Konsensusempfehlung veröffentlicht13, und 2023 erhielt Tidepool Loop als erstes Open-Source-AID-System die FDA-Zulassung.
Evidenz zu AID-Verwendung
Metaanalysen von randomisierten, klinischen Studien (RCT) zeigen, dass AID-Systeme im Vergleich zur Standardtherapie (Pumpe/Pen mit CGM) zu einer höheren TiR, weniger Hyperglykämien und Hypoglykämien sowie einer Senkung der HbA1c-Werte führen, und zwar über alle Altersgruppen mit Typ-1-Diabetes hinweg.14, 15 Auch im pädiatrischen Bereich haben Studien belegt, dass AID-Systeme sicher und effektiv sind und glykämische Ergebnisse verbessern.16–21 Ein früher Einsatz von AID-Systemen, bereits innerhalb weniger Tage oder Wochen nach der Diagnosestellung, hat einen eindeutig positiven Effekt auf die glykämische Kontrolle über einen Zeitraum von bis zu 48 Monaten nach Diagnose im Vergleich zu Systemen ohne Automatisierung.22–24 Neben RCT gibt es mittlerweile auch schon eine Vielzahl von Beobachtungsstudien, deren Real-World-Daten bestätigen, dass Kinder im AID-Modus konstant hohe Zeiten im Zielbereich erreichen und glykämische Vorteile ähnlich denen in RCT erzielen, bei gleichzeitig niedriger Abbruchrate.25–27
Unterschiedliche Konfigurationen von AID-Systemen
Kommerziell verfügbare AID-Systeme (Tab.) nutzen verschiedene Algorithmen zur Insulinberechnung (z. B. MPC, PID, Fuzzy Logic) und unterscheiden sich in Komponenten, Setup, Funktionsweise, modifizierbaren Einstellungen und Altersgrenzen. Einige integrieren den Algorithmus in die Pumpe (z. B. Medtronic MiniMed™ 780G, Tandem Control-IQ™), während modulare Systeme (z. B. CamAPS® FX) den Algorithmus auf externen Geräten ausführen und mit verschiedenen Sensoren und Pumpen kombiniert werden können. Es gibt eine wachsende Entwicklung hin zu Systemen, die mehrere Sensoren unterstützen, was besonders im Hinblick auf die Wahlmöglichkeiten der Nutzer:innen und Hautunverträglichkeiten wichtig ist.
Herausforderungen
Mahlzeiten und Kohlenhydratberechnung
Alle derzeit in Österreich und Deutschland kommerziell verfügbaren AID-Systeme sind Hybridlösungen, bei denen die basale Insulinabgabe automatisch angepasst wird, aber der Mahlzeitenbolus weiterhin manuell abgegeben wird, in der Regel durch genaue Eingabe des Kohlenhydratgehaltes der geplanten Mahlzeit. Fully-closed-Loop-Systeme, bei denen auch der Mahlzeitenbolus automatisch erfolgt, sind zum größten Teil noch in klinischer Testung.28 Der Übergang zu solchen Systemen ist aufgrund der Verzögerung bei der Erkennung postprandialer Glukoseanstiege und Insulinresorption komplex. In rezenten Studien unter Verwendung von kommerziellen Systemen scheint jedoch auch eine vereinfachte Eingabe des Kohlenhydratgehaltes der Mahlzeit bei gleichzeitig akzeptablen Ergebnissen in puncto Glukosekontrolle möglich.29–32
Sport
Menschen mit T1D, die AID-Technologie nutzen, haben bei körperlicher Aktivität mit Verzögerungen zwischen CGM-und Blutzuckerwerten sowie unphysiologisch hohen Insulinspiegeln durch vorhergehende Insulinabgaben („insulin on board“) zu kämpfen, was zu Hypoglykämien führen kann. AID-Systeme bieten spezielle Modi (z. B. Ease-off-, Aktivitäts- bzw. Sportmodus, temporäres SG-Ziel), die das Glukoseziel anpassen und Korrekturen reduzieren. Diese sollten idealerweise 60–120 Minuten vor der Aktivität aktiviert werden, wobei die genaue Empfehlung je nach Art und Intensität des Sports variieren kann. Ein kürzlich veröffentlichtes Positionsstatement fasst Empfehlungen zur Nutzung von AID-Systemen bei Sport zusammen.33
Resümee…
In den letzten zwei Jahrzehnten haben Innovationen bei Insulinpumpen und kontinuierlichen Glukosemesssystemen die traditionelle Basis-Bolus-Therapie ersetzt. Automatisierte Insulinabgabesysteme, die CGM und Pumpen kombinieren, bieten eine bessere glykämische Kontrolle und sind in vielen Ländern der Goldstandard für Kinder und Jugendliche mit T1D. Diesen Fortschritten entsprechend wurden auch die Therapieziele angepasst: HbA1c-Ziele wurden gesenkt, und die „Zeit im Zielbereich“ gewinnt zunehmend an Bedeutung. Die Zahl der verfügbaren AID-Optionen wächst, und internationale Richtlinien empfehlen ihren Einsatz insbesondere für Kinder und Jugendliche, idealerweise früh nach Diagnose.
…und Ausblick
Die Entwicklung von AID-Systemen schreitet kontinuierlich voran. Neben dem geplanten Einsatz von Sensoren, die nicht nur Glukose, sondern auch andere Parameter wie Ketone messen können34, wird sich auch der Einsatz von künstlicher Intelligenz basierend auf immer größeren Datenmengen die AID-Algorithmen weiterentwickeln. Ein anderer Fokus wird auch auf der Interoperabilität von CGM-Systemen, Algorithmen und Insulinpumpen liegen. Die weltweite Verfügbarkeit und Kostenerstattung bleiben jedoch Herausforderungen.
Fully-closed-Loop-Systeme werden hybride Systemezukünftig ersetzen; aktuell noch bestehende Hürden bei Mahlzeiten und körperlicher Aktivität werden überwunden werden. Lösungen könnten schnelleres Insulin, anpassungsfähigere Algorithmen und Multi-Hormon-Systeme wie Glukagon oder SGLT2-Inhibitoren sein.35–37