GYN-AKTIV KOMPAKT 2018 − Nachlese zu unserem 4. Fortbildungskongress am 8. 9. 2018, Apothekertrakt Schloss Schönbrunn
Eine professionelle Organisation und Abwicklung in verlässlicher Qualität ist die Grundvoraussetzung für einen nachhaltigen Erfolg eines Fortbildungs-Events: Seit Beginn liegt die Verantwortung dafür in den Händen eines hochprofessionellen Organisationsteams des MedMedia-Partners MedAhead unter der Leitung von Eva Pernek. Auch heuer wieder wurden die TeilnehmerInnen mit Fragebögen um eine Bewertung gebeten, um die Akzeptanz und Verbesserungsmöglichkeiten zu evaluieren. Das für uns sehr erfreuliche Feedback finden Sie grafisch aufbereitet im Info-Kasten „Das Publikums-Feedback“.
Für die inhaltliche Qualität sorgten wieder hochkarätige Vortragende: Univ.-Prof. Dr. Bernhard-Joachim Hackelöer, Hamburg (D), zur „Sonografie und Frühgeburtlichkeit“; Univ.-Prof. Dr. Herbert Kiss, Wien, zu „Virusinfektionen in der Schwangerschaft; Univ.-Prof. Dr. Bettina Toth, Innsbruck, mit einem „Update zur Hormonersatztherapie“; Univ.-Prof. DDr. Johannes Huber, Wien, zu „FSH – die Osteoporose und die menopausale Gewichtszunahme“; Univ.-Prof. Dr. René Wenzl, Wien, referierte „Aktuelle Therapiekonzepte beim Uterus myomatosus“; Univ.-Prof. Dr. Dr. h.c. Heinz Kölbl, Wien, behandelte „Rezidivierende Harnwegsinfekte jenseits der Antibiotikatherapie“ und Assoz. Prof. PD Dr. Ljubomir Petricevic die „Scheidengesundheit“; Assoz. Prof. PD Dr. Christoph Grimm analysierte das Potenzial von „Screening bei Zervix-, Endometrium- und Ovarialkarzinom“ und OA Dr. Wolfgang Pokieser, Wien, die „Praxisrelevanz der neuen gynäkologischen Zytologie-Nomenklatur“; und zum Abschluss sorgte ein Kongress-Stammgast, Univ.-Prof. Dr. Helmut Ofner, Wien, mit der Frage: „Haftet man für Diagnosefehler anderer Fachärzte?“ für intensive Diskussionen im Publikum.
Zum Thema „Quo vadis Zervixkarzinom-Screening?“ fand ein Lunch-Symposium (Fa. Hologic) statt. Ergänzt wurden die Vorträge und Diskussionen auch heuer wieder durch eine informative Industrieausstellung.
Durch das Programm führten die wissenschaftlichen Leiter der Veranstaltung: Univ.-Prof. Dr. Dr. h.c. Heinz Kölbl, Leiter der Klinischen Abteilung für Allgemeine Gynäkologie und Gynäkologische Onkologie, Univ.-Klinik für Frauenheilkunde, Medizinische Universität Wien, und GYN-AKTIV-„Senior Editor“ em. o. Univ.-Prof. Dr. Sepp Leodolter.
Im Folgenden haben wir für Sie einige ausgewählte Tagungsvorträge als kurze Abstracts mit Take-Home-Messages aufbereitet. Weitere Themen aus unserem Kongress wollen wir in den folgenden Ausgaben von GYN-AKTIV publizieren.
Virusinfektionen in der Schwangerschaft
In einem Überblicksvortrag zu Virusinfektionen in der Schwangerschaft behandelte Univ.-Prof. Dr. Herbert Kiss vor allem die Aspekte der Impfprophylaxe und den speziellen Therapiekontext Schwangerschaft.
Die gut verträgliche Impfung gegen Influenza ist wegen der besonderen Gefährdung dieser Risikogruppe sowohl Schwangeren als auch Frauen mit Kinderwunsch vor (und ev. auch noch während) der Influenzasaison (Oktober bis März) zum eigenen Schutz (weniger Hospitalisierungen und Reduktion schwerer Verläufe) und zum Schutz des Neugeborenen empfohlen. Ein verbessertes perinatales Outcome und eine Reduktion von Spitalsaufenthalten bei Influenza in der Schwangerschaft ist nachgewiesen worden.
Die Masernimpfung ist eine neue Herausforderung, da große Immunitätslücken bei jungen Frauen im gebärfähigen Alter bestehen und es auch durch Migration im erhöhten Maße zu Neuerkrankungen gekommen ist. Nicht-Impfung ist mit erhöhten finalen Komplikationen vergesellschaftet und kann zu nicht unbeträchtlichem schlechten Outcome führen. Neugeborene haben ein stark erhöhtes Risiko, als Folge von Masern an SSPE (subakute sklerosierende Panenzephalitis – führt meist zum Tod im Kindesalter) zu erkranken.
Bei fetaler Röteln-Infektion ist aufgrund der Schwere der Fehlbildungen (Röteln-Embryopathie, Fehlbildung stark abhängig vom Zeitpunkt der Infektion) ein Schwangerschaftsabbruch indiziert. Nach bekanntemRötelnkontakt sollte der Antikörper-Status bestimmt werden und bei negativen AK bis SSW 17 eine Amniozentese zum Ausschluss bzw. Nachweis einer fetalen Infektion erfolgen.
Bei Varizellen erfolgt eine Virusübertragung nur bei Primärinfektion. Das Risiko eines kongenitalen Varizellensyndroms (CVS) beträgt bis zur 21. SSW 2 %. Mütter ohne Varizellen in der Anamnese bzw. seronegative Schwangere (vor Immunglobulin aus Kostengründen den Immunstatus überprüfen) sollten bei Varizellenkontakt bis zur 22./23. SSW eine passive Prophylaxe (Varizella-Zoster-Immunglobulin) innerhalb von 72(–96) Stunden nach Kontakt erhalten (Vermeidung einer fetalen Infektion), bei bereits bestehendem Exanthem kann eine antivirale Therapie möglicherweise das kindliche Risiko mindern. Nach SSW 23 ist kein Fall von CVS bekannt.
Ringelröteln (Erythema infectiosum) führt zwar zu keiner Embryopathie, kann jedoch zu aplastischer Anämie, Hydrops fetalis und Abort führen. Insbesondere Hydrops fetalis stellt eine sonografische Herausforderung dar, bei Detektion sollte eine Chordozentese und Transfusion entsprechend dem fetalen Hb erfolgen.
Zytomegalie: Bei seronegativen Frauen kann es zu einer primären Zytomegalie-Infektion in der Schwangerschaft kommen, die oftmals – mit Ausnahme eines grippalen Infekts – inapparent verläuft. Da eine transplazentare Übertragung (in 30–40 %) mit schweren Folgen (ZNS-Schäden, Pneumonitis, Hepato-/Splenomegalie etc.) für den Fötus und auch Spätschäden postpartal verbunden ist, ist eine großzügige Recherche angebracht, wenn ein Verdacht auf eine Zytomegalie-Infektion besteht. Acht Wochen nach maternaler Erstinfektion kann in der Amnionflüssigkeit ein Virusnachweis erfolgen und bei Positivität ein Schwangerschaftsabbruch erwogen werden (bis 15 % post partum auffällig, bis 60 % neurologische Langzeitfolgen). Es gibt keine standardisierte Therapie.
Auf eine Überprüfung des Impfstatus vor allem bei Lebendimpfstoffen (Tab.) sollte schon vor der Schwangerschaft geachtet werden – „Prepare for Pregnancy“ – und Fehlendes laut Impfplan nachgeholt werden.
FSH, Osteoporose und Gewichtszunahme
Zwischen den postmenopausal erhöhten FSH-Spiegeln und einer Osteoporose-Entwicklung gibt es offensichtlich einen wichtigen Zusammenhang. Univ.-Prof. DDr. Johannes Huber präsentierte als Beleg u. a. eine Studie, in der ein Antikörper gegen die β-Einheit von FSH dem Knochendichteverlust durch Stimulation der Knochenbildung und Hemmung des Abbaus eine Schutzwirkung gegen Knochendichteverlust zeigen konnte (Zhu et al., Proc Natl Acad Sci USA 2012).
Aber auch mit der Entwicklung von viszeraler Adipositas ist ein erhöhtes FSH assoziiert und spielt hier eine pathophysiologische Rolle bei postmenopausalen Frauen: Durch FSH-Blockade wird das thermogene braune Fettgewebe und gleichzeitig der Körperfettanteil reduziert (Liu et al., Nature 2017). Hinsichtlich neuer medikamentöser Optionen zur Verbesserung der Fettkomposition des weiblichen Organismus präsentierte Prof. Huber auch neue Daten zum Beta-3-Agonisten Mirabegron (derzeit in der Therapie der überaktiven Blase zugelassen), für den in Studien die Förderung der Umwandlung von weißem Fettgewebe in braunes nachgewiesen wurde (Cypess et al., Cell Metabolism 2014). Die Rationale dahinter: Der lipolytische Effekt von Katecholaminen wie Noradrenalin wird postmenopausal durch verstärkten Abbau durch spezielle Fettgewebs-Makrophagen vermindert („Noradrenopause“). Eine lokale Anwendung (zur Minimierung systemischer Nebenwirkungen) von Mirabegron-Patches wird in Studien untersucht.
Aktuelle Therapiekonzepte beim Uterus myomatosus
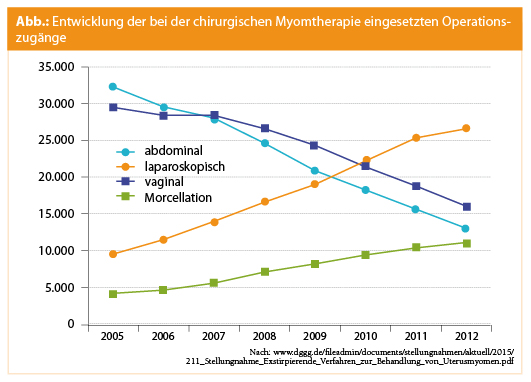
Univ.-Prof. Dr. René Wenzl berichtete über die Therapie bei Uterus myomatosus vor allem im Lichte der Diskussion um das Morcellement, der Indikationsstellung und der weiteren Entwicklung der konservativen Therapie.
Vor dem Risiko der Streuung unentdeckten kanzerösen Gewebes im Rahmen des laparoskopischen Power-Morcellements warnte 2014 auch die FDA. Das Uterussarkom ist allerdings ein sehr seltenes Malignom der Frau. Über 80 % der Patientinnen sind über 50 Jahre alt. Es gibt derzeit keine präoperative Untersuchung bzw. Diagnostik, die zwischen benigner und maligner Entität eindeutig unterscheiden kann.
Nach einem Positionspapier der DGGG (Beckmann et al., 2015) ist eine fundierte wissenschaftliche Aussage zum Risiko eines Uterussarkoms bezogen auf eine einzelne Operationsmethodik (laparoskopisch vs. laparotomisch) nicht möglich. Bei einem diagnostisch suspekten Uterusbefund mit Malignomverdacht wird von einem minimal invasiven Vorgehen allerdings abgeraten.
Nach einer Vergleichsanalyse zum Nettobenefit scheint ein laparoskopisches Vorgehen trotz des erhöhten Streuungsrisikos durch ein Morcellement der Laparotomie doch überlegen (Siedhoff et al., Am J Obstet Gynecol 2017).
Konservative Myomtherapie mit Ulipristalacetat – keine Schifffahrt auf ruhiger See: Der Bedarf an der Entwicklung neuer organerhaltender chirurgischer Therapien, aber auch neuer medikamentöser Therapien als Alternative zum radikalen chirurgischen Vorgehen ist groß, nicht nur wegen der immensen Kosten durch die chirurgische Myomtherapie, sondern speziell vor dem Hintergrund des Fertilitätserhalts bei Frauen im gebärfähigen Alter. Die Zulassung des SPRMs (selektiver Progesteronrezeptor-Modulator) Ulipristalacetat (UPA) vor einigen Jahren aufgrund der Daten des PEARL-Studienprogramms mit signifikanter Reduktion des Myomvolumens und verbesserte Hypermenorrhö-Kontrolle wurde deshalb als großer Fortschritt gefeiert. Nach Pharmakovigilanzdaten mit vermutetem kausalen Zusammenhang einer UPA-Medikation mit schweren Leberschäden als Nebenwirkung wurde heuer allerdings ein EU-Risikobewertungsverfahren zum Arzneimittel Esmya® (UPA 5 mg) eingeleitet, das – erst vor kurzem abgeschlossen – nun teilweise wieder Entwarnung gab. Es besteht also derzeit wieder die Möglichkeit, mit Esmya® zu therapieren, allerdings in den ersten beiden Zyklen unter Kontrolle der Leberwerte in 4-wöchigem Abstand (siehe dazu auch ausführlichen Beitrag von Prof. Kazem Nouri auf S. 48 in diesem Heft).
Probiotika und rezidivierende Harnwegsinfektionen
Bei rezidivierenden Harnwegsinfekten (> 2/Halbjahr oder > 3/Jahr) ist eine Antibiotikatherapie zum einen indiziert, stellt ihrerseits aber auch einen wichtigen ätiologischen Faktor eines HWIs dar (wenn sie in den letzten 2 bis 4 Wochen erfolgte), brachte Univ.-Prof. Dr. Dr. h.c. Heinz Kölbl ein therapeutisches Dilemma auf den Punkt. Es kommt zur Zerstörung der Mikrobiome und darüber hinaus zu Resistenzentwicklungen. Der Verlust der Diversität im „Mikrobiom Harnblase“ korreliert eng mit der Schwere der klinischen Symptomatik bei HWIs (Karstens et al., Front Cell Infect Microbiol 2016).
Probiose als neue Therapieoption zur Rezidivprophylaxe bzw. als Kombinationstherapie: Ein Probiotikum (von gr. pro bios = „für das Leben“) ist eine Zubereitung, die lebensfähige Mikroorganismen enthält. In ausreichenden Mengen oral aufgenommen, können Probiotika einen gesundheitsfördernden Einfluss auf den Wirtsorganismus haben.
Bei der Behandlung und Prophylaxe von HWIs sind sie der Antibiotikabehandlung unterlegen, bei der Prävention komplizierter Harnwegsinfekte haben sie jedoch einen Stellenwert. Vor dem Hintergrund möglicher Antibiotika-Unverträglichkeiten und Resistenzentwicklungen stellen Probiotika (Laktobazillen-Präparate etc.) eine akzeptable Alternative dar und scheinen auch für eine längerfristige Applikation geeignet.
Als Vorgehen in der Praxis wird bei HWI generell empfohlen:
- Orientierung am Leidensdruck und Wunsch der Patientin
- Harndiagnostik
- vermehrte Flüssigkeitszufuhr (~ 1,5 l – nicht mehr!)
- Ansäuerung des Harns (Methionin oder Ascorbinsäure)
- lokale Wärmeapplikation
- Antipyrese und Spasmolyse
- falls gewünscht oder klinisch indiziert: Antibiose 1–3 Tage
- parallel dazu: Probiose (nach Aufklärung)
- Anbieten von Ibuprofen
- bei Symptomfreiheit: Kontrolle nach 1 Woche!
Im Sinne eines „informed consent“, so Prof. Kölbl, sollten Frauen mit HWI auch auf die bemerkenswerten Ergebnisse einer vor wenigen Jahren erschienenen Studie hingewiesen werden, in der 2/3 der Frauen mit unkomplizierten HWI nur mit Ibuprofen und ohne Antibiose symptomfrei wurden (Gagyor et al., BMJ 2015).
Praxisrelevanz der neuen Gyn-Zyto-Nomenklatur
Die neuen Klassifikationen der WHO 2014 der Neoplasien des weiblichen Genitaltraktes (Kurman et al., IARC Press WHO 2014) und der Bethesda-Klassifikation 2015 für die Befunderstellung in der gynäkologischen Zytologie (Nayar R. et al., 2015) ergaben die Notwendigkeit einer Adaptation der österreichische Nomenklatur für gynäkologische Zytologie (Regitnig, Spectrum Pathologie 2017), erläuterte OA Dr. Wolfgang Pokieser, Präpräsident der Österreichischen Gesellschaft für Zytologie.
In der WHO-Klassifikation wurde in der Folge eines großangelegten Projekts in den USA eine weltweit gültige Terminologie für HPV-Läsionen festgelegt. Sie fasst morphologische HPV-Veränderungen und die ehemalige zervikale intraepitheliale Neoplasie Grad 1 (CIN1) zur niedriggradigen intraepithelialen plattenzelligen Läsionen (LSIL) und die ehemaligen zervikalen intraepithelialen Neoplasien Grad 2 und 3 (CIN2 und CIN3) zu hochgradigen intraepithelialen plattenzelligen Neoplasien (HSIL) zusammen.
Seit 1. 1.2018 neue österreichische Nomenklatur: Die Österreichische Gesellschaft für Zytologie (ÖGZ) hat in Zusammenarbeit mit der österreichischen Gesellschaft für Pathologie (ÖGPath) und österreichischen Gesellschaft für Gynäkologie und Geburtshilfe (ÖGGG), vertreten durch Prof. Dr. Elmar Joura und Prof. Dr. Andreas Widschwendter eine neue Nomenklatur erarbeitet, die seit 1. 1.2018 gültig ist. Aufgabe war eine Nomenklatur, die national verbindlich und international vergleichbar ist und eine Weiterentwicklung zur gewohnten Pap-Kategorisierung darstellt. Die Diagnosen sollen risikoadaptiert sein und eine gute Interobserver-Variabilität haben.
Die wichtigsten Unterschiede zur bisherigen Pap-Klassifikation:
- HPV-assoziierte Zellveränderungen (Koilozyten, Dyskeratozyten) gehören zur Gruppe Pap IIID/LSIL. Neue Studien (Darragh et al., Arch Pathol Lab Med 2012) haben ergeben, dass morphologisch eine HPV-Infektion mittels Koilozyten festgestellt werden kann, eine sichere morphologische Unterscheidung zwischen High-Risk- und Low-Risk-HPV nicht möglich ist. Eine Zunahme an Pap-IIID/LSIL-Diagnosen ist deshalb zu erwarten. Hier kommt der HPV-Typisierung in Zukunft eine besondere Bedeutung zu.
- Das unklare Zellbild (PAP III) kann auch Zellen enthalten, die morphologisch eine HSIL sein können. Dies wird verbal im Diagnosetext vermerkt, ist aber eine sehr seltene Diagnose. In der Dünnschichtzytologie kann hier eine p16/Ki-67-Doppelfärbung die Diagnose erleichtern.
Die neue zytologische Nomenklatur wird mit der Erhöhung höhergradiger Zytologiestufen wahrscheinlich zu einer Erhöhung invasiver Diagnostik führen. Der Algorithmus für therapeutische und diagnostische Konsequenzen im Zusammenhang mit der neuen Gyn-Zyto-Nomenklatur ist auf der Homepage der OEGGG ersichtlich – siehe www.oeggg.at/leitlinien-stellungnahmen/gynäkologie-1/.
SAVE THE DATE: Wir würden uns freuen, Sie nächstes Jahr beim 5. GYN-AKTIV KOMPAKT im September 2019 – der wieder im Apothekertrakt Schloss Schönbrunn stattfinden wird – als TeilnehmerInnen begrüßen zu dürfen!
Wissenschaftliche Leiter und Chairmen des 4. GYN-AKTIV KOMPAKT: em. o. Univ.-Prof. Dr. Sepp Leodolter und Univ.-Prof. Dr. Dr. h.c. Heinz Kölbl