UIM 03|2023
Zur Ausgabe »
Nichtvalvuläres Vorhofflimmern (VHF) ist eine häufige Begleiterkrankung bei Patient:innen mit terminaler Niereninsuffizienz (engl. End-Stage Kidney Disease – ESKD), die mit Hämodialyse zur Nierenersatztherapie behandelt werden. Die Prävalenz von VHF bei ESKD-Patient:innen beträgt bis zu 27 %.1 Durch VHF wird bei Hämodialysepatient:innen das Schlaganfallrisiko etwa verdoppelt.2 Das VHF-assoziierte Risiko eines Schlaganfalls stellt eine große klinische Herausforderung dar, weil die aktuelle Evidenz für Antikoagulation bei Hämodialysepatient:innen mit VHF größtenteils auf beobachtungsbasierten Daten beruht. Zudem sind die Ergebnisse dieser Beobachtungsstudien teils widersprüchlich, da sie keinen klaren Vorteil von Vitamin-K-Antagonisten bei der Vorbeugung von Schlaganfällen aufzeigen und ein erhöhtes Risiko für Blutungen im Zusammenhang mit der Antikoagulationstherapie bei Hämodialysepatient:innen belegen.3
Vor dieser Ausgangssituation wurde die VIVALDI-Studie, eine prospektive, bevölkerungsbasierte Beobachtungsstudie, initiiert. Ziel der Studie ist es, die Häufigkeit von Schlaganfällen und schweren Blutungen bei Patient:innen mit ESKD und VHF, die an der Hämodialyse behandelt werden, zu erfassen. Patient:innen wurden an 7 Hämodialyse-Zentren in Wien zwischen 2014 und 2015 innerhalb eines Jahres rekrutiert. Von ca. 860 Patient:innen, die zu dieser Zeit in Wien an der Hämodialyse waren, konnten 626 Patient:innen rekrutiert werden und so einen Großteil der Bevölkerung (73 %) abdecken. Patient:innen wurden über drei Jahre prospektiv beobachtet, letztlich lag die mittlere Beobachtungszeit bei 870 Tagen.
Prävalenz von Vorhofflimmern: Insgesamt wurde zum Einschlusszeitpunkt bei 166 Patient:innen (26,5 %) VHF diagnostiziert. Die VHF-Patient:innen waren überwiegend Männer (71,1 %) mit einem Medianalter von 71,5 Jahren (64–78). Die Prävalenz von VHF stieg mit zunehmendem Alter an, von 8,4 % (14/166) bei Patient:innen unter 55 Jahren auf 41,7% (68/163) bei Patient:innen ab 75 Jahren. Außerdem betrug die Prävalenz von VHF 23,7% bei Patient:innen mit ≤ 1 Jahr Dialysealter und stieg mit zunehmender Zeit an der Hämodialyse auf 32,2 % bei Patient:innen mit mehr als 5 Jahren Dialysealter an.4 In internationalen Registerstudien wird die Prävalenz von VHF bei Dialysepatient:innen zwischen 10 und 27 % geschätzt. Die 26,5 % der VIVALDI-Studie liegen somit im oberen Bereich. Die stringente Erhebung der Erkrankungsgeschichte der VIVALDI-Kohorte zeigt somit eventuell auf, dass die wahre Prävalenz von VHF in großen Registern unterschätzt wird.
Inzidenz von Vorhofflimmern: Während der Beobachtungszeit wurde bei 73 Patient:innen (15,9 % der zuvor nicht an AF erkrankten Patient:innen) de novo VHF diagnostiziert. Somit umfasste die VHF-Kohorte insgesamt 238 Patient:innen (38,1 %). Die Inzidenz von De-novo-VHF bei Hämodialysepatient:innen lag somit bei 7,5 pro 100 Patientenjahre.5
Mortalität: Während der Beobachtungszeit starben 256 Patient:innen (41,0 %) der VIVALDI-Kohorte, was einer Sterblichkeitsrate von 18,2 pro 100 Patientenjahre entspricht. Kardiovaskuläre Todesfälle traten bei 105 Patient:innen auf (16,8 %), mit einer Ereignisrate von 7,5 pro 100 Patientenjahre.
Antikoagulation von Patient:innen mit Vorhofflimmern: Im Rahmen der VIVALDI-Studie wurden auch die Auswirkungen von Antikoagulationsstrategien auf das Risiko für Thromboembolien und schwere Blutungen untersucht.
Die Hauptergebnisse zeigten, dass die Verwendung von Vitamin-K-Antagonisten nicht signifikant mit einem reduzierten Risiko für Thromboembolien verbunden war, aber mit einem erhöhten Risiko für schwere Blutungen und somit insgesamt mit einem klinischen Schaden verbunden sein kann. In der VIVALDI-Studie wurden 61 Patient:innen mit VHF (25,6 % der VHF-Patient:innen) mit einem Vitamin-K-Antagonisten (VKA) behandelt, 38 (16,0 %) mit niedermolekularem Heparin (NMH) an dialysefreien Tagen, und 139 Betroffene (58,4%) erhielten keine Antikoagulation, gemäß der klinischen Entscheidung der betreuenden Ärztinnen und Ärzte. Nach multivariabler Korrektur für Risikofaktoren, wie CHA2DS2-VASc-Score und Antiplättchentherapie, war das Risiko für thromboembolische Endpunkte, Schlaganfall, TIA und systemische Embolie in der Gruppe mit VKA nicht signifikant unterschiedlich (Hazard Ratio [HR] 1,41, 95%-KI 0,49–4,07), das Risiko für schwere Blutungen jedoch 2,3-fach erhöht (95%-KI 1,09–4,79) verglichen mit VHF-Patient:innen ohne Antikoagulation (Abb.).
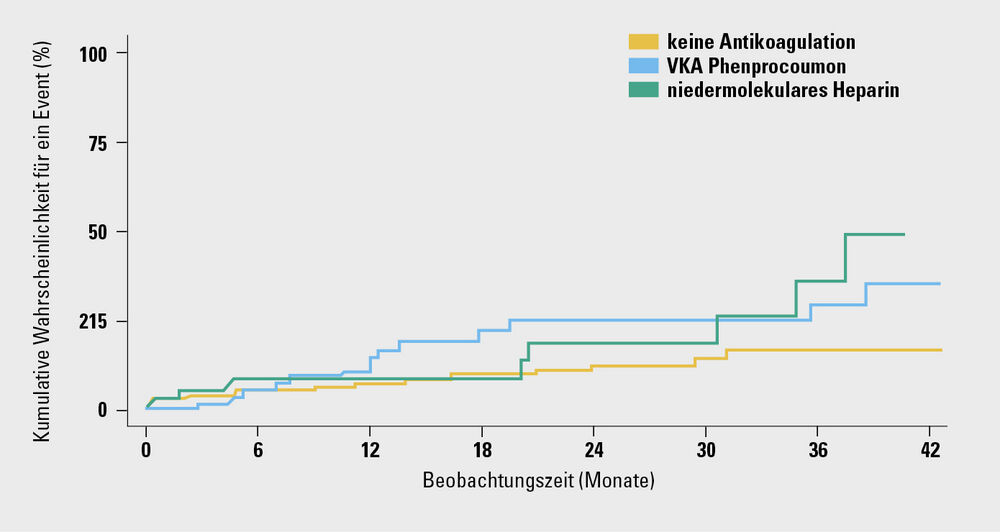
Abb.: Kumulative Wahrscheinlichkeit eines schweren Blutungsereignisses bei Patient:innen mit Vorhofflimmern unter Therapie mit VKA, niedermolekularem Heparin und keiner Antikoagulation im Vergleich
Bei Patient:innen, die eine Antikoagulation mit NMH an dialysefreien Tagen erhielten, war das Schlaganfallrisiko nicht statistisch signifikant reduziert (HR 0,49, 95%-KI 0,11–2,18) und das Blutungsrisiko nicht signifikant erhöht (HR 1,86, 95%-KI 0,81–4,28) verglichen mit nichtantikoagulierten Patient:innen mit VHF.5
Fazit: Trotz der Limitation der Beobachtungsstudie, dass es keine randomisierte und kontrollierte Antikoagulationsbehandlung gab, müssen die Ergebnisse als Warnung betrachtet werden. Antikoagulation bei Dialysepatient:innen ist mit einem hohen Blutungsrisiko assoziiert, das den Vorteil der Schlaganfallprävention übersteigen kann und so insgesamt ein klinischer Schaden verursacht werden kann.
Mögliche nachteilige Effekte von VKA bei Hämodialysepatient:innen: Bei Patient:innen mit terminaler Niereninsuffizienz an der Hämodialyse ist die Verwendung einer VKA-Therapie schwierig, da eine stabile INR durch die Downregulation von CYP450-Isoenzymen bei chronisch urämischen Bedingungen beeinträchtigt wird. In der VIVALDI-Studie wurden longitudinal INR-Werte bei VKA-Patient:innen über den Beobachtungszeitraum erhoben. Daraus wurde die Zeit innerhalb des therapeutischen Fensters (engl. Time in therapeutic Range – TTR) zwischen einer INR von 2,0 und 3,0 errechnet. In der VIVALDI-Studie lag die TTR bei 57 %. Darüber hinaus haben Hämodialysepatient:innen in der Regel mehrere Komorbiditäten und Medikamenteneinnahmen mit potenziellen Interaktionen mit VKA. Die benötigte Dosis von VKA, um therapeutische INR-Werte zu erreichen und aufrechtzuerhalten, nimmt mit sinkender Nierenfunktion ab. Ein weiterer Effekt von VKA bei Patient:innen mit Nierenerkrankung ist das Fortschreiten vaskulärer Kalzifizierung. Patient:innen mit terminaler Niereninsuffizienz leiden häufig an einer Kalziumüberladung, was zu einem Verlust von glatten Gefäßmuskelzellen führt, was wiederum zu Verkalkungen, insbesondere der arteriellen Tunica media und vorbestehenden intimalen atherosklerotischen Plaques, führt. Beide Arten der Verkalkung sind mit einer erhöhten Mortalität bei Patient:innen mit terminaler Niereninsuffizienz assoziiert.
Der physiologische Antagonist des Verkalkungsprozesses ist das Matrix-Gla-Protein, das für seine Carboxylierung Vitamin K benötigt. Die meisten Hämodialysepatient:innen sind jedoch Vitamin-K-defizient, sodass eine Therapie mit Vitamin-K-Antagonisten zu einer weiteren Reduktion von verfügbarem Vitamin K führen und den Verkalkungsprozess beschleunigen kann. Ob das Fortschreiten der vaskulären Verkalkung durch die Vitamin-K-Antagonisten-Therapie die antithrombotischen Vorteile überwiegt, muss noch untersucht werden.
DOAKs als mögliche Alternative: Hämodialysepatient:innen waren nicht in die großen randomisierten Phase-III-Studien mit direkten oralen Antikoagulanzien (DOAKs) bei VHF eingeschlossen, sodass es bei Hämodialysepatient:innen nicht den gleichen Grad an Evidenz für den Einsatz von DOAKs wie in der Allgemeinbevölkerung gibt. Die pharmakokinetischen Eigenschaften von DOAKs sind im Hinblick auf die Hämodialyse von besonderem Interesse. Die Faktor-Xa-Inhibitoren Rivaroxaban, Apixaban und Edoxaban werden größtenteils nicht renal eliminiert. Ein Einsatz der Xa-Inhibitoren bei HD-Patient:innen erscheint somit möglich, und es wurden bereits Bemühungen unternommen, in kleineren randomisierten Studien die Wirksamkeit und Sicherheit von DOAKs gegenüber VKA zu belegen. Die RENAL-AF-Studie mit 154 randomisierten Patient:innen und die AXADIA-AFNET-8-Studie mit 97 randomisierten Patient:innen hatte jedoch jeweils zu geringe Fallzahlen, um ihre jeweiligen Endpunkte im Vergleich zwischen Apixaban und VKA zu erreichen.6,7