UIM 09|2019 Themenheft Pneumologie
Cystische Fibrose – neue Triple-Therapie
Seit der Erstbeschreibung der Erkrankung cystische Fibrose (CF) im Jahre 1936 durch Guido Fanconi hat sich bekanntermaßen bezüglich der Betreuung, der Therapiemöglichkeiten, der Lebensqualität und der Lebenserwartung der Betroffenen ein enormer Fortschritt gezeigt. Die prognostizierte mediane Lebenserwartung der nach 2.000 geborenen Kinder mit CF hat schon das 50. Lebensjahr erreicht, und sehr häufig kann dieser mediane Wert – wie in allen Erwachsenambulanzen zu sehen ist – deutlich überschritten werden. Die markanten Sprünge der Verbesserung der Lebensqualität und -erwartung waren durch die Einführung der Pankreasenzymersatztherapie, das Paradigma der hochkalorischen Ernährung, den frühen Therapiebeginn durch das Neugeborenenscreening, die Therapie mit DNase und die Schemata der inhalativen Antibiotikatherapie zur Suppression bei chronisch Pseudomonas-aeruginosa-besiedelten Patienten möglich.
Kausale Therapie – CFTR-Modulatoren
Die Betreuung in Zentren mit einem multiprofessionellen Team gilt als Voraussetzung, um die Betreuungs- und Therapiekonzepte altersadäquat umsetzen zu können. Die Therapie ist extrem belastend und zeitaufwendig. Erfreulicherweise sind seit 2012 neben der symptomatischen Therapiekonzepte auch Möglichkeiten einer kausalen Therapie zugelassen. Diese kausal wirksamen Medikamente bewirken eine Steigerung des Chloridtransportes beim CFTR-Protein („cystic fibrosis transmembran regulator protein“), welches bei CF nicht genügend gebildet wird oder nicht/zu gering funktioniert, und sie werden als Modulatoren bezeichnet. Eingeteilt werden die Modulatoren in Potentiatoren (Aktivierung des CFTR-Proteins) und Korrektoren (Verbesserung der Struktur des CFTR-Proteins).
Einsatzgebiete
Die Modulatoren können je nach Mutation und Defekt des CFTR-Proteins eingesetzt werden.
Gating-Mutationen: Das klinisch eindrucksvollste Beispiel ist die Therapie mit dem Potentiator Ivacaftor (Kalyedeco®) bei Gating-Mutationen. Hier kann die Aktivität des CFTR-Moleküls um 35–40 % gesteigert werden, was eine enorme Verbesserung aller klinischen Parameter (wie Lungenfunktion, Gewichtszunahme, verminderte Exazerbationen und verbesserte Lebensqualität) zur Folge hat. Die Zulassungsstudie von Ramsey et al. aus dem Jahr 20111 wurde mittlerweile durch Studien in Altersstufen bis zum Säuglingsalter erweitert, sodass Ivacaftor bereits ab dem ersten Geburtstag zugelassen ist2, 3 und eine deutliche klinische Verbesserung im „real life“ zeigt. Der einzige Wermutstropfen ist, dass die Hauptmutation der Gating-Mutationen G544D (irische Mutation) in Mitteleuropa nur bei 2–3 % der Patienten vorkommt.
Homozygote F508del-Mutation: Der nächste Schritt der Modulatorentherapie betrifft die häufigste der bei uns vorkommenden Mutationen: F508del homozygot. Diese betrifft 50 % der österreichischen Patienten. Da bei dieser Mutation das CFTR-Molekül so schlecht gebildet wird, dass es die interne Zellkontrolle im Golgi-Apparat nicht übersteht und entsorgt wird, ist eine kombinierte Therapie mit einem Korrektor und einem Potentiator erforderlich. Mit dieser Kombinationstherapie – Lumacaftor und Ivacaftor (Orkambi®) – kann die CFTR-Aktivität auf 25 % gesteigert werden. Lumacaftor/Ivacaftor ist ab dem zweiten Lebensjahr zugelassen und bewirkt eine Verbesserung der Lungenfunktion um 3–4 %, aber vor allem eine signifikante Reduktion der pulmonalen Exazerbationen. Im Zweijahresverlauf zeigt sich eine signifikante Verbesserung der Lungenfunktion gegenüber nicht mit Modulatoren behandelten Patienten. Auch im Real-Life-Setting finden diese Stabilisierung und die deutlich verminderten Exazerbationen in allen Altersstufen Bestätigung.4–7
F508del/Residual-Function-Mutationen: Bezüglich eventueller Nebenwirkung mit Dyspnoe bei Therapieeinstellung und erhöhten Leberfunktionsparametern sowie Interaktion mit allen CYP3A-metabolisierenden Medikamenten ist der Einsatz bei einer Erkrankung wie CF mit den multimodalen Therapienotwendigkeiten nicht immer leicht. So muss bei Therapien mit Makroliden, Antimykotika, Antidepressiva, Rifampicin, aber auch mit Ovulationshemmern diese Interaktion genau beachtet werden und die Therapie mit dem Modulator eventuell abgesetzt werden. Diese Interaktionen und die Nebenwirkungen Dyspnoe und Leberbeeinträchtigung sind mit dem Korrektor der zweiten Generation Tezacaftor, der ähnliche Ergebnisse wie Lumacaftor zeigt und ab dem zwölften Lebenjahr zugelassen ist, deutlich vermindert, sodass nun dieses Medikament als Tezacaftor/Ivacaftor (Symkevi®) + Kalydeco® seit 2018 für F508del homozygot, aber auch für die „compound“ heterozygoten Mutationen F508del/Residual-Function zur Verfügung steht.8, 9
Resümee: Insgesamt sind mit diesen Möglichkeiten der Modulatoren die Hälfte aller Mutationen abgedeckt (Stand: 10.2019, Tab.): Gating-Mutationen (sowohl homozygot als auch „compound“ heterozygot mit allen anderen Mutationen), F508del homozygot und F508del/Residual-Function-Mutationen.
Triple-Combination-Regime
Um die Ergebnisse für F508del-homozygote Patienten zu verbessern sowie auch eine Therapieoption mit Modulatoren für Mutationen, die bisher nicht profitieren konnten, zu erreichen, wurden mehrere Korrektoren getestet, und letztendlich wurde im „Triple-Combination-Regime“ die Substanz Elexacaftor, ein zusätzlicher Korrektor mit sehr erfreulichen Daten, als „add-on“ ausgewählt. Die Aktivierung des CFTR-Proteins beträgt 40 % und zeigt somit eine ähnlich erfreuliche Verbesserung wie Ivacaftor bei den Gating-Mutationen. Ende Oktober 2019 wurde diese Dreifachkombination aus den beiden Korrektoren Tezacaftor und Elexacaftor sowie dem Potentiator Ivacaftor von der FDA zugelassen (Trikafta®).
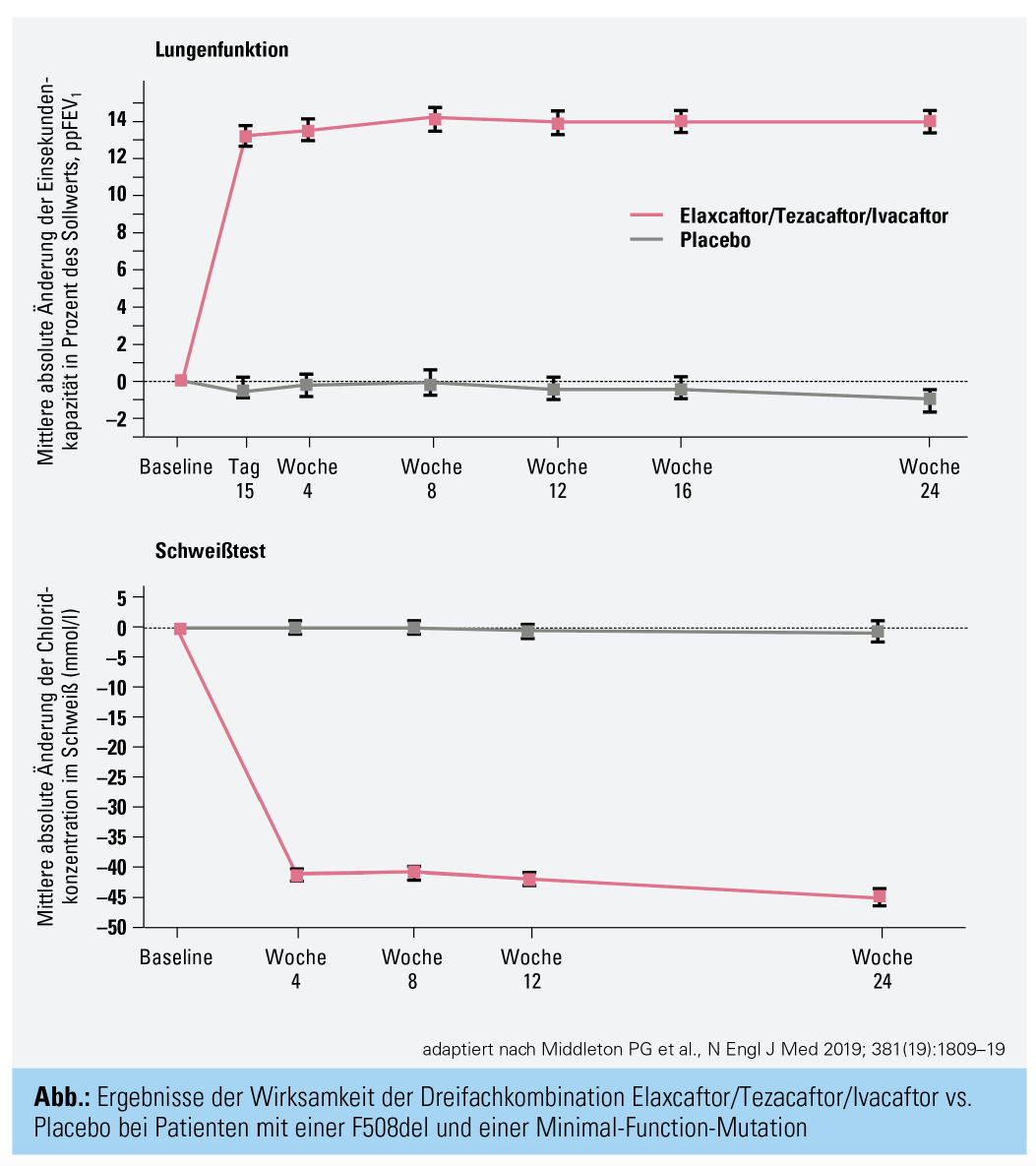
Die Ergebnisse dieser „Triple-Studie“ der US-Studienzentren wurden bereits in einer Presseaussendung im Mai 201910 kurz vor dem europäischen CF-Kongress und Ende Oktober 2019 beim nordamerikanischen CF-Kongress vorgestellt. Diese rezent publizierten Ergebnisse zeigten für Patienten mit einer F508del und einer Minimal-Function-Mutation unter der Dreifachkombination Elaxcaftor/Tezacaftor/Ivacaftor vs. Placebo eine signifikante Verbesserung der Lungenfunktion (um 13,8 % nach 4 und um 14,3 % nach 24 Wochen, Abb.). Zusätzlich kam es zu einer signifikanten Reduktion der pulmonalen Exazerbation gegenüber Placebo um 63 % im Studienzeitraum von 24 Wochen. Der CFQoL (Quality-of-Life-Fragebogen) und die Gewichtsentwicklung waren ebenfalls deutlich verbessert. Auch die Chloridkonzentration im Schweißtest als funktioneller Parameter der Wirkung konnte nach 24 Wochen gesenkt werden, um beachtliche 41,8 mmol/l (Abb.). Die Nebenwirkungsrate in Therapie- und Placebogruppe weist keinen Unterschied auf; Nebenwirkungen zeigten sich vor allem als die krankheitsbedingten pulmonalen Exazerbationen.11 An die placebokontrollierte Studie wurde eine zweijährige Open-Label-Studie angeschlossen, die noch am Laufen ist; Ergebnisse werden in einem Jahr erwartet. Klinisch können die Studienteilnehmer eine deutliche Verbesserung aller Parameter bestätigen.Die Ergebnisse werden in der internationalen Presse als „Miracle“ und „Game changer“ bezeichnet. Bei der EMA ist die Zulassung eingereicht.
Fazit
Diese Ergebnisse sind eine große Hoffnung für viele Patienten, aber auch für Betreuer. In Summe kommt damit in Österreich für ca. 85 % aller Mutationen eine Modulatorentherapie, und somit ein kausaler Therapieansatz, in Frage. Nicht zu vergessen ist, dass alle diese Studien unter Beibehaltung der symptomatischen CF-Therapie durchgeführt wurden, das bedeutet, dass alle erwähnten symptomatischen Therapien weiter erfolgen müssen. Zusätzlich ist das strenge Regime der Einnahme der Korrektoren und Potentiatoren, nämlich alle zwölf Stunden mit einer fettreichen Mahlzeit inklusive Verdauungsenzyme, für mache Patienten eine große Herausforderung. Nach wie vor verbleibt eine Patientengruppe von 15 %, die mit den derzeit untersuchten Modulatoren auf Grund ihrer Mutation keinen Therapieeffekt aufweisen. Für dieses Patientenkollektiv ist zu hoffen, dass bald ähnliche Substanzen als kausale Therapie gefunden werden. Die Patienten selbst spüren die Verbesserung bereits in der ersten Therapiewoche, Sätze wie „Ich fühle mich einfach fit, bin weniger verschleimt und die Verdauung klappt besser“ sind keine Seltenheit.