Moderne Einblicke in die MRD
Die Untersuchung der messbaren (minimalen) Resterkrankung (MRD) besitzt prognostische Aussagekraft und ermöglicht die Früherkennung eines Rezidivs nach Therapieversagen. Der MRD kommt somit eine hochrelevante Bedeutung in der Auswahl und der Steuerung einer risikoadaptierten Therapiestrategie zu.
MRD beim Multiplen Myelom:
Auch nach Erreichen einer Komplettremission (CR) nach den aktuellen Kriterien der International Myeloma Working Group (IMWG) ist bei der großen Mehrzahl der Patient:innen mit Multiplem Myelom eine MRD nachzuweisen.1 Ziel ist es, MRD-Negativität (minimale verbleibende Krankheitsnegativität, MRD–) zu erreichen. Die IMWG definiert MRD– als das Fehlen klonaler maligner Plasmazellen bei Patient:innen mit Verdacht auf CR, beurteilt durch Next Generation Flow (NGF) oder durch Next Generation Sequencing (NGS) mit einer Sensitivität von mindestens 10-5.2 Unabhängig von der Methode, mit der die MRD gemessen wird, ist das Vorliegen einer MRD– mit einer signifikanten Verbesserung des Überlebens assoziiert. Sowohl bei Patient:innen mit neu diagnostiziertem (NDMM; transplantabel und nicht-transplantabel) wie auch bei Patient:innen mit relapsiertem/refraktärem Multiplem Myelom (RRMM) ist das Erreichen einer MRD– über den gesamten Krankheitsverlauf hinweg mit einem verlängerten progressionsfreien Überleben (PFS) verbunden – und somit ein starker prognostischer Marker für PFS.3 Eine anhaltende MRD– ist bei transplantierten Patient:innen sowohl 3 als auch 9 Monate nach autologer Stammzelltransplantation (ASZT) mit einem verbesserten Outcome (PFS: p < 0,0001; Gesamtüberleben [OS]: p = 0,2756) vergesellschaftet.4 Trotz der prognostischen Relevanz der MRD-Beurteilung sind bis dato folgende Fragen unbeantwortet:
- Soll die Beurteilung der MRD in die klinische Praxis etabliert werden?
- Sollten CR und MRD– unabhängig/getrennt voneinander betrachtet werden?
- Welche Rolle spielt MRD bei der Behandlung von Hochrisiko-Patient:innen?
MRD routinemäßig erheben?!
Die MRD-Bestimmung ist aktuell kein Standard in den Verlaufsuntersuchungen. Zahlreiche Studien zeigen jedoch eine starke Korrelation zwischen MRD– und PFS.3 In einer retrospektiven Studie konnte belegt werden, dass sich die prognostische Aussagekraft der MRD– auch in die klinische (real-world) Praxis erstreckt.5 In einer Umfrage berichteten 32 von 89 Ärzt:innen, in der klinischen Praxis routinemäßig keine MRD-Bestimmung durchzuführen – die Gründe dafür sind vielfältig (es waren bis zu 3 Antworten erlaubt): nicht in der Lage, einen MRD-Test zu ordern (22 %), unklar, wann die MRD zu erheben ist (22 %), kein umsetzbares Ergebnis (19 %), Kosten/Versicherungsschutz (16 %), Unbehagen bei Knochenmarkaspiration (9 %), unzureichende Test-Sensitivität (3 %), kein geeigneter Surrogat-Endpunkt (3 %).6 Bis dato mangelt es an Evidenz aus prospektiven randomisiert-kontrollierten Studien für den Einsatz von MRD zur Unterstützung der Entscheidungsfindung in der klinischen Praxis. Es besteht aktuell Konsens über geeignete Schwellenwerte für MRD-Assays, der Population, bei der eine MRD-Bestimmung durchgeführt werden soll, dem Report von MRD-Daten und dem Zeitpunkt der MRD-Bewertung. Dafür, wie MRD als Leitfaden für Behandlungsentscheidungen eingesetzt werden soll, fehlt es jedoch an Leitlinien.7 Die Änderung der Behandlung in Abhängigkeit vom MRD-Status verbessert nachweislich das PFS, unabhängig davon, ob Patient:innen MRD-negativ oder MRD-positiv sind.8 Ergebnisse laufender MRD-adaptiver Studien könnten Aufschluss darüber geben, wie der MRD-Status als Leitlinie für die Therapie und den optimalen Zeitpunkt der MRD-Bewertung dienen kann.9−12 Zudem könnte die fortwährende Entwicklung hin zu weniger invasiven Methoden der MRD-Bestimmung künftig ein häufigeres MRD-Monitoring ermöglichen.13
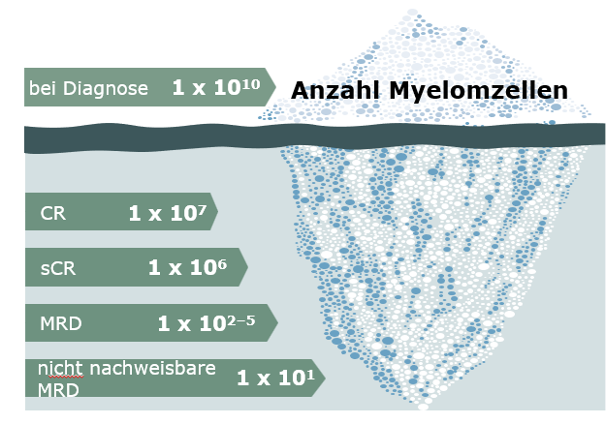
Abb.: Krankheitslast bei Patient:innen mit Multiplem Myelom | modifiziert nach Paiva B et al., Blood 2015; 125: 3059–68 | CR: Komplettremission; sCR: stringente Komplettremission; MRD: minimale Resterkrankung
CR vs. MRD–
Zwischen CR und MRD bestehen wichtige Unterschiede: Während die CR die Bestimmung des M-Proteins, welches als Surrogatmarker für maligne Myelomzellen gilt, erfordert,2 handelt es sich bei der MRD-Bestimmung um eine direktere Echtzeitmessung vorhandener Myelomzellen im Knochenmark.14 Gemäß den aktuellen IMWG-Leitlinien wird eine Testung auf MRD nur empfohlen, wenn der Verdacht auf eine CR besteht.2 Allerdings erreichen nicht alle MRD–-Patient:innen eine CR.15, 16 Diese Diskrepanz zwischen MRD– und CR kann möglicherweise durch einen falsch-positiven Nachweis von M-Protein erklärt werden. Eine Fehlinterpretation des Ansprechens aufgrund von nicht übereinstimmenden MRD- und CR-Ergebnissen kann in klinischen Folgen resultieren.15
Hochrisiko-Patient:innen
MRD–, solange sie aufrechterhalten ist, ist bei Hochrisiko-Patient:innen und Double-Hit-Populationen mit einem verbesserten PFS assoziiert.17 Obwohl Patient:innen mit Hochrisiko-Zytogenetik gut auf eine Induktionstherapie ansprechen, ist die Dauerhaftigkeit des Ansprechens im Vergleich zu Patient:innen mit Standard-Risiko oftmals unterlegen, insbesondere bei Ultra-Hochrisiko-Patient:innen.18, 19 Während viele Patient:innen mit ≥ 2 gleichzeitigen zytogenetischen Hochrisikoanomalien (HRCA) eine MRD–-Rate, die mit jener von Patient:innen mit Standard-Risiko oder 1 HRCA vergleichbar ist, erreichen, weist die Ultra-Hochrisiko-Population das höchste Risiko für ein Wiederauftreten der MRD auf, was folglich in einem schlechteren Outcome (PFS) resultiert. Eine anhaltende MRD– ist somit entscheidend, um die schlechten Überlebensoutcomes bei Patient:innen mit Hochrisiko-Zytogenetik zu überwinden.9 MRD-adaptive Studien könnten dazu beitragen, Behandlungsstrategien für Hochrisiko-Patient:innen auf Basis des MRD-Status festzulegen.9, 19 Neue Behandlungsstrategien für Hochrisiko-Patient:innen sind Gegenstand aktueller Studien, um eine anhaltende MRD– zu erreichen und somit die Langzeit-Outcomes zu verbessern.























































































