Stellenwert von Biomarkern beim SCLC
Das kleinzellige Lungenkarzinom (SCLC) ist ein aggressiver, high-grade neuroendokriner Tumor, der eine Reihe von klinischen, pathologischen und molekularen Charakteristika wie eine enorme genomische Instabilität aufweist und mit einer nach wie vor sehr schlechten Prognose einhergeht.
Die Lebenserwartung ebenso wie das therapeutische Standard-Armamentarium haben sich über die letzten Jahrzehnte kaum verändert. Nach einem initialen Ansprechen auf Chemotherapie und Radiatio kommt es sehr rasch zu einer Resistenzentwicklung und Tumorprogression mit aggressivem Wachstum und rascher Metastasierung. Die Erfolge mit den derzeit verfügbaren Standard-Therapieschemata sind bescheiden und frustran (das mediane Überleben bei fortgeschrittener Erkrankung liegt bei < 10 Monaten, die 5-Jahres-Überlebensrate bei 1–5 %)1, Hoffnungen richten sich daher auf neue Therapien.
Fortschritte im Verständnis der Tumorbiologie von SCLC haben zur Identifizierung einer Reihe potenzieller Targets geführt. Die Forschungen konzentrieren sich einerseits auf den immunmodulatorischen Ansatz und auf die Evaluierung möglicher, für den Erfolg von Immuntherapien prädiktiver Biomarker, andererseits auf zielgerichtete Tumortherapien und damit die Identifizierung tumorspezifischer Oberflächenrezeptoren als Targets und prädiktive Biomarker für den Einsatz dieser Therapien.
Etliche experimentelle Therapien werden derzeit in Studien untersucht – und damit korrelierend verschiedenste Biomarker hinsichtlich ihrer Prädiktionsgenauigkeit evaluiert.
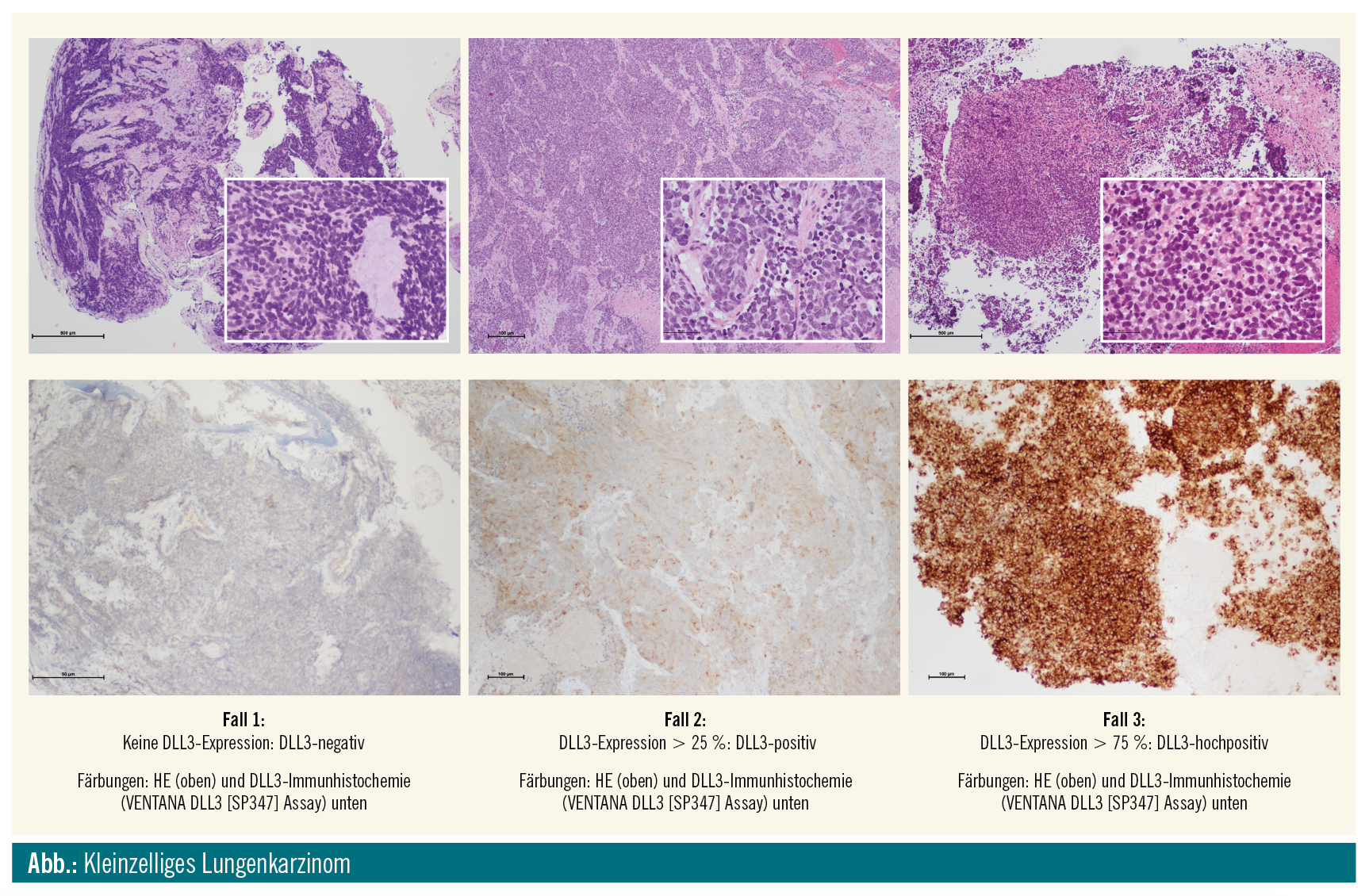
In klinischen Studien hat sich Rova-T (Rovalpituzumab-Tesirin), ein DLL3-zielgerichtetes Antikörper-Konjugat, als vielversprechender Therapieansatz erwiesen.2, 3 DLL3 (Delta-like protein 3) ist ein Inhibitor der Notch-Rezeptor-Aktivierung, dem in der neuroendokrinen Tumorgenese Bedeutung zukommt.4 In SCLC-Zellen wird DLL3 im Vergleich zu Normalgewebe signifikant auf der Zelloberfläche überexprimiert.5
Mit dem Antikörper-Konjugat Rovalpituzumab-Tesirin wird diese DLL3-Oberflächenexpression genutzt, um die Substanz zielgerichtet an und in weiterer Folge in die Zelle zu bringen, wo das Chemotherapeutikum freigesetzt wird und seine Wirkung entfalten kann.5 In seinem Kommentar bezeichnet Scott Dylla die neue Therapie daher auch als DLL3-gerichtetes „Trojanisches Pferd“.6
Die Therapie kann in Zentren, darunter auch am Otto-Wagner-Spital in Wien, im Rahmen eines Named-patient-use-Programms – nach DLL3-Biomarker-Bestimmung – bereits zur Anwendung kommen. Alle histopathologischen Untersuchungen erfolgen im Wilhelminenspital.
Spectrum Pathologie sprach mit Dr. Dagmar Krenbek, Pathologie Wilhelminenspital Wien, über den Stellenwert von Biomarkern beim SCLC.