[ECNP 2012] „Personalisierte Therapie“ – das neue Zauberwort in der Psychiatrie
Auch in der Psychiatrie spricht man immer häufiger von der „personalisierten Therapie“. Dies geschieht nicht zuletzt vor dem Hintergrund, dass die amerikanischen und europäischen Zulassungsbehörden FDA und EMA angekündigt haben, dass die Zulassung neuer Medikamente bald nur noch in Verbindung mit entsprechenden Gentests oder Biomarkern erfolgen soll. Dieses Modell, das erfolgreich bereits in der Onkologie praktiziert wird, soll künftig auch in anderen Indikationen gewährleisten, dass nur noch diejenigen Patienten mit neuen Substanzen behandelt werden, die auch wirklich davon profitieren.
Nosologie psychischer Störungen auf dem Prüfstand: Die Genforschung bietet hierzu zwar noch keine in der Praxis unmittelbar umsetzbaren Erkenntnisse, doch sie verändert die Diagnostik schon jetzt, indem sie wichtige Erkenntnisse zur Nosologie psychischer Störungsbilder liefert, so Prof. Alessandro Serretti, Bologna1. Dies ist umso wichtiger, als sich mit dem DSM V und dem ICD 11 die beiden wichtigsten Diagnosemanuale in einer Überarbeitung befinden. Auch für Prof. Alexander Nikulescu, Indianapolis, ist abzusehen, dass diese Erkenntnisse die bisher vorwiegend klinisch definierte psychiatrische Nosologie infrage stellen werden. Dies gilt vor allem für bipolare und schizophreniforme Störungen, Depressionen, Angststörungen und Alkoholabhängigkeit2. Auf dem ECNP 2011 wurden dazu einige interessante Studien mit Preisen ausgezeichnet.
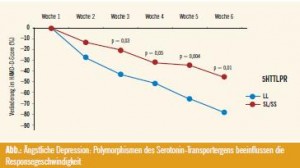
Eine Subgruppe, die davon auch therapeutisch profitieren könnte, sind Patienten mit einer ängstlichen Depression. Kandidatengene für diese schwerer behandelbare Population sind Polymorphismen des Serotonin-Transporters 5-HTT, die auch auf eine generell erhöhte Vulnerabilität für Depressionen hinweisen. Träger des S-Allels von 5-HTT zeigen einen deutlich langsameren Abfall der Depressionsscores als Träger des L-Allels (Abb.). 5-HTT-Mutationen sind damit nicht nur ein Genmarker für ein erhöhtes Risiko einer Depression, sondern auch für die Therapieresponse. Weitere prädiktive und therapeutische neue Ansatzpunkte sind der Cannabinoid-Rezeptor 1, die glutamaterge Transmission sowie das Neuropeptid γ 3, 4.
Auch bei der therapieresistenten Major Depression spielen 5-HTT-Polymorphismen offenbar eine wichtige Rolle5. S/SHomozygoten besitzen eine geringere Dicke im linken oberen temporalen Gyrus und ein geringeres Hippocampus- Volumen. Eine internationale Arbeitsgruppe lieferte neue Belege für die Hypothese, dass therapieresistente depressive Patienten offenbar eine Subgruppe mit unterschiedlichem neurobiologischem Profil sind6. Diese Patienten zeigen einen extremen Hyperkortisolismus und sprechen auch nicht mehr auf die Gabe von Antagonisten der Mineralkortikoid-Rezeptoren wie Spironolacton an. Offenbar, so die Folgerung, liegt bei dieser Subgruppe eine Dysfunktion der Mineralkortikoid-Rezeptoren vor.
Wie das EKT funktioniert: Die zugrunde liegenden neurobiologischen Mechanismen für die Wirkung der Elektrokrampftherapie (EKT) sind noch weitgehend ungeklärt. Eine Arbeitsgruppe der Universität Wien untersuchte jetzt erstmals die Rolle der serotonergen Transmission beim EKT in vivo und wurde für ihre Arbeit mit einem ECNP-Poster- und -Reisepreis ausgezeichnet7. Bei 10 Patienten mit einer schweren Major Depression wurden mittels PET-Scans das serotonerge Rezeptorbindungspotential in mehreren Hirnregionen (vorderes Cingulum, subgenualer Teil des Cingulums und orbitofrontaler Kortex) vor und nach EKT bestimmt. Die Autoren fanden in diesen Regionen eine signifikante Reduktion der Bindungsaffinität der 5-HT1A-Rezeptoren, die dort emotionale und kognitive Prozesse kontrollieren.
Forscher am Max-Planck-Institut für Psychiatrie in München haben einige Biomarker-Kandidaten für die Entwicklung einer postpartalen Depression identifiziert8. Die Forscher verglichen die peripartalen DNA-Transkriptionsprofile von 15 Frauen mit einer Postpartum-Depression, 21 gesunden Frauen und 10 Frauen, die vor und nach der Schwangerschaft unter einer Depression litten. In insgesamt 26 Transkriptionsprofilen fanden sich signifikante Erhöhungen von Bindungsstellen für Steroid-Hormone. Der Vergleich dieser Profile im 3. Trimester bei Frauen mit/ ohne Postpartum-Depression erlaubt, so die Autoren, eine Vorhersage einer Postpartum- Depression mit einer hohen Vorhersagegenauigkeit (Sensitivität: 88 %, Spezifität: 93,3 %). Die Studie wurde mit einem ECNP-Fellowship-Preis ausgezeichnet.
Cordance-EEG als Depressions-Biomarker: Ebenfalls vom Max-Planck-Institut für Psychiatrie in München stammt eine weitere preiswürdige Studie (ECNP-Fellowship- Preis), die sich mit Schlafparametern als Biomarker depressiver Erkrankungen beschäftigte9. Schlafstörungen sind zugleich Risikofaktor und Symptom depressiver Episoden. Das Schlaf-EEG zeigt charakteristische Veränderungen des objektiven Schlafs depressiver Patienten, beispielsweise eine gestörte Schlafkontinuität. Cordance ist ein quantitativer EEG-Parameter, der Informationen über absolute und relative Intensität von EEG-Spektren kombiniert und mit der regionalen Hirndurchblutung korreliert. Bisher wurde Cordance im Wachzustand zur Prädiktion des Ansprechens auf eine Psychopharmakatherapie genutzt.
In jüngster Zeit wird die Eignung von Cordance im Schlaf als Biomarker geprüft. In der Studie wurden die Schlaf- EEG von 20 stationär behandelten depressiven Patienten und 7 gesunden Kontrollen verglichen. Die Auswertung zur Cordance des Schlaf-EEG zeigte eine signifikant erhöhte präfrontale Cordance bei Respondern auf eine Pharmakotherapie im Vergleich zu Nonrespondern auf eine vom Arzt bestimmte antidepressive Therapie (p = 0,0055). Die Z-Scores korrelierten ebenfalls signifikant mit dem HAM-D-Score (p < 0,01). Auffällig war, dass Responder und Nonresponder keine signifikanten Unterschiede hinsichtlich der Einschlaf-Latenz sowie anderen wichtigen Schlafparametern einschließlich REM-Dichte aufwiesen. Die Kontrollpersonen hatten Z-Scores, die mit den Respondern übereinstimmten, nicht aber mit den Nonrespondern.
Retinadicke als Schizophrenie-Marker? Bei Patienten mit einer Multiplen Sklerose wird die Messung der paramakulären Retinadicke als Verlaufsmarker diskutiert. Die Ergebnisse einer Pilotstudie einer Arbeitsgruppe aus Saragossa deuten darauf hin, dass dieser Parameter möglicherweise auch bei schizophrenen Patienten Hinweise auf den Krankheitsverlauf sowie den axonalen Untergang geben könnte10. Der Vergleich von jeweils 10 schizophrenen und gesunden Patienten ergab eine signifikante negative Korrelation zwischen der Retinadicke und der Krankheitsdauer und dem Alter der Patienten. Keine Korrelation fand sich zwischen der Retinadicke und der Psychopathologie, gemessen mit dem PANSS. Die Retinadicke könnte nach Ansicht der Autoren ein Marker für die krankheitsbedingten Hirnanomalien und axonalen Schädigungen sein.
Ansätze für prokognitive Therapien: Ein wichtiges Forschungsfeld ist auch die Therapie kognitiver Defizite neuropsychiatrischer Erkrankungen. Eine deutsche Arbeitsgruppe stellte präklinische Daten zu dem Phosphodiesterase-2A-Hemmer BCR909 vor, dem prokognitive Effekte zugeschrieben werden11. Tierexperimentelle Studien zeigen unter der Gabe von BCR909 einen dosisabhängigen Anstieg von cGMP. cGMP ist ein Nukleotid und ein chemischer Botenstoff, der als second messenger in viele Signalkaskaden von Stoffwechsel und Hormonwirkung eingeschaltet ist. Dieser Effekt entspricht demjenigen des Acetylcholinesterasehemmers Donezepil.
flaute in der psychopharmakaforschungNeue Techniken in der Molekulargenetik und neue sensitive bildgebende Verfahren in der (prä-)klinischen Forschung sowie der verstärkte Einsatz biotechnologischer Methoden in der Arzneimittelentwicklung haben zu einem exponential wachsenden Erkenntnisgewinn geführt. Dies kontrastiert erheblich mit der gegenwärtigen Flaute in der Entwicklung von neuartigen Psychopharmaka, beklagte Prof. Guy Goodwin, Oxford. Goodwin ist zusammen mit Prof. David Nutt, London, Autor eines ECNP-Summit-Reports zur Zukunft der europäischen ZNS-Arzneimittelforschung, der eine alarmierende Entwicklung voraussagt12. Viele große Firmen mit einer hohen Expertise in der Neuropsychiatrie ziehen sich aus der Forschung zurück. Die Hoffnung, dass kleinere Biotech-Unternehmen diese Lücke füllen, wird sich nicht erfüllen, so der Report. Denn die Risiken angesichts des benötigten Kapitals sind zu hoch. Was von den Autoren nicht explizit gesagt wurde, wohl aber so gemeint ist: Die Psychopharmakotherapie wird sich mittelfristig mit den etablierten Substanzen zufrieden geben müssen, Kandidaten für innovative Medikamente sind rar.
Quelle: 24. Jahrestagung des European College of Neuropsychopharmacology (ECNP), 3.–7. 9. 2011, Paris
1 Serretti A, Abstract Nr. E.02.02
2 Niculesco A, Abstract Nr. S.15.01
3 Larsen G et al., Abstract Nr. C.01.01
4 Sa HP et al., Abstract Nr. P.1.e.019
5 Philips JL et al., Abstract Nr. P.1.e023
6 Juruena et al., Abstract Nr. P.2.c.030
7 Baldinger P et al., Abstract Nr. P.1.e.022
8 Mehta D et al., Abstract Nr. P.1.a.010
9 Pawlowski M et al., Abstract Nr. P.2.a.012
10 Sanz P et al., Abstract Nr. P.1.f.001
11 Langen B et al., Abstract Nr. P.1.g.012
12 ECNP Summit Report Europ Neurpsychopharmacol 2011; 21:495-9