Analgetika – Wechselwirkungspotenzial in der Multimedikation
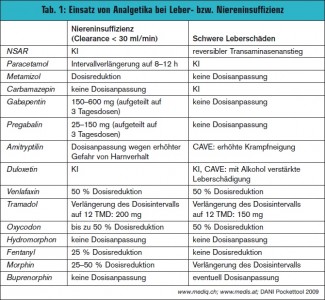
Beim Einsatz von Analgetika sollte immer die Nieren- bzw. Leberfunktion berücksichtigt werden, da sich die einzelnen Wirk – stoffe wesentlich hinsichtlich Metabolismus und Ausscheidung voneinander unterscheiden (Tab. 1).
NSAR: Noch immer ist die Gruppe der NSAR die am meist verordnete Indikationsgruppe zur Schmerztherapie. Der sicherlich einzigartigen entzündungshemmenden Wirkung stehen viele unerwünschte Arzneimittelwirkungen (UAW) wie akute Niereninsuffizienz, Verschlechterung der Herzinsuffizienz, verminderte Blutdrucksenkung, erhöhtes Blutungsrisiko im Gastrointestinaltrakt, Kolitis vor allem in Kombination mit vielen anderen Medikamenten, gegenüber. Sie führen die Liste derer Medikamente an, die durch UAW zu stationären Aufenthalten führen. Das Agency for Health Quality Research AHQR veröffentlichte 2009 einen Bericht über 16.500 Todesfälle bedingt durch NSAR-Gas – trointestinalblutungen in den USA.
Ein spanisch-italienisches Team unter Gonzales führte eine systematische Analyse von Beobachtungsstudien der Jahre 2000 bis 2008 zur Therapie mit nicht-steroidalen Antirheumatika (NSAID) mit in der Praxis üblichen Dosierungen durch. Dabei wurde überprüft, wie hoch die Wahrscheinlichkeit von Blutungen und Perforationen im oberen Gastrointestinaltrakt unter verschiedenen Substanzen war. Das relative Risiko für eine Blutung bzw. Perforation im oberen Gastrointestinaltrakt betrug 4,50 für traditionelle NSAID und 1,88 für Coxibe. Für Ibuprofen (2,69), Rofecoxib (2,12), Aceclofenac (1,44) und Celecoxib (1,42) lag das Risiko unter dem für alle NSAID errechneten Durchschnitt; für Ketorolac (14,54), Piroxicam (9,94), Naproxen (5,63), Ketoprofen (5,57), Indomethacin (5,40), Meloxicam (4,15) und Diclofenac (3,98) lag es dagegen über dem Durchschnitt. Der Grad der COX-1-Inhibition eignet sich offenbar nicht als Risikomesser, wohl aber eine über 80%ige Inhibition beider Isoenzyme. Eine weitere Korrelation ließ sich ausmachen: NSAID mit einer langen Halbwertszeit und einer langsamen Freisetzungskinetik gehen offenbar mit einem erhöhten Risiko für Komplikationen im oberen Gastrointestinaltrakt einher.
Zahlreiche internationale Kohortenstudien zeigen eine thrombozytenaggregationshemmende Wirkung bei SSRI, aber auch bei Venlafaxin, verursacht durch eine Hemmung der Wiederaufnahme von Serotonin in die Thrombozyten. Durch Kombinationen mit NSAR oder anderen Thrombozytenaggregationshemmern steigt das Risiko für GI-Blutungen massiv an: Da Abajo gibt bei einer Kombination mit NSAR eine Odds-Ratio von 4,8 an (2,8–8,3). Die Number Needed to Harm beträgt dann 250. Die Odds-Ratio steigt auf 9,1 (4,8 bis 17,3), wenn die Patienten zur Prophylaxe von Blutungen keinen Magensäureblocker einnahmen. Ob es Unterschiede in der Gruppe der SSRI gibt, ist noch nicht eindeutig geklärt. Es gibt Hinweise, dass auch der Effekt an den Thrombozyten umso ausgeprägter ist, je höher die Affinität zu Serotoninrezeptoren ist (Escitalopram, Citalopram, Sertralin). Bei Kombinationen von NSAR mit SSRI, sollte man immer auf ein bis zu 15-fach erhöhtes Blutungsrisiko achten. Die Ergebnisse einer im Mai 2011 erschienen Kohortenstudie aus Dänemark (83.677 Patienten mit Myokardinfarkt) weisen auf die hohe Wahrscheinlichkeit einer erhöhten Rate an Reinfarkt bzw. erhöhte Mortalität nach der Gabe von NSAR hin. Dabei schneidet Diclofenac am schlechtesten ab. Bereits in der ersten Woche der Gabe therapeutischer Dosen war das Risiko um das fast 5fache erhöht. Nur Naproxen scheint eine höhere kardiovaskuläre Sicherheit zu haben. Die Autoren kamen zu dem Schluss, dass bei kardiovaskulären Schäden auf den Einsatz von NSAR möglichst verzichtet werden sollte (Schjerning Olsen et al., Circulation 2011).
Weitere pharmakodynamische Interaktionen von NSAR mit:
- ACE-Hemmern: Gefahr des akuten Nierenversagens, verminderte Blutdrucksenkung, Hyperkaliämie
- Antidepressiva, Diuretika, Antikonvulsiva: Hyponatriämie über SIADH-Syndrom
- Chinolonen: erhöhte Neurotoxizität
- Diuretika: Wirkverlust und Ödeme
- Sulfonylharnstoffen: erhöhte Hypoglykämiegefahr
Weitere pharmakokinetische Interaktionen von NSAR:
- Mit MTX (Methotrexat) und Lithium: Kumulationsgefahr und Intoxikation wegen Hemmung der Ausscheidung
- CAVE akute Leberschädigung mit reversiblemTransaminasenanstieg ist möglich (auch bei therapeutischen Dosen von Diclofenac beschrieben, besonders bei i. v. Gabe).
Laut WHO-Stufenplan wären Paracetamol und Metamizol als mögliche Alternative zu NSAR zu sehen (wenn nicht eine antiphlogistische Wirkung notwendig ist). Wie sieht das Sicherheitsprofil in der Multimedikation aus?
Kasuistik Paracetamol
Ein 68-jähriger Patient mit Kolonkarzinom und seit Monaten stabilen, ausgedehnten Lebermetastasen klagt über leichte Oberbauchschmerzen.
Mit 4 x 500 mg Paracetamol wird eine gute Schmerzkontrolle erreicht. Innerhalb einer Woche wird er verwirrt, dann komatös und er stirbt. Bei der Autopsie ist kein Leberparenchym zu finden.
Paracetamol erfährt einen komplexen hepatischen Metabolismus. Etwa 98 % werden konjugiert, während im Normalfall nur ein geringer Anteil durch Cytochrom-P450-Enzyme zum hochreaktiven N-acetyl-Benzochinonimin hydroxyliert wird. Dieser Metabolit reagiert mit Glutathion und verliert dadurch seine Toxizität. Irreversible Leberzellnekrose tritt dann auf, wenn mehr von dem Metaboliten gebildet wird als vom vorhandenen Glutathion aufgefangen werden kann (in Dosen ab 6–8 g/Tag). Das ist dann der Fall, wenn das Leberparenchym geschädigt (z. B. bei Leberzirrhose, Fettleber) oder reduziert ist (z. B. durch ausgedehnte Lebermetastasen) und weniger Glutathion zur Verfügung steht. Aber auch dann, wenn eine Enzyminduktion (z. B. durch Phenytoin, Carbamazepin, Alkohol, Rifampicin) den Anteil des hydroxylierten Paracetamols erhöht. Hinsichtlich anderer Organschädigungen schneidet Paracetamol aber wesentlich besser als NSAR ab.
Metamizol: Der Einsatz dieses ausgezeichnet spasmolytisch wirksamen Analgetikums wird noch immer aufgrund eines vor allem in Schweden beschriebenen erhöhtem Agranulozytoserisikos (1:1.439) und der relativen Gefahr eines Widerstandsverlustschocks, sehr kritisch beurteilt. Um die Gefahr eines Schocks zu reduzieren, sollte nicht mehr als 1 ml beziehungsweise 0,5 g Wirkstoff pro Minute am liegenden Patienten injiziert werden. Schwere Hypotonie stellt eine Kontraindikation für die parenterale Verabreichung dar.
Neben dem Differenzialblutbild (Leukozytenzahl < 2.000/mm3; Granulozytenzahl < 500 bis 0/mm3) weisen Symptome wie Angina tonsillaris, Schüttelfrost und kontinuierliches Fieber sowie multiple Schleimhautnekrosen, die auf die geschwächte Immunabwehr zurückzuführen sind, auf eine Agranulozytose hin. Der Zusammenhang zwischen Schmerzmitteleinnahme und Agranulozytose wurde in der IAAAS-Studie (International Agranulocytosis and Aplastic Anaemia Study) von 1981 bis 1984 in Spanien, Bulgarien, Israel, Ungarn, Deutschland, Schweden und Italien an insgesamt 22,3 Millionen Menschen untersucht, die in der Woche vor Eintreten der Blutbildstörung Analgetika eingenommen hatten. Im Fall der Gabe von Metamizol wurde eine Inzidenz von 1,1 Agranulozytose-Erkrankungen pro Million exponierter Personen pro Behandlungswoche festgestellt.
In Barcelona, wo die Studie bis Juni 2001 fortgesetzt wurde, betrug die Inzidenz an Agranulozytose-Erkrankungen durch Metamizol 0,56 Fälle pro Million Einwohner pro Jahr. Eine prospektive polnische Studie von Juli 2002 bis Juli 2003 an 15 Millionen Menschen ermittelte nur 16 Agranulozytose-Fälle, die alle nicht auf eine Metamizol-Einnahme zurückzuführen waren. Metamizol darf bei Patienten mit bekannter Störung der Knochenmarkfunktion oder Erkrankungen des hämatopoetischen Systems nicht angewendet werden. Aufgrund der Hämolysegefahr ist es auch bei Glukose-6-Phosphat-Dehydrogenase- Mangel kontraindiziert.
Mögliche Interaktionen bei Metamizol: mit Cyclosporin sollten die Spiegel überprüft werden. Vorsicht mit Antihypertensiva: Hypotoniegefahr (v. a. bei zu rascher i. v. Gabe). Im Gesamtvergleich nicht-opioider Analgetika kam eine Metaanalyse, die epidemiologische Studien aus den Jahren 1970 bis 1995 auswertete, zum Ergebnis, dass das absolute Mortalitätsrisiko unter Metamizol und Paracetamol mit 25 von 100 Millionen Behandelten gleich gering und in beiden Fällen deutlich niedriger als das von Acetylsalicylsäure (185 von 100 Millionen) und Diclofenac (592 von 100 Millionen) ist.
Tramadol: Laut internationalen Guidelines verschiedener Schmerzgesellschaften wird bei chronischer Schmerztherapie oft die WHOStufe II übersprungen und relativ rasch der Einsatz von Opiaten dem Tramadol vorgezogen, meist aufgrund besserer Verträglichkeit. Der Teil des Tramadols, der an den zentralen μ-Rezeptoren angreift, um analgetisch zu wirken, muss nach Resorption durch das CYP-2D6-System in der Leber aktiviert werden. Bei Poor-Metabolizern bzw. bei der gleichzeitigen Verabreichung von CYP2D6 – Inhibitoren (z. B. Paroxetin, Risperidon etc.) kann diese Aktivierung vermindert sein. Zusätzlich wirkt Tramadol (ohne Aktivierung) auch über eine Erhöhung von Serotonin und Noradrenalin analgetisch. Dabei dürfte vor allem die Erhöhung von Serotonin für die sehr häufigen gastrointestinalen Nebenwirkungen wie Übelkeit und Erbrechen verantwortlich sein. In Kombination mit anderen serotonergen Substanzen ist immer auf das Auftreten eines Serotoninsyndroms zu ach – ten, gekennzeichnet durch Akathisie, Unruhe, Erbrechen, Tremor und Schwitzen etc.) (Tab. 2). Tramadol senkt die Krampfschwelle, was vor allem in Kombination mit Theophyllin, Antipsychotika, Bupropion und Alkohol zu Anfällen führen kann.
Opiate: Die am meisten eingesetzten Vertreter Morphin, Hydromorphon, Oxycodon, Fentanyl und Buprenorphin unterscheiden sich hinsichtlich ihres Metabolismus und ihrer Ausscheidung (Tab. 1). Bei Niereninsuffizienz müssen Hydromorphon und Buprenorphin nicht in der Dosis angepasst werden.
Vor allem beim Einsatz von Fentanylpflaster und Oxycodon sollte eine gleichzeitige Einnahme anderer anticholinerg wirksamer Medikamente vermieden werden, um kognitive Verschlechterung bis hin zum Delir vor allem beim alten Patienten zu verhindern. Es sind in der Literatur auch Einzelfälle eines Serotoninsyndroms in Kombination mit anderen serotonergen Substanzen, vor allem Antidepressiva beschrieben.
Bei allen Opiaten, vor allem bei i. v. Gabe, sollte auf eine Potenzierung der Gefahr der Atemdepression durch die gleichzeitige parenterale Gabe von Benzodiazepinen und Neuroleptika geachtet werden.
Andere Analgetika: Unter Carbamazepin kann es zu kognitiven Verschlechterungen, Leberschäden und einer starken Sedierung kommen, es ist auch ein sehr starker CYP-3A4-Induktor.
Gabapentin und Pregabalin erfordern im Fall bereits bestehender Nierenschädigungen unbedingt Dosisanpassungen, da sonst das Risiko schwerer ZNS-Nebenwirkungen (Schwindel, „Dizziness“) besteht.
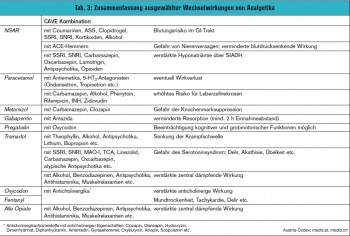
ZUSAMMENFASSUNG: Bei Interaktionen handelt es sich immer nur um Wahrscheinlichkeiten, deren Evidenz sich aus klinischen Erfahrungen und retrospektiven Kohortenstudien ergeben. Es sollte immer im individuellen Patientenfall Nutzen und Risiko einer möglichen Kombination bewertet werden. Zur Abschätzung der zu erwartenden klinischen Relevanz einer Wechselwirkung stehen internationale und nationale Guidelines der Schmerzgesellschaften bzw. Interaktionsprogramme – wie z. B. medis.at, mediq.ch – als Hilfestellung zur Verfügung. Ideal wäre ein Arzneimittelinformationszentrum, wo man im Einzelfall rasch und kompetent Auskunft bekommen könnte (ausgewählte Wechselwirkungen von Analgetika Tab. 3).
Literatur bei der Verfasserin