Antibiotikatherapie beim Patienten mit anaphylaktischen Reaktionen auf Penicilline
Allergische Reaktionen sind die häufigsten unerwünschten Antibiotikawirkungen, wobei die anaphylaktischen Reaktionen potenziell lebensbedrohlich sind. Dabei sind Penicilline wiederum die häufigste Ursache von anaphylaktischen Reaktionen auf Antiinfektiva – geschätzt bei 0,05 % der Verordnungen. Anaphylaktisch werden solche Reaktionen bezeichnet, die IgE-mediiert sind, als anaphylaktoid bezeichnet man dieselben Zustandsbilder, jedoch ohne IgE-Beteiligung.
Hinweise auf Anaphylaxie ergeben sich bereits aus der Anamnese (Tab. 1) und sollten in jedem Fall durch einen Facharzt auf dem Gebiet der Immunologie/Allergologie abgeklärt werden.
In-vitro- und In-vivo-Tests zur Abklärung von IgE-mediierten Reaktionen auf Antibiotika stehen zwar für manche Betalaktame, aber nicht für alle Antibiotika zur Verfügung. Umso wichtige ist daher die Anamneseerhebung, auch in Hinblick auf nicht IgE-mediierte anaphylaktoide Reaktionen, die ja trotzdem dieselben klinischen Konsequenzen haben können.
Das Management der anaphylaktischen Antibiotikareaktion unterscheidet sich nicht von dem der Reaktionen auf andere Substanzen wie Insektengifte oder Lebensmittel und soll hier nicht abgehandelt werden. Die immer wieder gestellte Frage, ob Antibiotika mit besonders langer Halbwertszeit (z. B. Azithromycin 2–4 Tage, Teicoplanin 3–7 Tage) in Hinblick auf Häufigkeit, Schweregrad oder Dauer allergischer Reaktionen nicht besonders gefährlich sind, kann verneint werden; die aus den klinischen Studien bekannten Sicherheitsdaten der in Frage kommenden Substanzen lassen diesen Schluss nicht zu.
Kreuzreaktivität: Ist anamnestisch mit und ohne Austestung das Vorliegen einer Anaphylaxie auf Penicillin anzunehmen, stellt sich in erster Linie die Frage nach therapeutischen Alternativen für die Therapie von Infektionskrankheiten. Zwischen Penicillinen und Cephalosporinen wie auch Carbapenemen ist von einer Kreuzreaktivität auszugehen. Interessanterweise gibt es bis heute keine eindeutigen Angaben, wie häufig derartige Kreuzreaktionen mit Cephalosporinen sind, man sollte von 2–5 % der Patienten ausgehen. Kasuistiken über Todesfälle bei Patienten mit Penicillinallergie, denen man Cephalosporine verabreicht hat, sind publiziert; einschränkend muss man aber festhalten, dass diese Patienten nicht mittels Hauttest ausgetestet wurden, und für die historischen Berichte gilt, dass Cephalosporine früher sehr wohl mit Penicillin verunreinigt waren.
Hauttests mit verschiedenen Penicillinen und deren Metaboliten haben einen negativen Prädiktivwert von 97–99 %, die positive Vorhersagekraft liegt bei nur 50 %. In einem Review über Cephalosporine bei Penicillinallergie wurden folgende Häufigkeiten von Cephalosporinreaktionen bei Patienten mit Penicillinallergie erwähnt: Patienten mit positivem Hauttest 4,4 %, Patienten mit negativem Hauttest 0,6 % und Patienten ohne Hauttest 11,8 %. Demgegenüber wird das Risiko anaphylaktischer Reaktionen auf Cephalosporine bei Patienten ohne Penicillinallergie mit 0,02 % angegeben. Zu bedenken ist dabei auch, dass die Hauttests keine Aussage über anaphylaktoide Reaktionen erlauben. Nach anamnestisch schwer verlaufenen anaphylaktischen Reaktionen wird man daher von der weiteren Gabe von Betalaktamen Abstand nehmen müssen. Noch dazu, da in der Praxis praktisch nie die Befunde einer Austestung verfügbar sind und diese Patienten dann doch deutlich häufiger reagieren.
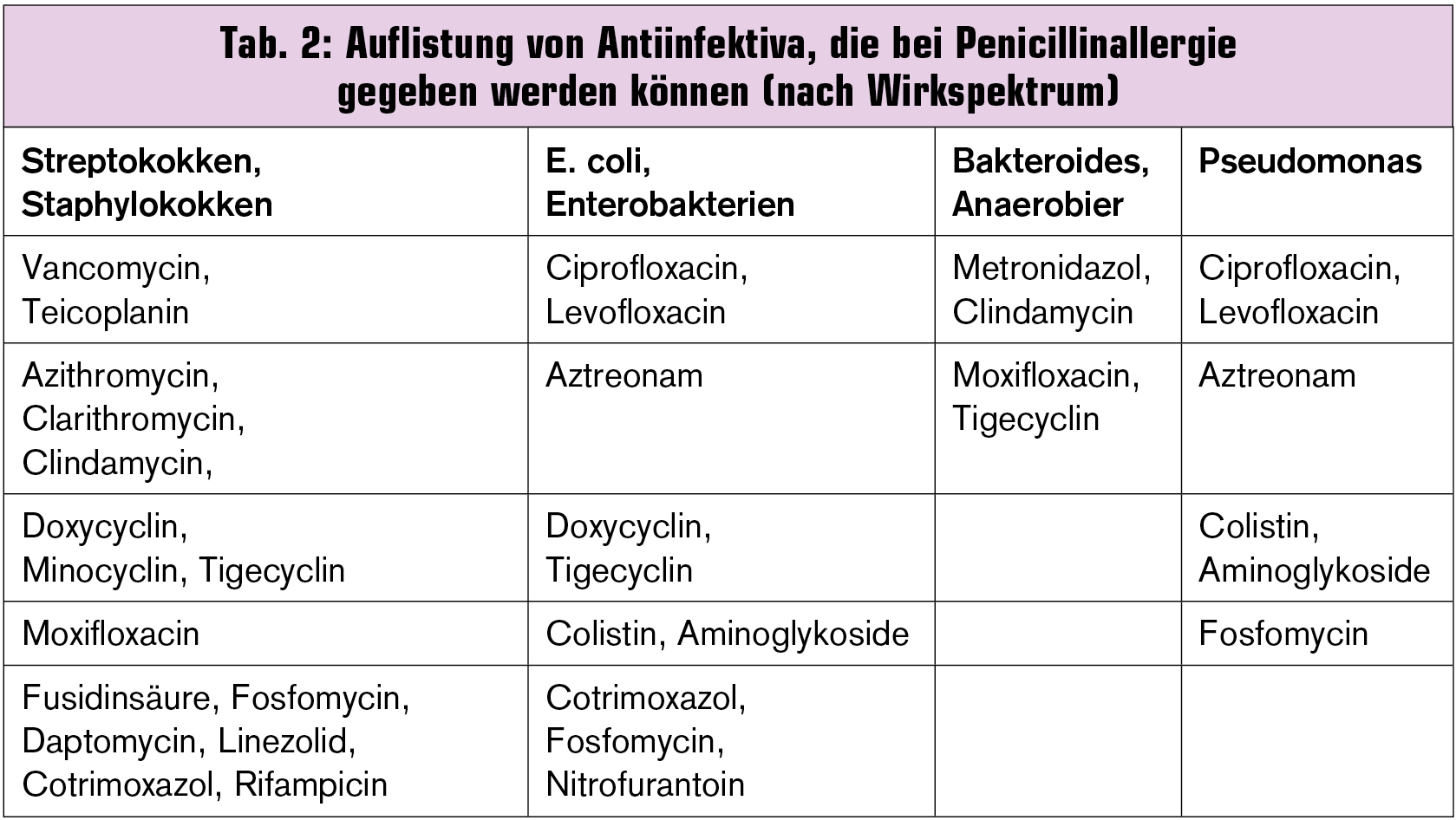
Therapeutische Alternativen: Welche „Nicht-Laktame“ kann man einem derartigen Patienten verordnen? Tab. 2 listet die Optionen geordnet nach Erregerart auf. Alle angeführten Substanzen mit Ausnahme von Aztreonam sind chemisch nicht mit Betalaktamen verwandt, daher sind keine Kreuzreaktionen zu erwarten. Unabhängig von Kreuzreaktion auf Basis einer chemische Verwandtschaft besteht natürlich immer die Möglichkeit, auch auf das „nicht verwandte“ Medikament zu reagieren, analog zur Möglichkeit, neben einer Allergie gegen Penicillin auch eine gegen Erdnüsse oder Katzenhaare zu haben.
Sonderstellung für Aztreonam: Aztreonam ist ein Monobaktam und verfügt nur über den Laktamring – nicht aber über den zweiten, penicillin- respektive cephalosporin- oder carbapenemtypischen Ring, also der für die Allergie relevanten Struktur – und ist daher das einzige Laktam, von dem keine chemischen Kreuzreaktionen bei Allergie auf Penicilline oder Cephalosporine zu erwarten sind. Das Wirkspektrum von Aztreonam ist auf gramnegative Erreger beschränkt und umfasst neben den Enterobakterien auch Pseudomonas aeruginosa. Keine Aktivität besteht gegenüber Staphylokokken und anaeroben Erregern. Aztreonam ist ein Spitalsantibiotikum, eine orale Gabe ist nicht möglich.
Die Auswahl des Antibiotikums aus der oben angeführten Liste wird sich selbstverständlich an den typischen Erregern der diagnostizierten Infektion orientieren:
- Harntrakt – Quinolone, Cotrimoxazol, Nitrofurantoin, Fosfomycin
- Atemwege – Makrolide, Quinolone, Tetracycline
- Haut- und Weichteilinfektionen – Clindamycin, Fusidinsäure, Tetracycline
Ein aktuelles Problem ist die Zunahme von Resistenzen gegen Antiinfektiva bei gramnegativen Erregern, wie sie für den Harntrakt typisch sind; Resistenzen gegenüber Cotrimoxazol bei bis zu 30–40 % und gegenüber Quinolonen bei bis zu 20 % der E.-coli-Isolate bedeuten für den Patienten mit Penicillinanaphylaxie ein erhebliches Problem und als letzte Alternativen für die p. o. Therapie Nitrofurantoin oder Fosfomycin-Trometamol.
Option Desensibilisierung: Als letzten Ausweg – wenn die Gabe von Penicillinen zwingend wäre – wäre noch die Desensibilisierung zu nennen. Dosierungsschemata sind publiziert und die Durchführung wird unter entsprechenden Sicherheitsmaßnahmen erfolgen.
Zwei empfehlenswerte Überblicksarbeiten zum Thema
The Diagnosis and Management of Anaphylaxis: An Updated Practice Parameters
Lieberman P. et al.: The Diagnosis and Management of Anaphylaxis: An updated Practice Parameter. J Allergy Clin Immunol 2005; 115 (3):483-523
Antibiotic Allergy
Gruchalla R.S. et al.: Antibiotic Allergy.
N Engl J Med 2006; 354:601-9