Neue Daten zu Blutungserkrankungen
ASH 2020 | Beim diesjährigen Kongress der American Society of Hematology (ASH) gab es viele interessante Vorträge im Bereich der hereditären Blutgerinnungsstörungen. In diesem Beitrag wird nur eine Auswahl der bedeutsamsten Studien zu Blutungserkrankungen genauer beschrieben, und einige werden nur kurz erläutert.
Hämophilie auf genetischer Ebene
Hämophilie A (Faktor-VIII-Mangel) und B (Faktor-IX-Mangel) sind seltene X-chromosomale Blutgerinnungsstörungen, die zu starken spontanen Blutungen führen können. Die genetische Diagnostik der Hämophilie ist dabei auch von klinischer Bedeutung, insbesondere für die Familienplanung, die Risikostratifizierung zur Entstehung von Inhibitoren gegen Ersatzpräparate und die Abschätzung des Schweregrads der Erkrankung. Jill Johnsen et al. analysierten auf molekularbiologischer Ebene 11.341 PatientInnen (742 Frauen) mit Hämophilie A oder B aus der Initiative „My Life, Our Future“ (MLOF).1 Bei mehr als 98 % aller PatientInnen wurden klinisch relevante, genetische Varianten entdeckt. Insgesamt wurden 1.919 „unique variants“ beschrieben, von denen 744 neuartig waren. Bei schwerer Hämophilie A war die F8-Inversion am häufigsten vertreten (44,7 %), während bei Hämophilie B am häufigsten „missense“-Mutationen gefunden wurden. Die AutorInnen beschrieben auch, dass das Auftreten von Inhibitoren mit einer schweren Hämophilie assoziiert war und dass diese PatientInnen auf genetischer Ebene vor allem Deletionen und komplexe Inversionen im betroffenen Gen aufwiesen. Insgesamt war die Inzidenz neuer Varianten sehr hoch, weshalb die Sequenzierung der F8- und F9-Gene zum besseren Verständnis der Hämophilie auf genetischer Ebene weiterhin von großer Relevanz bleibt.
Gentherapie bei Hämophilie B
Die ersten Daten aus der Phase-III-Studie des „HOPE-B Gene Therapy Trial“ wurden in der Plenary Session des ASH 2020 präsentiert.2 Steven Pipe et al. untersuchten die Wirksamkeit und Sicherheit der Gentherapie basierend auf einem Adeno-assoziierten Virus-Serotyp-5-(AAV5-)Vektor, der ein für die Faktor-IX-Padua-Variante kodierendes Gen beinhaltet. In dieser Studie erhielten von 75 gescreenten männlichen Patienten 54 Patienten (44 mit schwerer und 10 mit moderater Hämophilie B) eine intravenöse Applikation von Etranacogene dezaparvovec (2 x 1013 gc/kg) und wurden über 26 Wochen lang beobachtet. Vor Therapiebeginn hatten 38 aller Patienten (mittleres Alter [Standardabweichung] 41,5 [15,8] Jahre) Blutungen, und 23 wiesen neutralisierende Antikörper gegen AAV5 auf. Nach der Therapie kam es zu einem mittleren Faktor-IX-Anstieg auf 37,2 %. Neutralisierende Antikörper gegen AAV5 hatten keinen Einfluss auf den Therapieerfolg. Ein Patient mit einem enorm hohen Titer an neutralisierenden Antikörpern hatte jedoch kein Ansprechen auf die Therapie. 96,3 % aller Patienten mussten keine Prophylaxe applizieren, und 72,2 % hatten in diesen 26 Wochen keine Blutungen, während die restlichen 15 Patienten insgesamt nur 21 Blutungsereignisse berichteten. Von den bei 37 Patienten beschriebenen Nebenwirkungen waren die meisten milder Natur (81,5 %). Es wurden keine schweren Nebenwirkungen oder Tod berichtet. Die Daten dieser weltweit größten Gentherapie-Studie legen eine effiziente und sichere Therapieoption für Patienten mit schwerer oder moderater Hämophilie B nahe, auch wenn sie neutralisierende Antikörper gegen AAV5 besitzen.
Immunthrombozytopenie
Immunthrombozytopenie (ITP) ist eine seltene Autoimmunerkrankung, die mit einem erhöhten Blutungsrisiko und Fatigue assoziiert ist. Die empfohlene First-Line-Therapie bei Neudiagnose sind hochdosierte Kortikosteroide, welche jedoch zu diversen Nebenwirkungen führen können. Außerdem ist das Ansprechen auf Kortikosteroide sehr heterogen und auch mit einer hohen Rate von Wiederauftreten der ITP verbunden; lediglich um 20 % aller PatientInnen verbleiben in kompletter Remission.
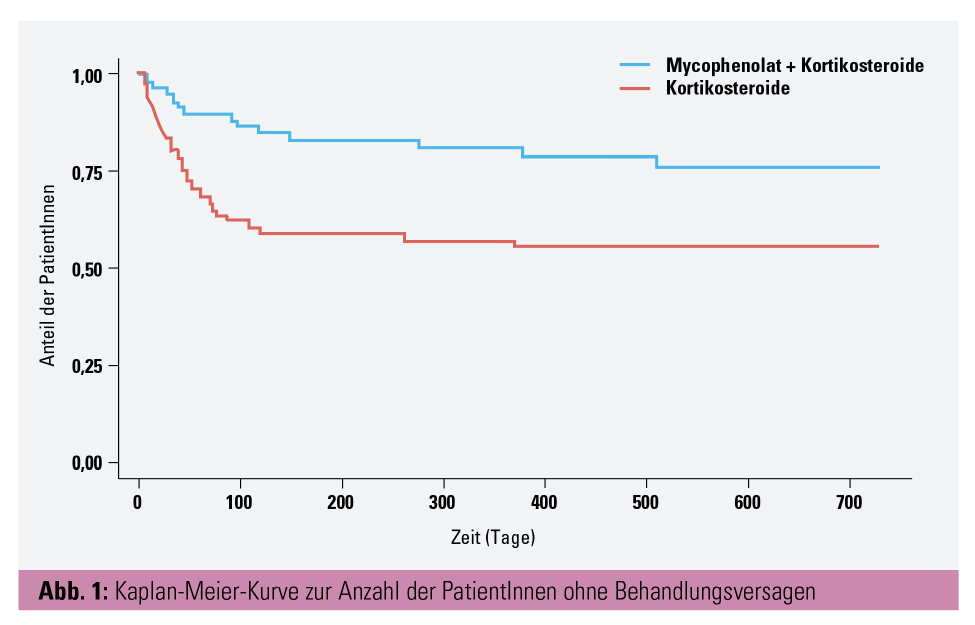
Im Rahmen der Late-Breaking Plenary Session wurden Ergebnisse aus dem FLIGHT Trial präsentiert, einer multizentrischen, randomisierten Studie zur Therapie von neudiagnostizierter ITP.3 Dabei untersuchen die AutorInnen rund um Charlotte Bradbury und Nichola Cooper das Ansprechen und die Verträglichkeit einer First-Line-Kombinationstherapie von Kortikosteroiden und Mycophenolat (MMF), das oft als Second-Line-Therapie verwendet wurde und retrospektiv eine hohe Wirksamkeit zeigte. Insgesamt wurden 120 ITP-PatientInnen (52,4 % Männer, mittleres Alter: 54 Jahre mit einer Range von 17–87) untersucht, die älter als 16 Jahre alt waren und bei denen eine ITP neudiagnostiziert wurde. Ausschlusskriterien waren unter anderem HIV, Schwangerschaft oder Stillen. Die mittlere Thrombozytenzahl betrug 7 x 109/l und der mittlere Beobachtungszeitraum 18 Monate. Die beiden Studienarme der PatientInnen unter Therapie mit Kortikosteroiden (n = 61) und jener, die Kortikosteroide und MMF (n = 59) erhielten, unterschieden sich nicht in ihren demografischen Eigenschaften. PatientInnen, die zusätzlich MMF erhielten, hatten signifikant weniger Therapieversagen (22 % vs. 44 %; Abb. 1). Das Nebenwirkungsspektrum war in beiden Gruppen ähnlich. Allerdings waren einige der Parameter zur Lebensqualität bei PatientInnen im Studienarm mit MMF-Therapie stärker beeinträchtigt.
Tranexamsäure bei thrombozytopenen hämatologischen PatientInnen
Ein weiteres Highlight war die Studie von Terry Gernsheimer et al. zur zusätzlichen Anwendung von Tranexamsäure bei thrombozytopenen PatientInnen unter hämatologischer Therapie, die Thrombozytenkonzentrate bekommen müssen (a-TREAT Trial).4 Die StudienautorInnen konnten zeigen, dass die Zugabe von Tranexamsäure zu keinem Nutzen bei Verhinderung von Blutungen (ab WHO-Grad II) führt (Odds Ratio [95%-KI]: 0,86 [0,52–1,38]; p = 0,74). Es wurde lediglich eine erhöhte Inzidenz von Okklusionen von zentral-venösen Kathetern im Studienarm mit Tranexamsäure beobachtet.
Blutgruppe 0 und Blutungsrisiko
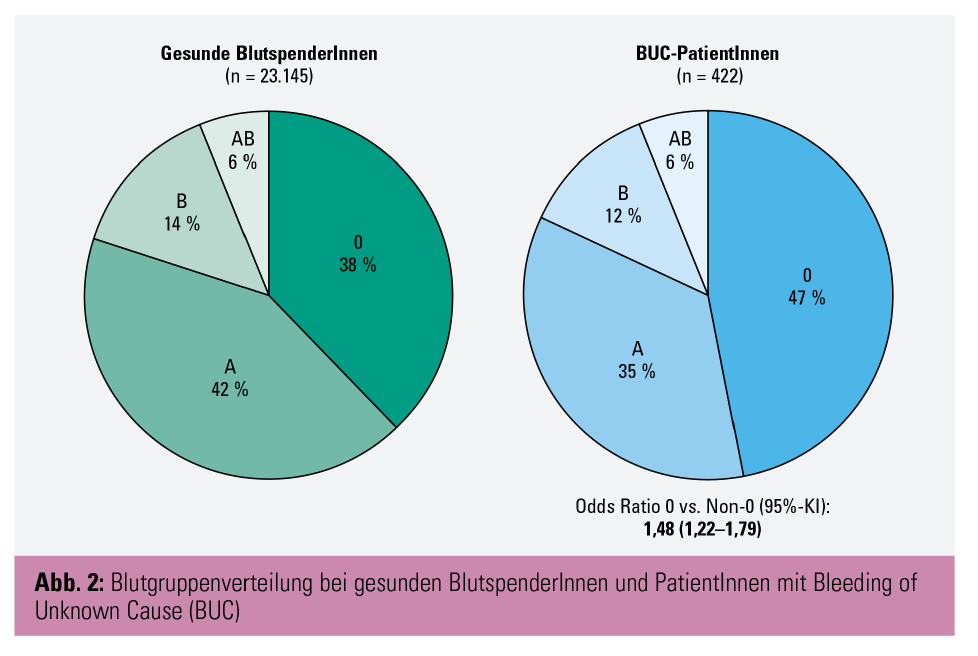
Ein Vortrag unserer Forschungsgruppe an der Abteilung für Hämatologie und Hämostaseologie der Medizinischen Universität Wien um Prof. Ingrid Pabinger beschäftigte sich mit dem Einfluss der AB0-Blutgruppe auf den Blutungsschweregrad bei PatientInnen mit Bleeding of Unknown Cause (BUC).5 Wir konnten eine höhere Prävalenz von Blutgruppe 0 bei unseren PatientInnen mit BUC (47,2 %) im Vergleich zu einer großen Kohorte von 23.145 ErstblutspenderInnen (37,6 %) (OR [95%-KI]: 1,48 [1,2–1,79]) nachweisen (Abb. 2). PatientInnen mit Blutgruppe 0 im Vergleich zu PatientInnen mit Blutgruppe A, B oder AB (Non-0) hatten auch einen signifikant höheren Blutungsschweregrad und eine höhere Anzahl an Blutungsmanifestationen. Diese Ergebnisse waren unabhängig vom Von-Willebrand-Faktor und Faktor VIII statistisch signifikant. Auch hatten PatientInnen mit Blutgruppe 0 signifikant häufiger Blutungen aus der Mundhöhle (26,1 vs. 14,3 %). In weiteren Analysen der Gerinnselbildung im Plasma (Plasma Clot Formation Assay) sowie im Vollblut (ROTEM) konnten wir zeigen, dass Blutgruppe 0 die Festigkeit des Blutgerinnsels beeinflusst.
Unsere Studie erhielt den Mary Rodes Gibson Award für den höchstbewerteten Abstract im Bereich „Hämostase und Thrombose“ und wurde beim „Best of ASH“ zitiert; auch konnten wir die Daten rezent im Journal Blood Advances publizieren.5
Resümee
Beim ASH 2020 wurden viele wichtige Daten aus klinischen Studien zu Blutungskrankheiten wie Hämophilie B oder Immunthrombozytopenie präsentiert, die in naher Zukunft zu Adaptierungen der Standardbehandlung von BlutungspatientInnen führen könnten. Viele Ergebnisse aus der translationalen Forschung könnten in Zukunft zu weiteren Fortschritten bei der Diagnostik und Behandlung von BlutungspatientInnen führen.
- Johnsen JM et al., Results of Genetic Analysis of 11,341 Participants Enrolled in the My Life, Our Future (MLOF) Hemophilia Genotyping Initiative. Blood 2020; 136(Suppl 1):19
- Pipe SW et al., First Data from the Phase 3 HOPE-B Gene Therapy Trial: Efficacy and Safety of Etranacogene Dezaparvovec (AAV5-Padua hFIX variant; AMT-061) in Adults with Severe or Moderate-Severe Hemophilia B Treated Irrespective of Pre-Existing Anti-Capsid Neutralizing. Blood 2020; 136(Suppl 2): LBA-6
- Bradbury CA et al., A Multicentre Randomised Trial of First Line Treatment Pathways for Newly Diagnosed Immune Thrombocytopenia: Standard Steroid Treatment Versus Combined Steroid and Mycophenolate. the Flight Trial. Blood 2020; 136(Suppl 2):LBA-2
- Gernsheimer TB et al., Effects of Tranexamic Acid Prophylaxis on Bleeding Outcomes in Hematologic Malignancy: The a-TREAT Trial. Blood 2020; 136(Suppl 1):1–2
- Mehic D et al., Association of ABO blood group with bleeding severity in patients with bleeding of unknown cause. Blood Adv 2020; 4(20):5157–5164