Endovaskuläre Therapie der pAVK
Die periphere arterielle Verschlusserkrankung (pAVK) gewinnt in Anbetracht der immer älter werdenden Bevölkerung zunehmend an gesundheitsökonomischer Bedeutung. Einerseits spielt das Alter als Risikofaktor für die Entwicklung arteriosklerotischer Gefäßveränderungen eine entscheidende Rolle, andererseits weisen pAVK-Patienten häufig eine Vielzahl kardiovaskulärer Komorbiditäten und Risikofaktoren auf.1–3 Aus diesem Grunde ist es selbstverständlich, dass die Therapie nicht auf eine Wiedereröffnung verschlossener Gefäße beschränkt ist, sondern dass individuell sämtliche kardiovaskuläre Risikofaktoren und Komorbiditäten behandelt werden sollten.4 Endovaskuläre Verfahren werden als minimalinvasive Alternative zu chirurgischen Therapieoptionen seit Jahrzehnten in der Behandlung der pAVK angewendet, wobei gerade in den letzten Jahren durch die Entwicklung medikamentenbeschichteter Ballone und Stents die Langzeitergebnisse nach perkutaner transluminaler Angioplastie (PTA) wesentlich verbessert werden konnten.
Behandlungspfade abhängig von Klinik
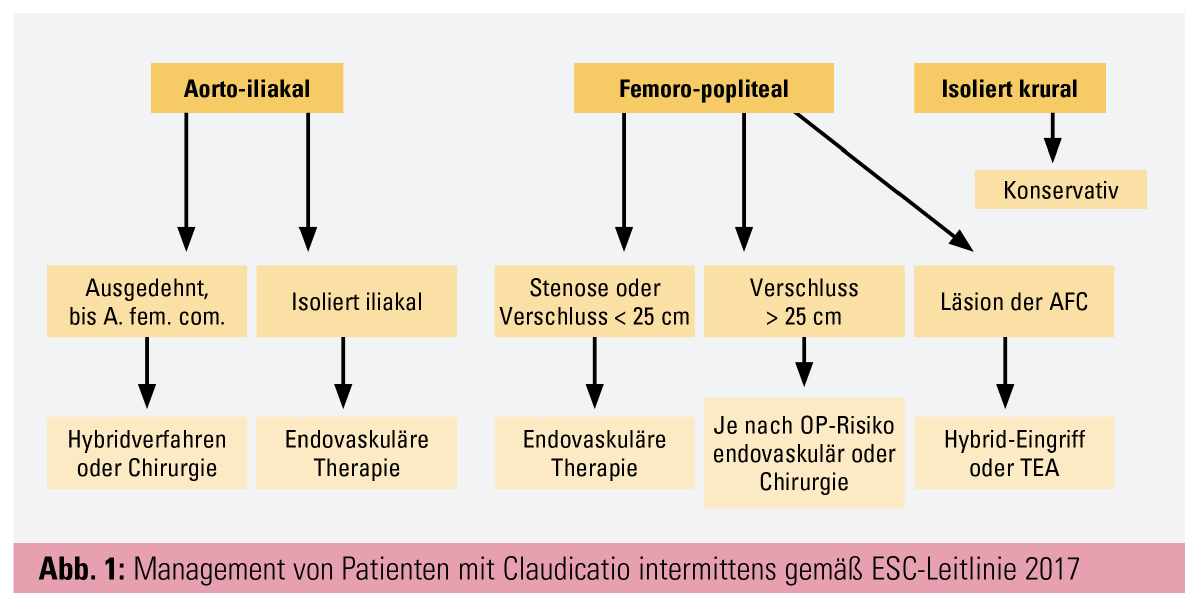
Die 2017 veröffentlichte ESC-Leitlinie zur Diagnose und Therapie der peripheren arteriellen Erkrankung stellt eine Richtlinie zur stadiengerechten Behandlung der pAVK dar. Abhängig vom betroffenen Gefäßgebiet stehen konservative, endovaskuläre und offen chirurgische Techniken zur Auswahl (Abb. 1). Bei chronisch kritischer Extremitätenischämie wird, sofern eine Revaskularisation technisch möglich erscheint, die endovaskuläre Therapie bevorzugt. Die Schwierigkeit solcher endovaskulärer Therapieverfahren liegt bereits in der Draht-Passage bei multisegmentalen langstreckigen Läsionen, welche auch den Unterschenkel betreffen können. Es ist festzuhalten, dass aus diesem Grunde vor Jahren die Läsionslänge eine entscheidende Limitierung bei endovaskulären Eingriffen darstellte. Nunmehr ist es möglich, durch den kombinierten Einsatz verschiedener Zugangswege, wie zum Beispiel die gleichzeitige Punktion am Unterschenkel mit distaler retrograder Drahtpassage von Gefäßverschlüssen, auch komplexe und langstreckige Läsionen komplikationsarm zu überwinden und nachfolgend mittels Ballonangioplastie oder Stentimplantation zu versorgen. Nach erfolgreicher Passage der Läsion mit dem Führungsdraht stellt sich jedoch die Frage, welche endovaskuläre Therapie gewählt werden sollte. Neben einer Ballonangioplastie werden heutzutage verschiedene gefäßmodulierende Verfahren im Rahmen einer sogenannten „vessel-preparation“ eingesetzt. Hierzu zählen ablatierende Verfahren wie die Atherektomie, Laserverfahren, Vordilatation mit metallverstärkten Ballonen oder die Stoßwellen-Lithoplastie von Kalkplaques mittels spezieller Lithoplastie-Ballonkatheter. In der Regel folgt anschließend eine Ballondilatation mit herkömmlichen Ballons oder auch medikamentenbeschichteten Ballonen.
Medikamentenbeschichtete Devices
Paclitaxel-beschichtete Ballone erhielten vor allem im femoropoplitealen Bereich in den letzten Jahren einen großen Stellenwert, da diese im Vergleich zu herkömmlichen Ballonen eine wesentlich geringere Restenose- und Reinterventionsrate aufwiesen. Durch den Einsatz solcher Ballone konnte zudem in vielen Fällen auf eine sekundäre Stentimplantation verzichtet werden. Eine Vielzahl von Studien konnte diese positiven Effekte bestätigen, sodass zahlreiche Paclitaxel-beschichtete Ballonkatheter und Stents zum Einsatz im femoropoplitealen Bereich zugelassen wurden. Im Dezember 2018 wurde von Katsanos erstmals eine Metaanalyse veröffentlicht, welche einen möglichen Zusammenhang dieser Paclitaxel-beschichteten Devices mit einer erhöhten Mortalität untersuchte.5 Nach einem Beobachtungszeitraum von 1 Jahr gab es bei 4.432 in diversen Studien untersuchten Patienten keinen Unterschied betreffend Mortalität. Die Autoren beschrieben jedoch im längeren Beobachtungszeitraum nach 2 Jahren bei über 2.300 Patienten eine erhöhte Mortalität im Paclitaxel-Arm von 7,2 % verglichen zu 3,8 % in der Kontrollgruppe. Ein ähnliches Ergebnis wurde bei einer kleineren Gruppe mit längerem Beobachtungsintervall von bis zu 5 Jahren (3 RCTs mit 863 Patienten) berichtet (Mortalitätsrisiko von 14,7 % im Paclitaxel-Arm verglichen zu 8,1 % in der Kontrollgruppe). Diese Studie schlug große Wellen, es folgten zahlreiche Nachberechnungen, Untersuchungen durch die FDA, zahlreiche Podiumsdiskussionen und Boards mit unterschiedlichen länderspezifischen Empfehlungen.6 Auf der anderen Seite gab es im selben Zeitraum einen deutlichen Rückgang des Einsatzes von Paclitaxel-beschichteten Ballonen im klinischen Alltag. Eine Arbeitsgruppe in Münster untersuchte, ob diese Beobachtung tatsächlich auch außerhalb von Studien nachvollzogen werden kann. Der Einsatz von Paclitaxel-beschichteten Devices wurde anhand der Codierung versicherungstechnischer Daten der BARMER-Krankenversicherung von 2007 bis 2015 erhoben, und diese Fälle wurden bis Ende 2017 nachverfolgt.7 Im gewählten Zeitraum wurden über 100.000 endovaskuläre Therapien durchgeführt und hierbei über 23.000 medikamentenbeschichtete Devices eingesetzt. Es konnte jedoch im Gegensatz zu den von Katsanos publizierten Daten keine erhöhte Mortalität im Vergleich zur Kontrollgruppe festgestellt werden.
Peri- und postinterventionelle medikamentöse Therapie
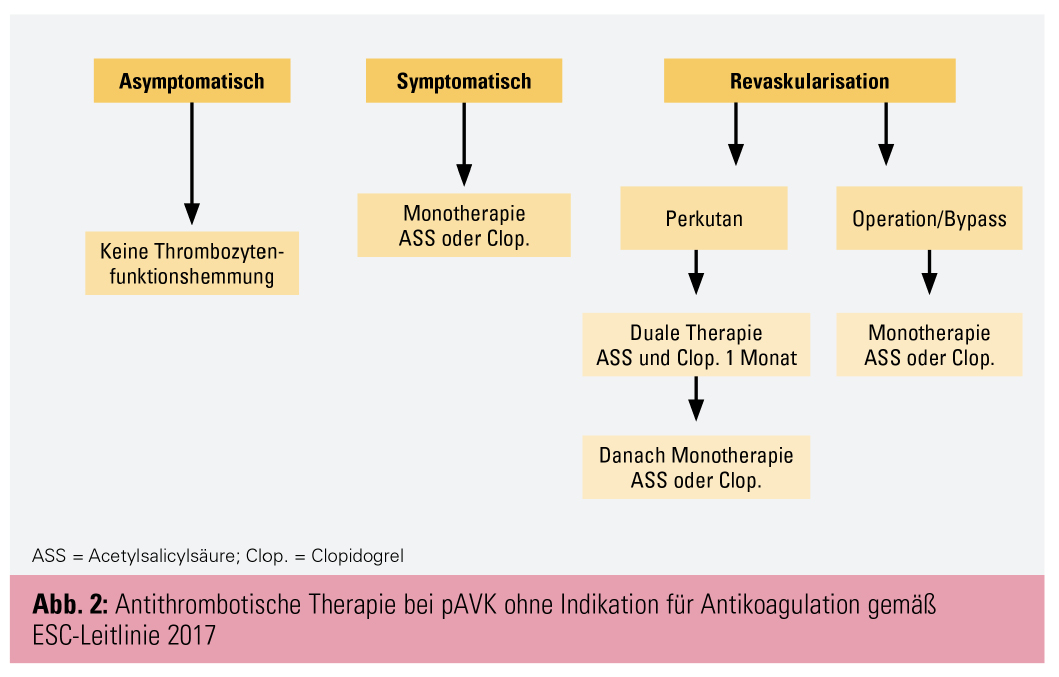
Nachdem bei jedem endovaskulären Eingriff der Zugang über eine Schleuse erfolgt, welche selbst das Lumen etwas einengt und durch den Kunststoff und den Totraum in der Schleuse durchaus thrombophil ist, wird routinemäßig periinterventionell Heparin appliziert. Die Dosis ist nicht einheitlich, meist werden zwischen 2.000 IU und 5.000 IU unfraktioniertes Heparin periinterventionell verabreicht. Postinterventionell scheint für die Dauer der Hospitalisierung eine Thromboseprophylaxe ausreichend zu sein. Neben der periinterventionellen Hemmung des plasmatischen Gerinnungssystems wird im Rahmen der Sekundärprophylaxe eine Thrombozytenfunktionshemmung empfohlen. Gemäß ESC-Leitlinien wird nach endovaskulärer Therapie eine Monotherapie bzw. in speziellen Fällen eine duale antithrombotische Therapie empfohlen (Abb. 2).4
Die COMPASS-Studie untersuchte bei fast 27.400 Patienten die Anwendung von niedrig dosiertem Rivaroxaban in Kombination mit ASS 100 mg verglichen zu ASS allein.8 Die Studie wurde aufgrund der positiven Daten in der Zwischenanalyse vorzeitig gestoppt. Rivaroxaban reduzierte die Mortalität in diesem Kollektiv um 20 %, sodass die Kombination von Rivaroxaban 2,5 mg 2-mal täglich und ASS 100 mg täglich im Hinblick auf eine Reduktion der Gesamtmortalität und kardiovaskulären Mortalität die derzeit vielversprechendste Kombination darstellt.
Tagesklinische Therapie
Endovaskuläre Therapien der Beinarterien erfolgen fast ausschließlich mit einem antegraden oder retrograden Gefäßzugang über die A. femoralis communis. Aufgrund der Größe der zu behandelnden Gefäße und der Größe verschiedener Devices werden Schleusen mit einer Größe zwischen 4F und 6F eingesetzt. Nach fakultativem Verschluss der Punktionsstelle mit einem Verschluss-System, einer manuellen Kompression der Punktionsstelle und schließlich der Anlage eines Druckverbandes werden die Patienten postinterventionell im stationären Bereich nachbeobachtet. Dies geschieht in der Regel bis zum Folgetag. Mit dem Tag der Aufklärung und Vorbereitung ist eine Gefäßintervention in den meisten Fällen mit 2 Übernachtungen im Krankenhaus verbunden. Einzelne Studien untersuchten die Möglichkeit einer tagesklinischen Gefäßintervention.9, 10 Der Eingriff wird wie oben beschrieben durchgeführt, die Patienten werden 6 Stunden nachbeobachtet und bei komplikationslosem Verlauf entlassen. Eine Untersuchung von knapp 500 Patienten konnte diesen tagesklinischen Ansatz bestätigen, wobei die Raten an medizinisch notwendigen Nachuntersuchungen und Wiederaufnahmen mit 1,8 % und 0,6 % sehr niedrig waren.9
Zusammenfassung und Ausblick
Die periphere arterielle Verschlusserkrankung wird aufgrund der demografischen Entwicklung weiterhin zunehmend an Bedeutung gewinnen. Neben einer Optimierung kardiovaskulärer Risikofaktoren stellen endovaskuläre Therapieverfahren sowohl bei Patienten mit Claudicatio intermittens als auch mit chronisch kritischer Extremitätenischämie eine vielversprechende Therapie dar. Neue Devices und spezielle beschichtete Ballonkatheter oder Stents haben das Ziel, die bereits guten Langzeitergebnisse weiter zu verbessern. Medikamentenbeschichtete Devices stehen zwar in Diskussion, die derzeitige Datenlage unterstützt jedoch den weiteren Einsatz. In speziellen Fällen scheinen tagesklinische Interventionen sicher durchführbar zu sein.
- Kersting J et al., Fortschr Röntgenstr 2019; 191:311–22
- Lawall H et al., VASA 2016; 45 (Suppl. 95):1–100
- Malyar N et al., Eur Heart J 2013; 34:2706–14
- Aboyans V et al., Eur Heart J 2018; 39(9):763–816
- Katsanos K P et al., J Am Heart Assoc 2018; 7(24):e011245
- Beckman JA, White CJ, Circulation 2019; 140(16):1342–51
- Freisinger E et al., Eur Heart J 2019; pii: ehz698. DOI: 10.1093/eurheartj/ehz698. [Epub ahead of print]
- Branch KR et al., Circulation 2019; 140(7):529–37
- Malekzadeh S et al., Diagn Interv Imaging 2019; 100(6):347–52
- Islam AM et al., Catheter Cardiovasc Interv 2018; 92(2):358–63