PRO & CONTRA AUS DER SICHT DES KARDIOLOGEN
Die Aortenklappenstenose ist die häufigste strukturelle Herzerkrankung in Europa, sie tritt zumeist bei älteren Erwachsenen auf.1–3 Die Prognose der Patienten mit unbehandelter signifikanter Aortenklappenstenose ist schlecht: insbesondere bei symptomatischen Patienten tritt der plötzliche Herztod bei ca. 1 % der Patienten ein, ein symptomfreies Überleben innerhalb von 2 Jahren bewegt sich lediglich zwischen 20 und 50 %! Insbesondere beim Auftreten von ersten klinischen Beschwerden verschlechtert sich die Überlebensprognose signifikant – und dies bereits innerhalb weniger Monate.4 Dementsprechend werden, je nach klinischem Zustandsbild, klare graduelle Empfehlungen zur operativen Sanierung einer Aortenklappenstenose abgegeben.5
Operationsrisiko
Das Operationsrisiko ist im Allgemeinen gering (1–3 %), dies allerdings nur bei reinem Aortenklappenersatz. Wird die Operationsindikation auf Interventionen an den Koronargefäßen oder an der Aorta ausgedehnt, steigt das Risiko auf 10–25 %.6 Kommen Faktoren wie schlechte Linksventrikelfunktion, hohes Alter oder zusätzliche Komorbiditäten dazu, wird das OP-Risiko noch um ein Vielfaches höher. Aus diesen Gründen wurden und werden nach wie vor zahlreiche Patienten mit oben erwähntem höheren Operationsrisiko bezüglich eines konservativen Klappenersatzes abgelehnt oder erst gar nicht evaluiert.7 Dies wird durch statistische Überlegungen bestätigt, dass allein in der Europäischen Union ca. 600.000 Patienten eine Indikation für einen Aortenklappenersatz hätten, pro Jahr aber „nur“ 60.000 operiert werden.8
Alternativen
Genau hier setzen innovative Konzepte der modernen Aortenklappenintervention an: Nachdem die konservative Therapie der symptomatischen signifikanten Aortenklappenstenose mit einem wesentlich schlechteren Überleben kombiniert ist9, die perkutane Aortenklappensprengung mittels Ballonvalvuloplastie nur intermediäre klinische Erfolge verzeichnete und daher als „Bridging“ empfohlen wird, suchte man nach alternativen Verfahren und wurde, dank technischer und medizinischer hochkarätiger Entwicklung, fündig. Das Resultat sind die kathetergestützten Aortenklappeninterventionsverfahren mittels transfemoralen, transapikalen, transaortalen oder transaxillären (Subclavia) Zugängen. Aus kardiologischer Sicht imponiert bei diesen kathetergestützten Techniken der weniger invasive Zugangsweg im Vergleich zur Operation am offenen Herzen. Das somit mögliche Umgehen der extrakorporalen Zirkulation sowie die potenzielle Intervention ohne Vollnarkose eröffnen neue Perspektiven. Weitere Vorteile liegen in der kürzeren Erholungszeit, der schnelleren Mobilisierung und der Reduktion von Infektionen und Bluttransfusionen.
Entwicklung und Lernkurve
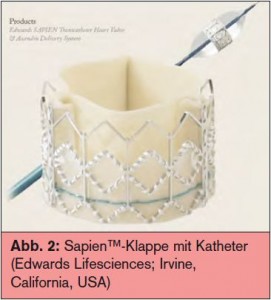
Die ersten Untersuchungen mit der Core Valve- ReValving™-Klappe (Medtronic; Minneapolis, Minnesota, USA), einer selbstexpandierenden Nitinol-gestützten Klappe mit Schweineperikard, als auch der Sapien™-Klappe (Stainless- Steel-Klappe mit Rinderperikardbesatz; Edwards Lifesciences; Irvine, California, USA) waren reine Machbarkeits- und Sicherheitsstudien. Die technische Machbarkeit dieser Interventionen war von Anfang an gegeben (Erfolgsrate 95–100 %!), die Komplikationsraten waren häufig, aber akzeptabel. Letztere betrugen für Schlaganfälle zwischen 5 und 9 %, Myokardinfarkte/ Troponinanstiege bis 20 %, Gefäßkomplikationen bis 22 % und, insbesondere bei der CoreValve™, eine notwendige dauerhafte Schrittmacherimplantationsrate von bis zu 25 %.10–13 Diese konnte inzwischen jedoch durch eine bessere Auswahl der Klappenimplantationshöhe deutlich verbessert werden. Die Lernkurve mit mehr erfahrenen Operateuren sowie die immer kleiner werdenden Größen der klappentragenden Katheter (derzeit 18 French für CoreValve™, 22 French für Sapien ™) trugen zuletzt zu einer deutlichen Reduktion der Komplikationsraten bei. Zudem wurde (auch rezent in Österreich über eine eigens eingerichtete Task-Force der Österreichischen Kardiologischen Gesellschaft und der Österreichischen Gesellschaft für Thorax- und Herzchirurgie) per Positionspapier die Formierung so genannter „Heart Teams“ eingefordert, in welchen Herzchirurgen und interventionelle Kardiologen anhand der Klinik des Patienten und seiner vorliegenden Befunde die Indikation für den Transkatheter-Aortenklappeneingriff gemeinsam beschließen und planen. Auch die hierzu notwendigen logistischen, bildgebenden und personellen Strukturen werden analog zu internationalen Kriterien definiert.
Randomisierter Methodenvergleich
Trotz allem muss klar gesagt werden, dass es bisher keine eindeutig randomisierte Studie gibt, welche Patienten mit konventioneller Aortenklappenoperation mit TAVI-Patienten vergleicht. Diese Studien (PARTNER-Studie, Kohorte A und B) laufen jedoch und erste Ergebnisse sollten Ende 2011 vorliegen. Im Vergleich zur medikamentösen Standardtherapie (PARTNER-Studie, Kohorte B) zeigte sich jetzt bereits zum ersten Mal in einer randomisierten Studie, dass die TAVI-Behandlung beim inoperablen Patienten Überleben und Lebensqualität gegenüber der medikamentösen Therapie signifikant verbessert.14 Zu bedenken bleibt, dass die PARTNER-Studie nur bei Patienten mit transfemoralem TAVIZugang durchgeführt wurde. Der transapikale Ansatz mit weniger vaskulären Komplikationen, weniger Schlaganfällen trotz eines vielfach „schlechteren“ Patientenguts, könnte hier zusätzlich für ergänzende Antworten sorgen. Im europäischen nicht-randomisierten großen SOURCE-Register werden dagegen sowohl transfemorale als auch transapikale TAVI-Patientendaten bezüglich der Therapieerfolgsund Komplikationsraten erfasst, diese jedoch nicht randomisiert mit konservativ behandelten Patienten verglichen.
Optimale Patientenselektion
Zahlreiche präinterventionelle Untersuchungen beim Screenen der TAVI-Patienten müssen dazu beitragen, den „richtigen“ Kandidaten für den Transkatheter-Eingriff zu definieren. Viele anatomisch-morphologische, klinische und geriatrische Aspekte müssen hier zusammengetragen werden, um in die interdisziplinäre Entscheidung einzufließen. Die Tatsache, dass mit der TAVI-Technik eine neue Dimension der Aortenklappentherapie eröffnet wird, hat bereits dazu geführt, dass immer mehr, früher als untherapierbar geltende ältere Patienten mit hohem OP-Risiko zur Evaluierung ihrer Therapieoptionen neuerlich oder sogar primär zugewiesen werden. Dies wird, kombiniert mit der demographischen Entwicklung der Bevölkerung in den nächsten Jahren, dazu beitragen, dass wir mehr und mehr Patienten sehen werden, die bezüglich ihrer Aortenklappenerkrankung neu evaluiert werden müssen und unter Umständen auch an spezialisierten Zentren konventionell operiert werden. Eine spannende Entwicklung, wenn man bedenkt, welch große wirtschaftlichen und ethischen Überlegungen hier beinhaltet sind. Nur unter diesen Voraussetzungen jedoch kann derzeit ein nicht operabler Patient zum TAVI-Eingriff selektioniert werden. Die Ergebnisse der konventionellen Aortenklappenchirurgie, insbesondere bei fehlenden Daten bezüglich der Klappenhaltbarkeit bei TAVI, sind definitiv zu gut, um als Goldstandard beim operablen Patienten abgelöst zu werden. Motivierend ist es jedoch, zu lernen, zu erfahren und dazu beizutragen, dass es für Patienten mit hochgradiger Aortenklappenstenose, die vor nicht allzu langer Zeit noch als untherapierbar galten, viel versprechende neue Möglichkeiten der Lebensverlängerung und Verbesserung der Lebensqualität gibt.
FACT-BOX
Der „nicht operable“ Hochrisikopatient mit
signifikanter Aortenklappenstenose
bekommt durch den TAVI-Eingriff eine neue
therapeutische Perspektive bezüglich
Lebensverlängerung und Lebensqualität.
Einführung und Verbesserung der Lernkurve
der neuen Techniken können nur durch
enge Kooperation zwischen interventionellen
Kardiologen und Herzchirurgen
gewährleistet werden. Die Ergebnisse von
randomisierten Studien (TAVI vs. konventionelle
OP) sind dringend gefordert, erste
diesbezügliche Daten werden noch in diesem
Jahr publiziert.
1 Soler-Soler J. et al., Heart 2000; 83:721-725
2 Lung B. et al., Eur Heart J 2003; 24:1231-1243
3 Stewart B.F. et al., J Am Coll Cardiol 1997; 29:630-634
4 Lund O. et al., Thorac Cardiovasc Surg 1996; 44:289-295
5 Vahanian A. et al. Eur Heart J 2007; 28:230-268
6 Kolh P. et al., Eur J Cardiothorac Surg 2007; 31:600-6
7 Lung B. et al., Eur Heart J 2005; 26:2714-2720
8 Serruys P.W., EuroInterv 2009; 4:558-565
9 Varadarajan P. et al., Ann Thorac Surg 2006; 82:2111-5
10 Piazza N. et al., EuroInterv 2008; 4:242-249
11 Gerckens U. et al., JACC Cardiovasc Interv 2010; 3:244-50
12 Thomas M. et al., Circulation 2010; 122:62-69
13 Rodés-Cabau J. et al., J Am Coll Cardiol 2010; 55:1080-90
14 Leon M.B. et al., N Engl J Med 2010; 363:1597-1607