„Vascular protection“ bei Patienten mit chronischer pAVK
Mit einer Prävalenz von ca. 15 % ist die pAVK eine weit verbreitete Erkrankung, welche zumeist auf fortschreitender Arteriosklerose beruht. Die Prävalenz nimmt mit steigendem Lebensalter stetig zu, sodass bei den über 80-Jährigen sogar jeder Fünfte betroffen ist.1–3 Arteriosklerose betrifft selten nur einen Gefäßabschnitt und tritt oftmals generalisiert auf, was sowohl das Risiko für kardiovaskuläre als auch für zerebrovaskuläre Ereignisse erhöht. Vielfach konnte der Zusammenhang zwischen pAVK und erhöhter kardiovaskulärer Mortalität sowie Morbidität gezeigt werden, sowohl bei symptomatischen als auch bei asymptomatischen Patienten.4 In Anbetracht des hohen kardiovaskulären Risikos sind ein frühzeitiges Erkennen, die Etablierung einer adäquaten Therapie sowie ein konsequentes Management der Risikofaktoren somit unverzichtbar.
Klinik und Diagnose
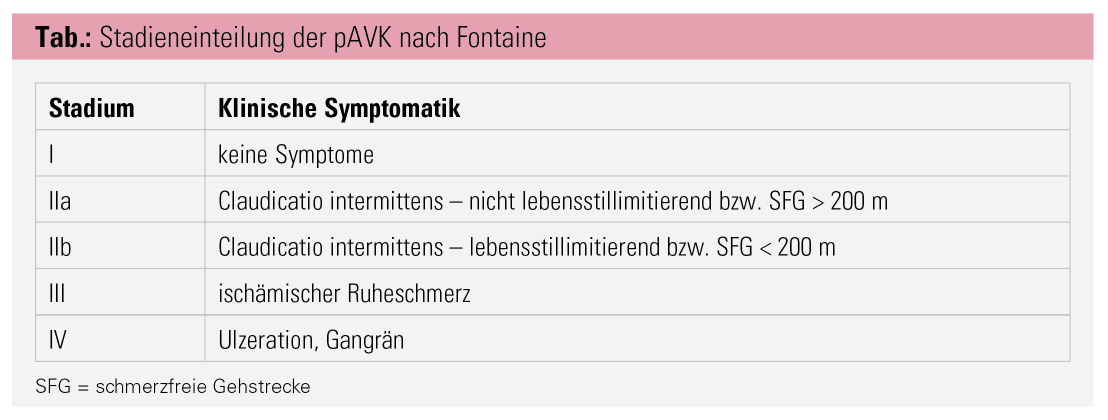
Im Gegensatz zur akuten pAVK, welche durch lokale Thrombosen oder arterielle Embolien entsteht und sich durch akut einsetzenden ischämischen Schmerz äußert, entwickeln sich chronisch obliterierende Gefäßprozesse eher langsam und bleiben länger unterdiagnostiziert. Die Klinik ist vom Grad der Lumeneinengung des Gefäßes abhängig (eine Übersicht der Stadieneinteilung ist in der Tabelle abgebildet) und reicht vom kompletten Fehlen von Symptomen über die klassische Claudicatio-intermittens-Symptomatik („Schaufensterkrankheit“) bis hin zum Ruheschmerz oder Bestehen von chronischen Wunden. Bedenkt man das hohe kardiovaskuläre Risiko sowie die damit verbundenen Risiken, ist besonders auf die Gruppe der asymptomatischen pAVK hinzuweisen. Bis zu 50 % der Patienten haben lange Zeit keine Symptome, bleiben somit lange unterdiagnostiziert und erhalten folglich auch keine optimale Therapie im Sinne einer kardiovaskulären Risikoreduktion.5
Als einfaches Screeningtool dient die ABI-Messung (Knöchel-Arm-Index, engl.: „ankle-brachialindex“), welche gut mit dem allgemeinen kardiovaskulären Risiko korreliert.6 Laut den aktuellen Guidelines der European Society of Cardiology (ESC) zur pAVK von 20177 wird eine ABI-Messung für folgende Patientengruppen empfohlen:
- Patienten mit V. a. pAVK (fehlende/abgeschwächte Fußpulse, typische Claudicatio-intermittens-Symptomatik, chronische Wunden, …)
- ALLE Patienten ab 65 Jahren
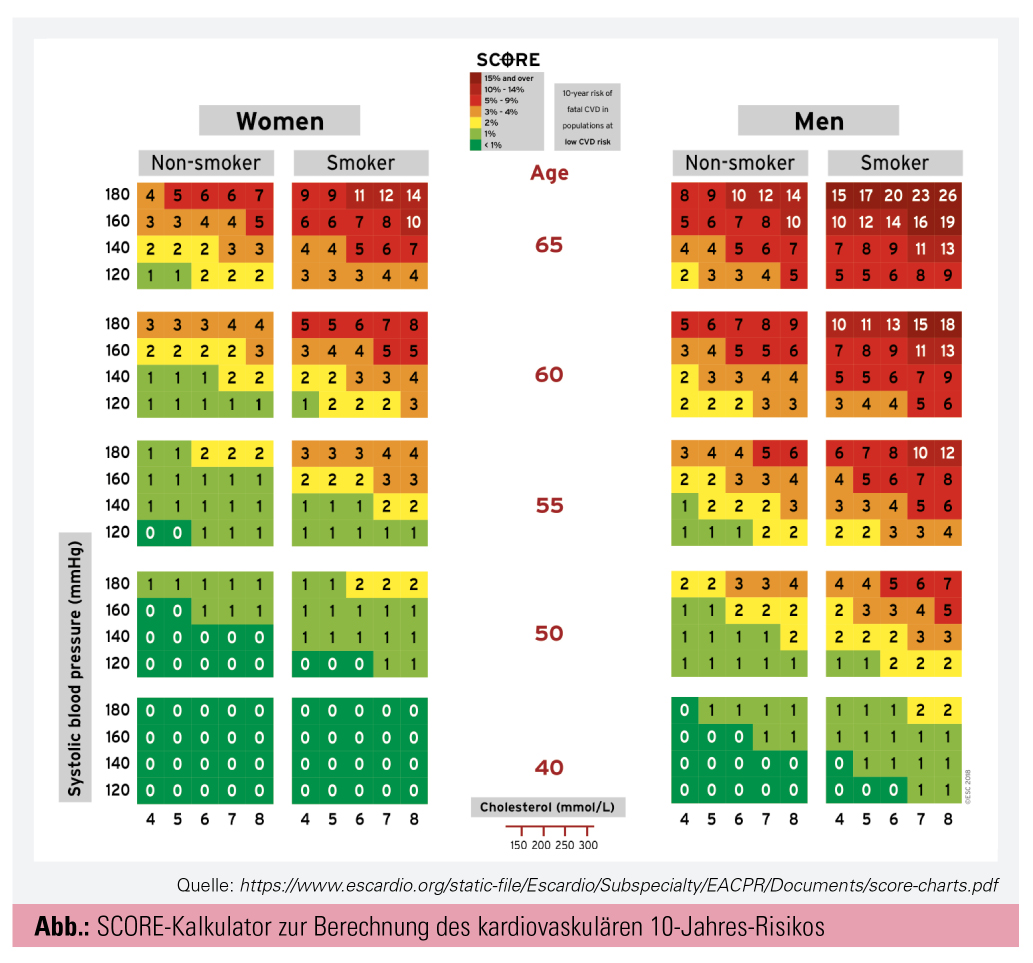
- Patienten < 65 Jahren mit hohem kardiovaskulärem Risiko lt. ESC (Abb.)
- Patienten ab 50 Jahren mit positiver Familienanamnese hinsichtlich pAVK
- Patienten mit hohem Risiko für das Vorliegen einer pAVK aufgrund ihrer Vorerkrankungen (andere arteriosklerotische Erkrankung, KHK, bekanntes abdominelles Aortenaneurysma, chronische Niereninsuffizienz oder Herzinsuffizienz)
Bei pathologischem ABI (< 0,9 als Hinweis auf das Vorliegen einer pAVK oder > 1,4 bei Mediasklerose) sollte weiterführend eine farbkodierte Duplexsonografie erfolgen. Eine weiterführende Bildgebung mit Hilfe von CT- oder MR-Angiografie ist bei unzureichender duplexsonografischer Untersuchungsqualität hilfreich, jedoch zur Diagnosefindung nicht grundsätzlich notwendig.
Therapieprinzipien im Sinne einer „vascular protection“
Ist die Diagnose einmal gestellt, gilt es, das kardiovaskuläre Risiko des Patienten bestmöglich zu senken. Die Basis einer jeden pAVK-Therapie stellt neben der Lifestylemodifikation ein adäquates Management der Risikofaktoren dar. Hierzu zählen Hyperlipidämie, arterielle Hypertonie, Diabetes mellitus sowie Nikotinabusus.1 Ziel einer optimalen Therapie sind einerseits die Behandlung symptomatischer Läsionen sowie die Verhinderung von Folgeschäden und andererseits die Verhinderung einer weiteren Progression der bestehenden arteriosklerotischen Veränderungen sowie eine Plaquestabilisierung.
Lifestylemodifikation: Allen voran sei hier die dringende Notwendigkeit einer Nikotinkarenz erwähnt. Sowohl aktives Rauchen als auch die Höhe der Packyears korrelieren gut mit dem Vorhandensein einer pAVK, ein konsequenter Rauchstopp kann sowohl die Symptome einer pAVK lindern als auch das kardiovaskuläre Risiko senken.2 Wenn möglich, sollten zur Förderung der Compliance strukturierte Raucherentwöhnungsprogramme in Anspruch genommen werden. Weitere Grundpfeiler der konservativen Therapie sind die regelmäßige Durchführung eines strukturierten Gehtrainings sowie eine ausgewogene Ernährung und das Anstreben von Normalgewicht.8
Hyperlipidämie: Alle Patienten sollten als Basismedikation ein Statin erhalten. Zielwert ist ein LDL-Cholesterin < 55 mg/dl bzw. eine Senkung um zumindest 50 % vs. Baseline.9
Arterielle Hypertonie: Als einer der Hauptrisikofaktoren für Arteriosklerose ist für alle pAVK-Patienten ein Blutdruckzielwert von < 140/90 mmHg anzustreben. Hierzu sind alle Antihypertensiva geeignet, wobei in Hinblick auf ihre Potenz, das kardiovaskuläre Risiko zu reduzieren, primär ACE-Hemmer bzw. Angiotensinrezeptorblocker empfohlen werden.7 Entgegen der weitläufigen Meinung ist die Verwendung von Betablockern bei pAVK-Patienten nicht grundsätzlich kontraindiziert. Statistisch gesehen konnte bisher kein Nachteil bei der Behandlung mit Betablockern nachgewiesen werden, weder hinsichtlich Verschlechterung der Gehstrecke noch hinsichtlich der Einjahresmortalität oder Amputationsrate.10, 11 Einzig bei chronisch kritischer Extremitätenischämie ist die Gabe derselben zu überdenken.
Diabetes mellitus: Eine strikte Blutzuckerkontrolle wird für alle Betroffenen empfohlen. Im Vergleich zu Patienten ohne Diabetes entwickeln Diabetiker früher arteriosklerotische Veränderungen und erleiden meist einen schwereren Verlauf mit häufig auftretenden Ischämien.12 Besonders problematisch ist hier auch die Tatsache, dass die Symptomatik durch die oftmals auch bestehende diabetische Polyneuropathie verschleiert und die Diagnose somit verzögert wird. Die Wahl der Medikation sollte entsprechend den aktuellen diabetologischen Richtlinien erfolgen.
Thrombozyten-aggregationshemmer
Die Etablierung eines Thrombozytenaggregationshemmers wird zur Sekundärprophylaxe für alle symptomatischen Patienten sowie für jene, welche sich einer interventionellen oder chirurgischen Sanierung einer Gefäßstenose unterzogen haben, lebenslang empfohlen. Eine grundsätzliche Thrombozytenaggregationshemmung bei asymptomatischen Patienten (als Primärprävention) sollte nicht erfolgen, da hier in Studien kein Vorteil belegt werden konnte.7 Besonderes Augenmerk und eine gezielte Anamneseerhebung sei hier auf die sogenannte „maskierte AVK“ gelegt – z. B. Patienten, welche aufgrund einer zusätzlich bestehenden Erkrankung wenig Bewegung betreiben und daher keine Claudicatio-Symptomatik entwickeln. Prinzipiell sollte Clopidogrel der Vorzug vor T-ASS gegeben werden. Bei gleichzeitig bestehender Indikation zur oralen Antikoagulation ist diese als Basistherapie ausreichend. Das Therapieregime nach Intervention, etwa vorübergehende duale Thrombozytenaggregationshemmung nach Stentimplantation, sollte vom betreuenden Zentrum vorgeschrieben werden.
Interventionelle Sanierung
Bei asymptomatischen Patienten oder Patienten mit akzeptabler Claudicatio-intermittens-Symptomatik ohne Wunden sollte ein konservatives Procedere gewählt werden. Ab dem klinischen Stadium IIb, d. h. den Lebensstil einschränkenden Symptomen, sowie im Stadium III und IV sollte ein gefäßeröffnendes Prozedere angestrebt werden. Läsionen im infrapoplitealen Bereich stellen sowohl interventionell als auch chirurgisch aufgrund der schlechten Erreichbarkeit sowie der geringen Gefäßgröße im Vergleich zu proximalen Regionen eine besondere Herausforderung dar und sollten lediglich bei kritischer Ischämie (Stadium III oder IV) saniert werden. Aus internistisch-angiologischer Sicht sollte einem interventionellen Vorgehen, wenn möglich, der Vorzug gegeben werden. Je nach Lokalisation der Problematik kann jedoch auch ein primär chirurgisches Vorgehen sinnvoll sein (vgl. TASC-II-Kriterien). Eine gute interdisziplinäre Zusammenarbeit zwischen Interventionalisten und Chirurgen sollte jedenfalls, besonders bei komplexen Läsionen, angestrebt werden.
Resümee
Das Vorhandensein einer pAVK sowohl in symptomatischen als auch in asymptomatischen Stadien stellt für Betroffene ein hohes kardiovaskuläres Risiko dar. Neben einer frühzeitigen Diagnosestellung sowie einem Screening für Risikogruppen und generell ab einem Lebensalter von 65 Jahren ist vor allem ein striktes Management der Risikofaktoren zur individuellen Senkung des kardiovaskulären Risikos von großer Bedeutung. Betroffene sollten engmaschig kontrolliert und frühzeitig an Spezialisten angebunden werden, um die Lebensqualität zu steigern, den Extremitätenerhalt sowie die Reduktion von Mortalität langfristig zu ermöglichen.
- Gul F, Janzer SF, Peripheral Vascular Disease. [Updated 2020 Nov 20]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2020 Jan
- Shammas NW, Vasc Health Risk Manag 2007; 3(2):229–34
- Lawall H et al., CardioVasc 2014; 14:34–40
- Criqui MH, Aboyans V, Circ Res 2015; 116(9):1509–26
- Kalbaugh CA et al., J Am Heart Assoc 2017; 6(5):e003796
- Visonà A et al., Eur J Intern Med 2020; 77:79–85
- Aboyans V et al., Eur Heart J 2018; 39(9):763–816
- McDermott MM, J Vasc Surg 2017; 66(5):1612–20
-
Mach F et al., Eur Heart J 2020; 41(1):111-88
- Paravastu SC et al., Cochrane Database Syst Rev 2013; 2013(9):CD005508
- Mirault T et al., Medicine 2017; 96(5):e5916
- Balletshofer B et al., Exp Clin Endocrinol Diabetes 2019; 127(S 01):S105–S113