Diabetes mellitus Typ 2 – Management beim geriatrischen Patienten
Global steigt die Diabetesprävalenz vor allem bei geriatrischen Patienten stetig. Bei weltweit geschätzt 451 (8,4 %) Millionen Fällen wird für 2045 ein Anstieg auf 693 (9,9 %) Millionen prognostiziert, wobei der stärkste altersspezifische Anstieg für die Gruppe der 60–79-jährigen Bevölkerung vorausgesagt wird.1, 2
Das Kollektiv der geriatrischen Patienten mit Diabetes mellitus Typ 2 (T2DM) ist jedoch heterogen: Einige Patienten sind weitgehend gesund, entwickeln Diabetes spät und erleiden infolgedessen keine Komplikationen. Andererseits weisen 40 % der älteren Diabetespatienten vier oder mehr Komorbiditäten auf.3, 4 Zudem führt die implementierte Medikation infolge der Multimorbidität zu Polypharmazie und ferner zu arzneimittelinduzierten Komplikationen mit Prognoseverschlechterung.5Aufgrund dieses heterogenen und in Zukunft weiterwachsenden Kollektivs war es in den letzten Jahren notwendig, das Management des geriatrischen Patienten mit T2DM, inklusive Therapiezielsetzung und Therapiewahl, zu überdenken.
Diagnosestellung
Die Diagnosestellung wird zwar bei allen Altersklassen gleich gestellt, mittels Bestimmung der Nüchternblutglukose, der 2-Stunden-Glukose nach Gabe von 75 g im OGTT oder des HbA1c-Wertes, jedoch kommt es aufgrund der progredienten β-Zell-Dysfunktion bei älteren Patienten häufig zu postprandialen Hyperglykämien. Die Diagnosestellung kann durch alleinige Nüchternblutzuckermessungen verzögert werden. Infolgedessen sollte im Rahmen des Screenings der HbA1c-Wert (oder OGTT) herangezogen werden.6
Therapie: Wie intensiv?
In randomisierten kontrollierten Studien konnte nachgewiesen werden, dass eine intensivierte Blutzuckerkontrolle, das heißt bei einem HbA1c-Wert von zumindest unter 7 %, einen mikro- und makrovaskulären Benefit bringt, jedoch erst nach einer längeren Behandlungsdauer von 5 bis 10 Jahren, sodass dieser bei geriatrischen Patienten möglicherweise nicht mehr erlebt wird. Auch zeigte sich zum Beispiel in der ACCORD-Studie 2008, dass bei älteren Patienten mit fortgeschrittener Erkrankung, Komplikationen und Multimorbidität eine aggressive Therapie mit einem HbA1c-Wert von unter 6,5% schaden kann.7
Neben Hypoglykämien, die das Risiko einer Demenzentwicklung und die Frailty (Gebrechlichkeit) steigern, gilt es jedoch auch, Hyperglykämien zu vermeiden: HbA1c-Werte über 8 % sind mit erhöhten Infektionsraten, Hospitalisierung und Mortalität assoziiert.8, 9
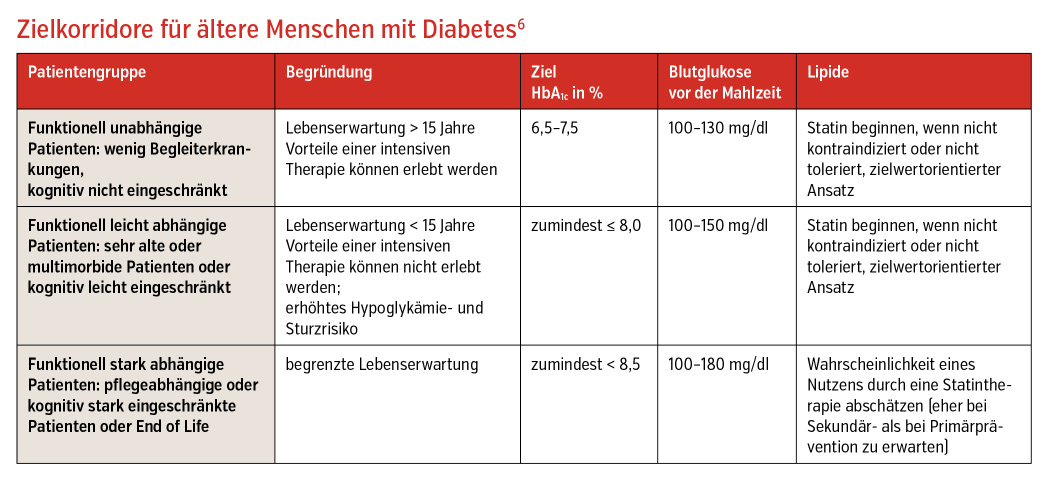
Um diesem komplexen Patientenkollektiv gerecht zu werden, empfiehlt die Österreichische Diabetes Gesellschaft eine Anpassung der Therapieziele an den funktionellen Status, die Komorbiditäten und die Kognition (siehe Tabelle).
Therapieziele: Lipide
Die Zielwerte wurden entsprechend den ESC/EAS-Lipid-Leitlinien 2019 modifiziert10: Für Patienten mit Diabetes mellitus mit hohem kardiovaskulären Risiko wird ein LDL-Zielwert von < 70 mg/dl und mit sehr hohem kardiovaskulären Risiko, also insbesondere jenen mit bereits bestehender kardiovaskulären Erkrankung, ein LDL-Therapieziel von < 55 mg/dl gefordert. In Analogie zur antidiabetischen Therapie ist bei ausgeprägter Multimorbidität, fortgeschrittener Demenz und stark eingeschränkter Lebenserwartung die Indikation individuell zu evaluieren (Tabelle).
Therapieoptionen6
Die Auswahl entspricht prinzipiell jener für jüngere Patienten und wird je nach Komorbiditäten, Verträglichkeit, Nebenwirkungen und Kontraindikationen getroffen. Die Compliance fördernd sind einmal täglich zu verabreichende Antidiabetika und Kombinationspräparate. Besonders bei normal- beziehungsweise untergewichtigen hochbetagten Patienten ist weiters die gewichtsreduzierende Wirkung der SGLT2-Inhibitoren und der GLP1-Analoga zu beachten. Auch sind bei zumeist klinisch relevantem β-Zell-Defizit Insulinsekretagoga (Sulfonylharnstoffe, Gliptine) häufig wenig wirksam.
Orale Diabetestherapie
Metformin ist wegen des niedrigen Hypoglykämierisikos auch bei hochbetagten Patienten zu empfehlen. Zu achten ist auf die gastrointestinalen Nebenwirkungen, die leichte Gewichtsabnahme und die abnehmende Nierenfunktion: Ab einem GFR von < 30 ml/min ist Metformin kontraindiziert, da das Risiko einer Laktatazidose steigt. Engmaschige Kontrollen der Nierenfunktion sind alle 3‒6 Monate obligat. Kontraindiziert ist Metformin weiters bei reduzierter Organfunktion von Leber und Herz. Der Vitamin-B12-Spiegel sollte in regelmäßigen Abständen kontrolliert werden, da Metformin die Vitamin-B12-Resorbtion hemmt.
SGLT-2-Hemmer (Gliflozine) weisen eine hohe Sicherheit in Bezug auf Hypoglykämien auf. Für Gliflozine zeigten sich zudem substanzspezifisch günstige Effekte auf das kardiovaskuläre Risiko, die Nephroprotektion sowie die Herzinsuffizienzentwicklung, in unterschiedlicher Weise belegt für Canagliflozin, Dapagliflozin und Empagliflozin. Bei eingeschränkter Nierenfunktionsleistung (GFF < 45 ml/min) dürfen laut aktueller Zulassung SGLT-2-Hemmer jedoch nicht mehr eingesetzt werden. Auch kann es in Einzelfällen durch den erhöhten Flüssigkeitsverlust zu Blutdruckabfall und akutem Nierenversagen kommen. Weiters treten genitale Pilzinfektionen gehäuft auf. Zu berücksichtigen ist auch die Gefahr einer euglykämischen Ketoazidose, ausgelöst beispielsweise durch Operationen oder Infektionen infolge eines relativen Insulinmangels. Glitazone (Pioglitazon) sind eine sinnvolle Option bei Patienten mit Insulinresistenz. Auch gibt es weder eine Einschränkung aufgrund der Nierenfunktion noch ein erhöhtes Hypoglykämierisiko. Eingeschränkt ist der Einsatz aufgrund einer Kontraindikation bei Herzinsuffizienz (NYHA I‒IV) und Ödemneigung sowie einer erhöhten Frakturrate bei postmenopausalen Frauen.
DPP-4-Hemmer sind für ältere Patienten eine gut verträgliche Medikamentengruppe, da kein erhöhtes Hypoglykämierisiko bei günstigem Nebenwirkungsprofil besteht. In großen Endpunktstudien zeigten sie Neutralität bezüglich kardiovaskulärer Komplikationen. Bis auf Linagliptin, das größtenteils über die Galle und den Darm ausgeschieden wird, muss die Dosis jedoch an die Nierenfunktion angepasst werden.
Sulfonylharnstoffe sollten aufgrund des Hypoglykämierisikos generell ab einer GFR < 30 ml/min vermieden werden. Bei schwerer Leberinsuffizienz werden diese aufgrund prolongierter Hypoglykämien ebenfalls nicht empfohlen. Gliclazid weist prinzipiell das geringste Hypoglykämierisiko auf.
α-Glukosidasehemmer (Acarbose) sind vorteilhaft aufgrund ihres niedrigen Hypoglykämierisikos sowie der wirkungsvollen Kontrolle einer postprandialen Hyperglykämie. Die Compliance einschränkend sind jedoch die notwendige präprandiale Einnahme mehrmals täglich sowie gastrointestinale Nebenwirkungen.
Subkutane Therapie
Für einzelne GLP-1-Analoga (Liraglutid, Semaglutid, Dulaglutid) konnte eine signifikant niedrigere Rate an kardiovaskulären Ereignissen in Studien nachgewiesen werden, weshalb sich die Substanzen besonders für diese Risikogruppe eignet. GLP-1-Analoga verursachen gelegentlich gastrointestinale Nebenwirkungen und führen zu einer deutlichen Gewichtsreduktion, die bei älteren Menschen nicht immer erwünscht ist. Zudem müssen sie derzeit subkutan verabreicht werden: Dafür sind ausreichender Visus sowie motorische und kognitive Fertigkeiten notwendig.
Insulintherapie ist indiziert, wenn das gesetzte Therapieziel trotz Ausschöpfung der genannten Therapieoptionen nicht erreicht werden kann. Bei geriatrischen Patienten ist zur Testung der kognitiven und motorischen Funktion ein Uhren- oder Geldzähltest vor Einschulung auf eine Insulintherapie zu erwägen. Es ist zu beachten, dass die Hypoglykämiewahrnehmung bei älteren Menschen reduziert ist und die gegenregulatorischen Mechanismen weniger wirksam sind. Empfehlenswert ist ein möglichst einfaches Insulinregime, wie zum Beispiel die basalunterstützte orale Therapie (BOT): Ein langwirksames Insulin beziehungsweise Insulinanalogon ergänzt die orale antidiabetische Therapie. Bei Nichterreichen des Therapieziels kann auf eine Mischinsulintherapie erweitert werden. Ein niedriger Anteil
an rasch wirksamem Insulin (30/70, 25/75) ist dabei zu bevorzugen, da im geriatrischen Setting Mahlzeiten oft nicht vollständig eingenommen werden.