Volkskrankheit Osteoporose
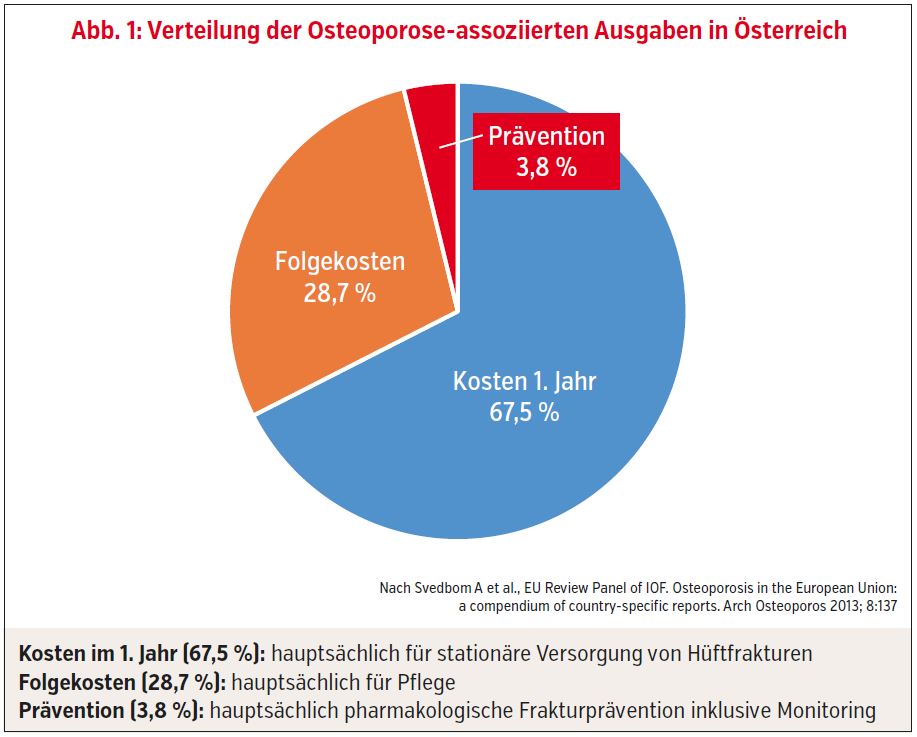
Weltweit erleiden durchschnittlich jede dritte Frau und jeder fünfte Mann im Laufe ihres Lebens eine Fragilitätsfraktur (Frakturen, die ohne adäquates Trauma auftreten). Laut einem Bericht der Europäischen Union (EU), in dem die durch Osteoporose verursachten Kosten der EU-Länder verglichen wurden, lag Österreich im Spitzenfeld – sowohl was die Frakturfrequenz als auch was die Kosten betrifft. Hierzu-lande betrugen im Jahr 2010 die direkten, durch Osteoporose verursachten Kosten circa 800 Millionen Euro; extrapoliert für 2018 sind das circa 900 Millionen Euro pro Jahr. Davon wurden mehr als ⅔ , nämlich 67,5 %, im 1. Jahr nach einer Fragilitätsfraktur (hauptsächlich für die stationäre Versorgung von Hüftfrakturen), 28,7 % für Folgekosten (hauptsächlich für die Pflege), aber nur 3,8 % für die Prävention (hauptsächlich für pharmakologische Frakturprävention und deren Monitoring), aufgewendet (Abb. 1).
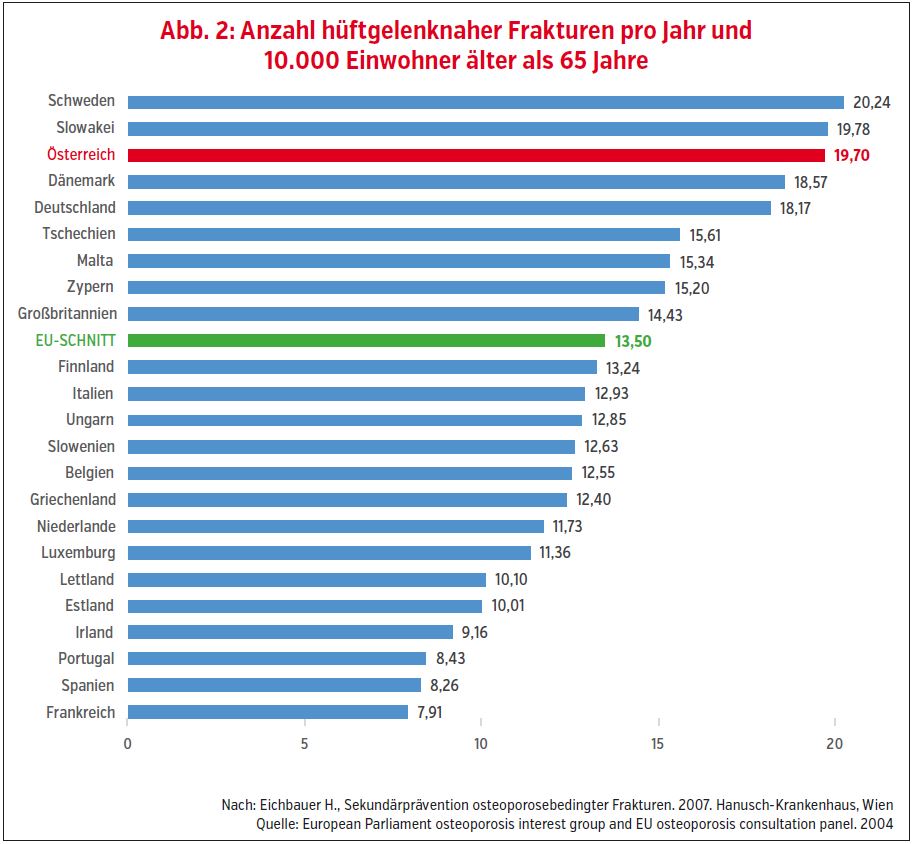
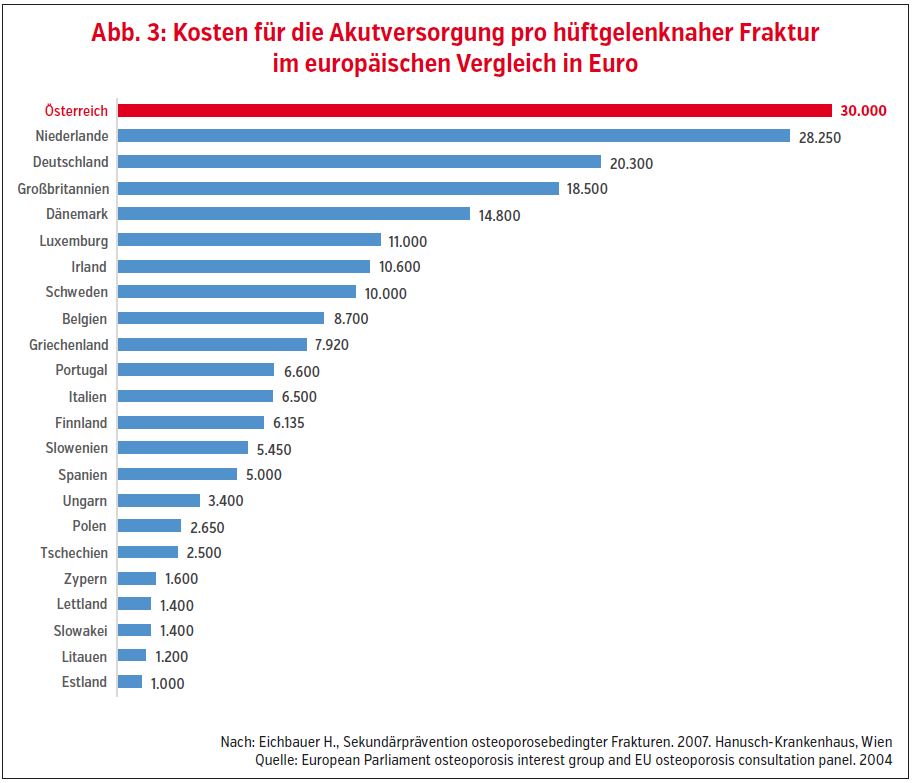
Österreich hat nicht nur eine der höchsten Hüftfrakturraten der EU (Abb. 2), sondern ist auch, laut einem aus Mitteln des Hauptverbandes der österreichischen Sozialversicherungsträger geförderten Projekt, das teuerste aller EU-Länder für die stationäre Versorgung dieser Frakturen (Abb. 3).
Deshalb haben die Autoren des EU- Berichtes den dringenden Appell an die Verantwortlichen in der Gesundheitspolitik gerichtet, geeignete strukturpolitische Maßnahmen zur Verbesserung der ineffizienten Versorgung betroffener Patienten zu treffen.
Da von politischer Seite die dafür notwendigen Maßnahmen bis heute verhindert werden, bleibt es dem Engagement des einzelnen an der Osteologie interessierten Arztes überlassen, zu einer Verbesserung der Versorgung beizutragen; ein Tropfen auf den heißen Stein!
Knochendichte allein ist schlechter Prädiktor
In Wien kann man heute zwar „an jedem Eck“ die Knochendichte messen lassen, eine qualitativ verbesserte Versorgung der Bevölkerung wurde dadurch aber nicht erreicht. Stattdessen wurde eine Situation geschaffen, in der viele Ärzte ohne osteologische Ausbildung sich dazu verleiten lassen, Therapieentscheidungen einzig aufgrund von Knochendichtewerten zu treffen. Das führt dazu, dass geschätzte ⅔ der Patientinnen, die eine spezifische Osteoporosetherapie erhalten, diese nicht benötigen, während etwa ¾, die eine solche Therapie benötigen, sie nicht erhalten!
Zur Risikoeinschätzung für Fragilitätsfrakturen sind die Resultate von Knochendichtemessungen keinesfalls ausreichend. Untersuchungen aus den USA haben gezeigt, dass nur 6,4 % aller post menopausalen Frauen, die im ersten Jahr nach einer Knochendichtemessung eine solche Fraktur erlitten hatten, T-Scores von ≤ –2,5 aufgewiesen hatten; das heißt, 93,6 % hatten laut WHO-Definition keine Osteoporose, sondern eine Osteopenie oder normale Knochendichtewerte. Dies waren mehrheitlich Frauen im Alter zwischen 40 und 65 Jahren. Unsere im Jahr 2017 im Ambulatorium KLIMAX ausgewerteten Daten von 100.000 Patientinnen zeigten, dass 67 % der Frauen mit nicht-vertebralen Frakturen unter 65 Jahre alt waren. Der Großteil der Fragilitätsfrakturen trat bei osteopenischen oder normalen Knochendichtewerten auf.
Wie identifiziert man nun jene Patienten, die ein hohes Frakturrisiko haben?
Zunächst gilt es, aus dem Wust anamnestischer Informationen, klinischer Risikofaktoren und sekundärer Ursachen der Osteoporose zielorientiert die weiteren diagnostischen Maßnahmen zu veranlassen. Dabei können computergestützte Programme zur Risikoberechnung, zum Bei-spiel FRAX®, und diverse sich aus obigen Informationen ergebende osteologische Laborparameter hilfreich sein.
Die Laboruntersuchungen sollen situationsabhängig Parameter des Knochenstoffwechsels wie Kalzium, Phosphat, Parathormon, alkalische Phosphatase, Vitamin D und zumindest einen Knochenumbaumarker, zum Beispiel CTX-Crosslaps, beinhalten; außerdem sollen die Nierenfunktion mittels Kreatininspiegels und glomerulärer Filtrationrate (cave: Bisphosphonate und reduzierte Nierenfunk tion!), die Schilddrüsenfunktion mittels TSH und freiem T4 und, bei Bedarf, die Sexualhormone FSH, Estradiol (E2) und Progesteron (P4), sowohl vor Therapiebeginn als auch zum Monitoring, geprüft werden; auch Parameter des Zuckerstoffwechsels (Nüchtern-BZ, HbA1c), Entzündungsparameter und Leberwerte sollen im Bedarfsfall bestimmt werden. Insgesamt ist bei den Laborwerten, abhängig von eventuell bestehenden Grunderkrankungen, Funktionsstörungen und Medikamenten, Flexibilität erforderlich.
Die physikalische Untersuchung und die Knochendichtemessung können einen Hinweis auf das Vorliegen von Wirbelkörperfrakturen geben. Besteht ein entspre-chender Verdacht, soll ein Röntgen der gesamten Wirbelsäule (anterior-posterior und seitlich), am besten mit der standardisierten semiquantitativen Graduierung der höhenreduzierten Wirbel nach Genant, durchgeführt werden. Die Wirbelkörper können im anterioren (am häufigsten), medianen oder posterioren Bereich einbrechen. Wirbelkörper mit einer Höhenreduktionen von < 20 % werden als Grad 0, von 20 bis 25 % als Grad 1, von 25 bis 40 % als Grad 2 und von > 40 % als Grad 3 definiert.
Die Knochendichte soll mit Dual-X-Ray-Absorptiometrie-(DXA-)Geräten gemessen und die Befunde sollen hinsichtlich lagerungsbedingter Darstellung und Analyse kritisch beurteilt werden. Bei guter Beurteilbarkeit eignen sie sich, neben ihrem Einfluss auf die Diagnose, auch als Dokumente der Verlaufskontrolle für Patienten mit und ohne medikamentöse Therapie (Monitoring). Die Aussagekraft der Befunde kann durch eine zusätzliche Analyse der ebenfalls mit DXA gemessenen Körperzusammensetzung (Body Composition, BC) erhöht werden. Der Muskelschwund (Sarkopenie), aber auch eine nur geringfügig reduzierte Muskel-masse, am besten gemeinsam mit der Ganggeschwindigkeit beurteilt, sind zusätzliche Risikofaktoren. Muskulatur und Skelett sind direkt voneinander abhängige Teile des muskuloskelettalen Systems. Die Kombination von Sarkopenie und Osteoporose wird deshalb auch als Sarkoosteoporose bezeichnet. Letztere ist auch oft mit Übergewicht oder Adipositas und ei-ner eingeschränkten Mobilität vergesellschaftet. Dieses „Dysmobilitätssyndrom“ gilt als unabhängiger Prädiktionsfaktor für Fragilitätsfrakturen.
Therapie und primäre Frakturprävention
Eine sinnvolle nichtmedikamentöse therapeutische Maßnahme ist das Krafttraining, denn: Muskelaufbau reduziert Knochenabbau! Die Substitution mit Vitamin D beziehungsweise Kalzium-Vitamin-D-Präparaten ist in unseren Breiten grundsätzlich zu empfehlen. Beides gilt sowohl im Rahmen der Prävention, ob als singuläre Maßnahme ohne weitere Therapie oder begleitend zu einer Hormonsubstitution, als auch in Kombination mit einer knochenspezifischen medikamentösen Therapie.
Eine hauptsächlich zur primären Frakturprävention geeignete pharmakologische Maßnahme ist die Hormonersatztherapie (menopausale Hormontherapie, MHT). Richtig angewendet, überwiegt ihr Nutzen bei Weitem das Risiko, wie sämtlichen international gültigen Leitlinien der Fachgesellschaften zu entnehmen ist. Die natürlichen, körperidenten Hormone Estradiol (E2), am besten morgens transdermal als Gel, und Progesteron (P4) – nicht aber synthetische Gestagene –, abends oral verabreicht, sind auch bei längerer als 5-jähriger Anwendungsdauer nicht mit einem erhöhten Risiko für Brustkrebs, venöse Thromboembolien, Herzinfarkt und Schlaganfall assoziiert. Es konnte im Gegenteil mit E2 plus P4 eine kardioprotektive Wirkung nachgewiesen werden, wenn die Therapie innerhalb der ersten 6 Jahre postmenopausal begonnen wurde. Prinzipiell soll eine MHT nicht später als 10 Jah-re nach der Menopause initiiert werden (Window of Opportunity). Die osteoprotektive Potenz der Hormonsubstitution konnte in zahlreichen Studien nachgewiesen werden und wurde unter anderem anschaulich demonstriert, als infolge des massenhaften Absetzens nach Publikation der Daten der Women’s Health Initiative (WHI) im Jahre 2002 das Risiko für Hüftfrakturen gegenüber jenen Patientinnen, die ihre MHT weiter anwendeten, um 55 % anstieg. Das war umso bemerkenswerter, als in diesem Zeitraum die Zahl der Bisphosphonat-Verschreibungen von 8 % auf 23 % zunahm.
Orale Bisphosphonate, wie Alendronat und Risedronat, sind trotz ihrer geringen Wirksamkeit und häufigen gastrointestinalen Nebenwirkungen noch immer die am meisten verordneten Osteoporosemedikamente. Allerdings nehmen nach einem Jahr nur noch 30 % und nach 5 Jahren sogar nur noch 9 % das jeweilige Präparat (niedrige Persistenz). Intravenöse Bisphosphonate, wie Ibandronat (vier-mal jährlich) und Zoledronat (einmal jährlich), sind zwar deutlich besser wirk-sam und haben höhere Persistenzraten, jedoch kommt es auch hier bei etwa 1/3 der Patientinnen zu teils starken Neben-wirkungen. Typisch sind die bei Zoledronat auftretenden grippeähnlichen „Postinfusionssymptome“, wie Fieber, Myalgie, Arthralgie und Kopfschmerzen.
Ganz anders verhält es sich mit dem 2010 zugelassenen monoklonalen RANKL-Antikörper Denosumab. Aufgrund des von den Bisphosphonaten völlig verschiedenen Wirkmechanismus – Denosumab imitiert die Wirkungen des körpereigenen Osteoprotegerins – treten kaum Nebenwirkungen auf. Diese gute Verträglichkeit bei gleichzeitig hoher Effizienz und die einfache subkutane Verabreichung (zweimal jährlich) führt, wie eine Analyse unserer Daten aus 2015 zeigt, zu einer Persistenz von 81 % nach 2 Jahren. Vorläufige Ergebnisse einer derzeit laufenden Auswertung von > 900 Patienten, die derzeit in unserem Ambulatorium mit Denosumab betreut werden, bestätigen diese hohe Persistenzrate; sie liegt nach 6 Jahren immer noch zwischen 75 % und 80 %. Die MHT, Bisphosphonate und Denosumab sind antiresorptive Therapien, das heißt, sie reduzieren primär den Knochenabbau. In der Folge führen sie, bei zwar ebenfalls, aber geringer reduziertem Knochenanbau, zu einem Anstieg der Knochendichte und einer Senkung der Frakturrate.
Sekundäre Frakturprävention
Denosumab und Bisphosphonate werden auch zur sekundären Frakturprävention, also bei bereits bestehenden Frakturen, eingesetzt. Die einzige derzeit in Öster-reich zugelassene anabole (den Aufbau der Knochenmatrix fördernde) Substanz, Teriparatid, wird ausschließlich in der Sekundärprävention verwendet.
Die sekundäre Frakturprävention in Österreich gibt ein jämmerliches Bild ab: Weniger als 20 % der Patienten erhalten nach der chirurgischen Versorgung ihrer Fragilitätsfrakturen eine Osteoporosetherapie. Das ist ein schweres Versäumnis der zuständigen Gesundheitspolitiker, die nicht in der Lage beziehungsweise nicht willens sind, den betroffenen Patienten eine adäquate Betreuung zu ermöglichen. Menschen, die bereits eine Fragilitätsfraktur erlitten haben, sind Hochrisikopatienten. Sie müssen medikamentös behandelt werden, denn die erste Fraktur verdoppelt das Risiko für weitere Frakturen. Deshalb sollte, als wichtigste politische Maßnahme, endlich ein flächendeckendes „Fracture Liaison Service“ (FLS) etabliert wer-den, das die Patientinnen und Patienten nach der Erstversorgung auffängt und sie in osteologische Zentren mit den notwendigen diagnostischen und therapeutischen Kapazitäten weiterleitet.
Die Implementierung eines derartigen FLS würde über eine deutliche Reduktion zukünftiger Frakturen nicht nur den Betroffenen unermesslich viel Leid ersparen, sondern auch zu einer für das Gesundheitsbudget substanziellen Kostenreduktion in der Höhe dreistelliger Millionenbeträge führen.