Die bisherige Problematik
In Österreich ist das Bronchialkarzinom unter allen malignen Erkrankungen nach wie vor diejenige mit der höchsten Mortalität. Insgesamt zeigte die Entwicklung der letzten Jahre annährend stabile Neuerkrankungszahlen bei relativ gleichbleibend hohen Sterbezahlen (2020: 4.985 Neuerkrankungen und 4.053 Todesfälle).1 Diese nichtzufriedenstellende Situation ergibt sich einerseits aus der späten Diagnosestellung aufgrund einer oftmals lange bestehenden Symptomfreiheit – weit über zwei Drittel aller Bronchialkarzinome werden erst in fortgeschrittenen Stadien erkannt – und andererseits aus den bislang limitierten Therapieoptionen in ebendiesen Situationen. Es gibt daher Bestrebungen, die Früherkennung durch Thorax-CT-basierte Screeningmodelle, die in Studien einen Vorteil in Hinsicht auf die Mortalitätsreduktion zeigen konnten, zu verbessern.2 Der Entwicklungsprozess ist allerdings aufgrund der Komplexität der Zielgruppendefinition und aufgrund der Schwierigkeiten einer breiten Etablierung noch nicht abgeschlossen.3 Während das Screening noch nicht praxistauglich wurde, gibt es auf der therapeutischen Seite jedoch bereits bedeutende Veränderungen.
Immuntherapien
In der Therapie des fortgeschrittenen Bronchialkarzinoms waren die letzten Jahre von einem grundlegenden Wandel des Behandlungskonzepts geprägt. Durch die zunehmende Etablierung der Immuncheckpoint-Inhibitoren wurden mittlerweile sowohl beim kleinzelligen (SCLC) als auch beim nichtkleinzelligen (NSCLC) Bronchialkarzinom teilweise sehr gute Therapiefortschritte erzielt.
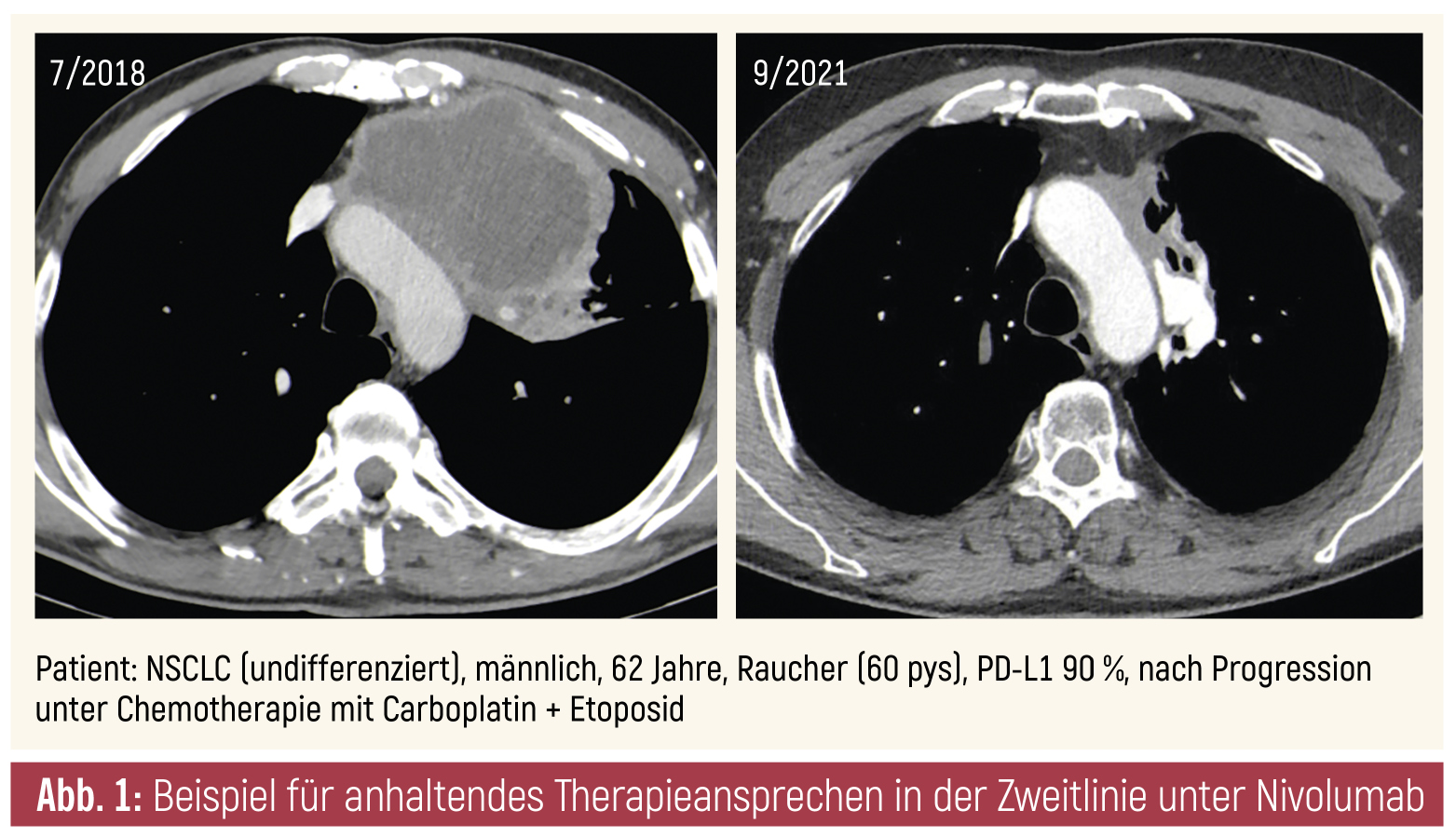
Das Grundprinzip: Immuncheckpoints – wie der PD-1-/PD-L1-Signalweg – sind Oberflächenrezeptoren an Immunzellen bzw. T-Lymphozyten (PD-1), welche die körpereigene Immunantwort modulieren. Bei Tumorzellen kann es zu einer Hochregulierung von Liganden (PD-L1) kommen, welche die Aktivierung des Immunsystems blockieren und so zu einer Toleranz gegenüber Tumorzellen führen (Immunevasion). Solche Signalwege können als Angriffsziele von Tumortherapien genutzt und gezielt mit Antikörpern blockiert werden. Beginnend ab 2015, als die PD-1-Inhibitoren Nivolumab (Abb. 1) und später Pembrolizumab als NSCLC-Zweitlinientherapie zugelassen wurden, begann eine sukzessive Erweiterung der Indikationen für die Immuntherapien. Besonders erwähnenswert ist die Publikation von drei Studien (KEYNOTE-189/-407 und PACIFIC) im Jahr 2018, die den Therapiestandard für fortgeschrittene Stadien des NSCLC neu definierten.
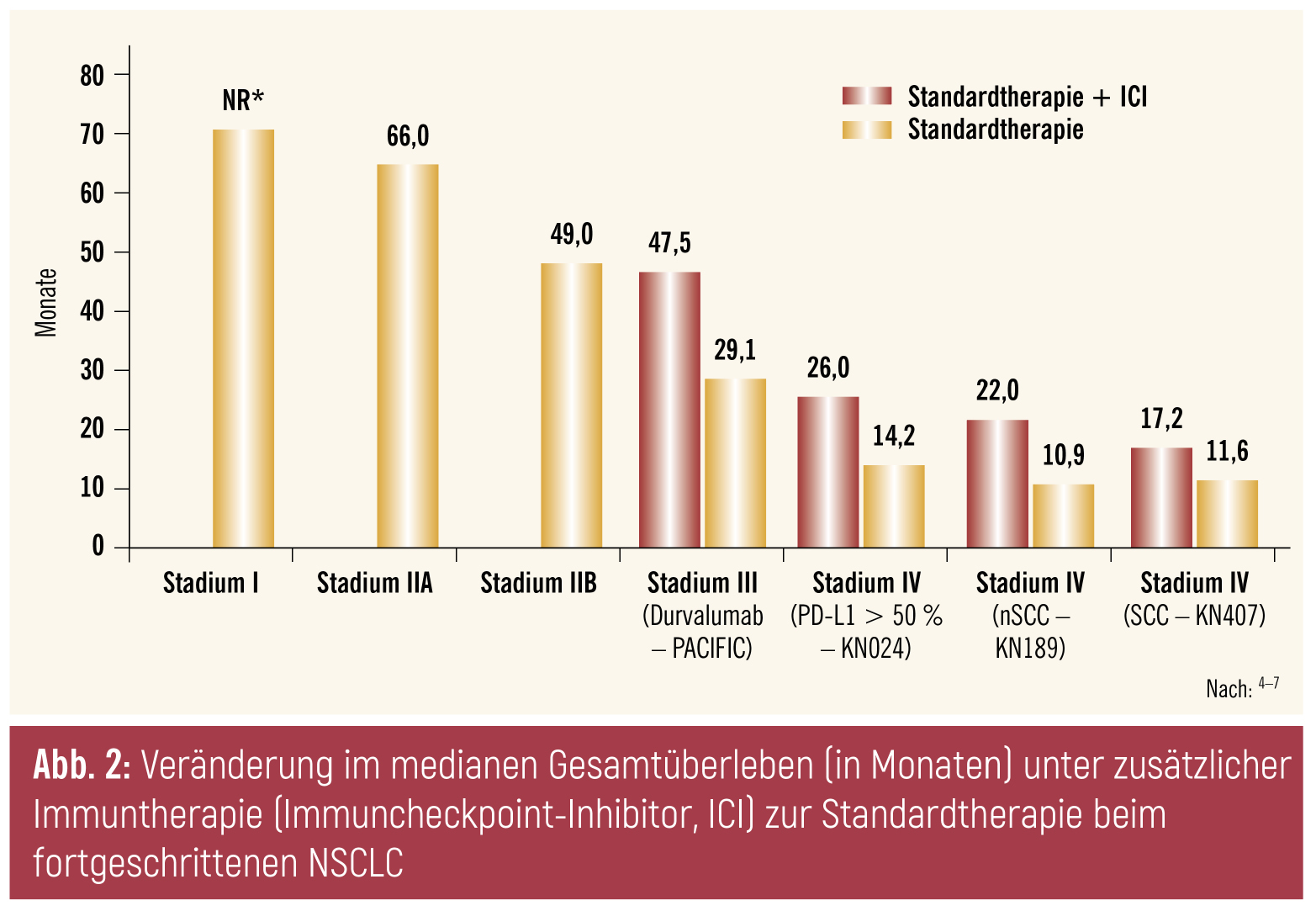
In den KEYNOTE-Studien konnte das mediane Überleben durch die Zugabe von Pembrolizumab zur bisherigen platinbasierten Standardchemotherapie beim Adenokarzinom um knapp 12 Monate (22,0 vs. 10,6 Monate)4 und beim Plattenepithelkarzinom um etwa 6 Monate (17,2 vs. 11,6 Monate)5 verlängert werden (Abb. 2). Mittlerweile besteht zunehmend das Bestreben, gänzlich auf konventionelle Chemotherapien zu verzichten, in den meisten Fällen ist dies derzeit allerdings noch nicht möglich. Jedoch erwies sich in Studien, dass bei hoher Expression des PD-L1-Biomarkers eine alleinige Immuntherapie als Alternative zu einer Kombinationstherapie möglich ist6 und man damit bei einem Teil der PatientInnen die Nachteile und Risiken einer Chemotherapie oftmals lange hinauszögern kann.
Nebenwirkungen: Durch die neuen Therapieoptionen müssen nun allerdings auch zusätzliche Nebenwirkungen im klinischen Alltag beachtet werden. Diese sind von jenen einer Chemotherapie in ihrem Entstehungsmechanismus grundlegend zu unterscheiden. Während zytostatische Chemotherapien die Zellteilung unterbinden und sich damit viele Effekte erklären lassen, kann es bei systemischer Blockade mit Immuncheckpoint-Inhibitoren zu einer Überaktivierung des Immunsystems mit Autoimmunreaktionen kommen. Es können dabei verschiedenste Organe betroffen sein, am häufigsten sind Störungen der Schilddrüsenfunktion, Hautausschläge und entzündliche Darmveränderungen zu beobachten. Selten, aber sehr problematisch, ist das Auftreten einer Pneumonitis, die ein rasches Erkennen und eine umgehende Therapie – in der Regel eine vorübergehende Verabreichung von Kortison – erforderlich macht. In den meisten Fällen sind die immuntherapieassoziierten Nebenwirkungen allerdings nicht therapielimitierend und weitgehend gut beherrschbar. Da sie allerdings auch zeitlich verzögert auftreten und sich auch mit jenen einer Chemotherapie überschneiden können, die therapeutische Konsequenz dann jedoch eine gänzlich andere ist, besteht weiterhin die Notwendigkeit regelmäßiger klinischer Kontrollen aller PatientInnen mit Immuntherapien.
Zielgerichtete Therapien
Ein gänzlicher anderer Ansatz wird mit gezielten Tumortherapien versucht. Darunter werden im Allgemeinen Inhibitoren von Wachstumsrezeptoren bzw. Tyrosinkinase-Inhibitoren (TKI) verstanden. Diese können als „small molecules“ gezielt Wachstumssignalwege von Tumorzellen blockieren. Dazu ist es allerdings erforderlich, dass strukturell veränderte Wachstumssignalrezeptoren – oder auch Treibermutationen genannt – überhaupt von Tumorzellen exprimiert werden. Therapierbare Angriffspunkte gibt es leider bislang nur bei einem geringen Teil der PatientInnen, und bei Weitem haben nicht alle potenziellen Rezeptormutationen zugelassene therapeutische Möglichkeiten. Auch das Auffinden von Treibermutationen bringt große diagnostische Herausforderungen mit sich. Daher wird mittlerweile die Tumor-DNA-Sequenzierung durch Next Generation Sequencing (NGS) immer mehr zu einer tragenden Säule in der Diagnostik.
Die wichtigsten TKI sind die Inhibitoren des EGF-Rezeptors, wie z. B. Afatinib oder Osimertinib, bzw. jene des ALK-Rezeptors, wie z. B. Alectinib, Brigatinib oder Lorlatinib. Diese sind mittlerweile auch schon in mehreren Generationen verfügbar und ermöglichen damit auch unter Umständen sequenzierte Therapiepfade, sodass ein Zurückgreifen auf Chemotherapien lange vermieden werden kann. Durch die Tatsache, dass diese Therapien sehr spezifisch auf Angriffspunkte an Tumorzellen zugeschnitten sind, werden sie in der Regel von den PatientInnen auch gut vertragen und bieten damit eine hohe Lebensqualität unter der TKI-Therapie.
Fazit
Zusammenfassend kann man die Therapieoptionen bei fortgeschrittenen Tumorerkrankungen der Lunge im Vergleich zu anderen malignen Erkrankungen noch immer nicht als zufriedenstellend betrachten. Die Entwicklungen der letzten Jahre zeigen allerdings, dass das Bronchialkarzinom nun nicht mehr als gänzlich unbehandelbare Erkrankung angesehen werden darf. Mit neuen Therapiekonzepten konnte nun die Überlebenszeit für viele PatientInnen auch hier bei gleichzeitig guter Lebensqualität bzw. reduzierten therapieassoziierten Nebenwirkungen verbessert werden. In Zukunft sind aus der Vielzahl der derzeit laufenden Studien noch weitere Therapiefortschritte zu erwarten.
- Statistik Austria
- de Koning HJ et al., N Engl J Med 2020; 382(6):503–13
- Statement der Österreichischen Gesellschaft für Pneumologie (ÖGP) von 7. 2. 2020
- Gray J et al., J Thorac Oncol 2021; 16(Suppl 3):224
- Robinson AG et al., J Thorac Oncol 2021; 16(Suppl 4):748–749
- Reck M et al., J Clin Oncol 2021; 39(21):2339–49
- Faivre-Finn C et al., J Thorac Oncol 2021; 16(5):860–67