UIM 02|2021 Themenheft Biologika
Update 2021 – Asthma bronchiale: Antikörpertherapie und Studiendaten
Weltweit leiden mehr als 300 Millionen Patienten an Asthma bronchiale.1 Obwohl weniger als 20 % an schwer behandelbarem und weniger als 5 % an schwerem Asthma leiden, binden diese Patienten einen Großteil der Ressourcen.2, 3 Patienten mit schwer behandelbarem Asthma haben trotz Mittel- bis Hochdosis-ICS (inhalatives Kortikosteroid) + LABA (langwirksames Beta-2-Sympathomimetika) eine unzureichende Asthmakontrolle. Diese Patienten müssen gezielt auf Faktoren überprüft werden, welche eine optimale Asthmatherapie verhindern. Sehr häufig sind dies eine schlechte Therapieadhärenz (besonders bei ICS) sowie eine inadäquate Inhalationstechnik. Bei den meisten Patienten ist eine neuerliche Inhalationsschulung notwendig. Relevante Komorbiditäten (kardiovaskulär, Übergewicht, Schlafapnoe, chronische Rhinosinusitis, Reflux, Depression) müssen gezielt abgefragt und untersucht werden. Wenn trotz optimierter „Confounding factors” und bestmöglicher Behandlung von Komorbiditäten weiterhin keine adäquate Asthmakontrolle zu erreichen ist, kann die Diagnose schweres Asthma bronchiale gestellt werden.
T2-high- vs. T2-low-Asthma
Sowohl allergisches wie auch eosinophiles Asthma fallen in die Kategorie des Type-2-(T2-)high-Asthmas. Dieses ist nach der Freisetzung bestimmter Zelltypen benannt (Th2-Lymphozyten, Innate Lymphoid Cells [ILC2]), welche wiederum mit bestimmten Zytokinen (IL-4, IL-5, IL-13) assoziiert sind. Patienten mit Type-2-low-Asthma (z. B. Asthma bronchiale bei Adipositas, Asthmaformen mit verstärkter neutrophiler Entzündung) zeigen ein schlechtes Ansprechen auf eine Kortikosteroidtherapie, sowohl inhalativ (ICS) als auch systemisch (orales Kortikosteroid, OCS).4 In der Praxis ist es wichtig T2-high- von T2-low-Asthma zu unterscheiden, da derzeit nur für T2-high-Patienten Biologicals zur Verfügung stehen. Parameter zur Identifikation von T2-high-Asthmatikern sind Anamnese (Zeitpunkt des Krankheitsbeginns, Rhinosinusitis etc.), Eosinophile in Blut (150–400 Zellen/μl) sowie Sputum (> 2 %), Fractional excretion of Nitric Oxide (FeNO, > 20–50 ppb) sowie eine Allergiediagnostik.
Therapie
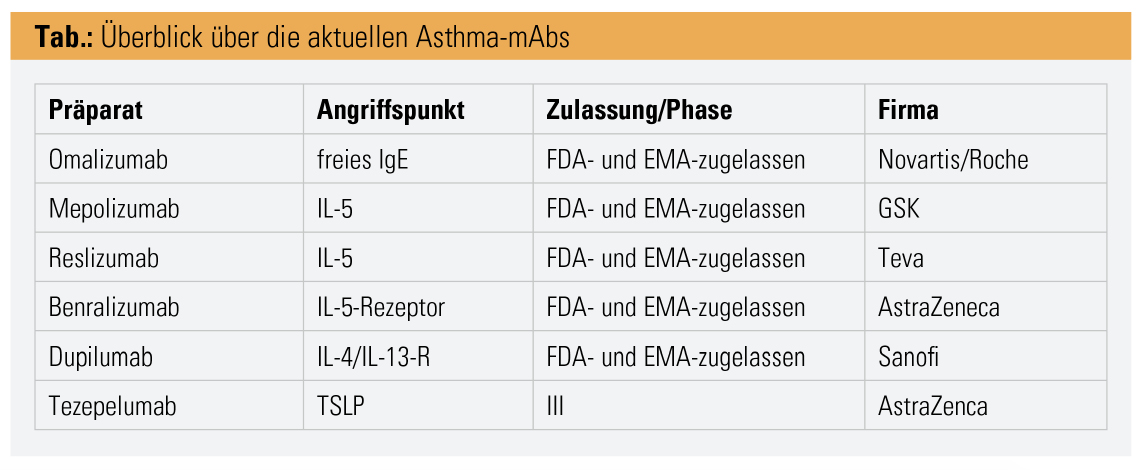
Die meisten und spannendsten Neuerungen in der Therapie des schweren Asthmas sind im Bereich der Antikörper zu finden. Dennoch ist auch bei diesen Patienten eine korrekt und konsequent durchgeführte inhalative Therapie als Grundpfeiler essenziell. Vor Therapiebeginn mit Biologicals sollten die konventionellen (und auch kostengünstigeren) Therapien ausgeschöpft werden. Dies inkludiert phänotypenunabhängig ab dem 6. Lebensjahr Tiotropium sowie eventuell Leukotrienrezeptorantagonisten. Letztere sind besonders beim Subtyp der AERD (Aspirin-exazerbierte Atemwegserkrankung) oft erfolgreich.5 Wenn auch mit dieser erweiterten Therapie keine Asthmakontrolle erzielt werden kann, muss der Patient auf ein Biologikum evaluiert werden. Derzeit sind zur Therapie des schweren Asthmas bronchiale fünf monoklonale Antikörper (mAB) zugelassen (Tab.). Omalizumab, welches freies IgE bindet sowie Mepolizumab, Reslizumab und Benralizumab, die mABs gegen IL-5 (Mepolizumab, Reslizumab) beziehungsweise den IL-5-Rezeptor (Benralizumab) sind. Die letzteren drei mAB führen zu einer Reduktion der Eosinophilie und deutlichen klinischen Verbesserungen bei Patienten mit schwerem eosinophilem Asthma.
T2-high
Omalizumab ist seit 2005 in Europa zugelassen und wird Gesamt-IgE-Spiegel- sowie körpergewichtsabhängig alle zwei oder vier Wochen subkutan verabreicht. Voraussetzung ist ein schweres allergisches Asthma mit einer nachgewiesenen Allergie gegen ein ganzjähriges Aeroallergen. Es ist ab dem 6. Lebensjahr zugelassen. Real-Life-Studien über bis zu 9 Jahre konnten langfristige Therapieerfolge zeigen.6
Mepolizumab wird alle vier Wochen in einer fixen Dosis (40 mg von 6 bis 11 Jahren, 100 mg ab dem 12. Lebensjahr) subkutan verabreicht. Die großen Zulassungsstudien SIRIUS, MENSA und MUSCA konnten bei Patienten mit Blut-Eosinophilen > 300 Zellen/μl eine signifikante Reduktion der Exazerbationsrate, der OCS-Dosis sowie eine Verbesserung der Asthmakontrolle (ACQ5) zeigen. Die Lungenfunktion (FEV1) war statistisch, aber nicht klinisch signifikant gebessert.7–9 Eine gepoolte Analyse von Open-label-Extensions dieser Studien zeigte ein Anhalten dieses Therapieerfolges über bis zu 3 Jahre.
Reslizumab ist für erwachsene Patienten zugelassen und wird alle vier Wochen körpergewichtsdosiert (3 mg/kg KG) intravenös verabreicht. In den zwei Zulassungsstudien konnten bei Patienten mit Blut-Eosinophilen von > 400 Zellen/μl statistisch und klinisch signifikante Verbesserungen der Exazerbationsrate, der Asthmakontrolle (ACQ7) sowie der Lungenfunktion (FEV1) gezeigt werden.10 Auch für Reslizumab gibt es Open-label-extension-Daten welche ein Beibehalten des Therapieerfolges bis zu 3 Jahren zeigen können.11 Eine 2018 im „Blue Journal“ publizierte Studie zeigte signifikante Verbesserungen von FEV1 und ACQ5 unter Reslizumab bei Patienten mit inadäquater Asthmakontrolle unter Mepolizumab.12 Limitierend ist die kleine Fallzahl (n = 10) und dass die genannten klinischen Parameter sekundäre Endpunkte waren. Die i. v. Applikation ist in der Praxis etwas zeitaufwändiger, die körpergewichtsabhängige Dosierung könnte jedoch bei adipösen Patienten von Vorteil sein.
Benralizumab führt über den IL-5-Rezeptor alpha zur zellmediierten Zytotoxizität und wird s. c. alle vier Wochen und ab der dritten Gabe alle acht Wochen verabreicht. Benralizumab hat damit das längste Dosierintervall der bisher zugelassenen Asthma-mAbs. Zwei Phase-3-Studien, SCIROCCO und CALIMA, haben bei schweren Asthmatikern mit einer Blut-Eosinophilie von > 300 Zellen/μl eine statistisch sowie klinisch signifikante Reduktion der Exazerbationsrate (primärer Endpunkt) sowie der Asthma-Kontrolle und Lungenfunktion zeigen können.13, 14 Die ZONDA-Studie zeigte 75 % Reduktion der OCS-Dosis.15 Eine Open-label-extension-Studie konnte ein Anhalten dieser Effekte über 2 Jahre zeigen.16 Insgesamt waren in den Benralizumab-Phase-III-Studien mehr als 3.000 Patienten eingeschlossen. Benralizumab führt im Gegensatz zu Mepolizumab zu einer beinahe vollständigen Depletion der Blut-Eosinophilen. Indirekte Vergleiche der Studiendaten zeigen auch leicht bessere Anstiege bei Asthmakontrolle und Lungenfunktion gegenüber Baseline. Direkte „Head-to-Head“-Vergleichsstudien gibt es jedoch nicht.
Dupilumab bindet an den IL-4-Rezeptor und hemmt damit die IL-4- und -13-Signalwege. In der Zulassungsstudie von Castro et al. hatten Patienten mit FeNO über 25 ppb geringere Exazerbationsraten und höhere FEV1-Zugewinne.17 Allerdings muss erwähnt werden, dass es sich hierbei um sekundäre Wirksamkeitsendpunkte handelte und der primäre Endpunkt (die Exazerbationsrate) abhängig von Eosinophilie war. Zugelassen ist Dupilumab ab dem 12. Lebensjahr für Patienten mit T2-high-Asthma (definiert als eosinophiles Signal und/oder erhöhtes FeNO). Eine weitere Zulassung hat Dupilumab bei erwachsenen Patienten mit mittelschwerer bis schwerer atopischer Dermatitis. Die Verabreichung erfolgt s. c. alle zwei Wochen, 300 mg für Patienten mit OCS-Therapie sowie Patienten mit schwerem Asthma und atopischer Dermatitis bzw. 200 mg bei allen anderen. Die erste Dosis ist jeweils doppelt. Dupilumab ist somit auch eine potenzielle Therapie für Patienten mit T2-high-Signalen, auch wenn die Verschreibungskriterien für die „klassischen“ Therapien bei schwerem allergischem Asthma (Omalizumab) und schwerem eosinophilem Asthma (Mepolizumab, Reslizumab und Benralizumab) nicht zutreffen. Alle bisher genannten Therapien zeigten bisher ein gutes Nebenwirkungsprofil. Bei einzelnen Dupilumab-Patienten kam es zu einer Hypereosinophilie, welche bei manchen zu einem Therapieabbruch führte.17
Real-World-Evidenz: Die meisten Neuerungen für zugelassene mAB-Therapien bei schwerem Asthma betreffen die Zunahme von solider Evidenz für Real-life-Effectiveness von Anti-IL5/IL-5R- sowie -IL4/IL13R-mABs. Randomisiert kontrollierte Studien, welche für die Zulassung von neuen Therapien notwendig sind, generieren Daten zur Wirksamkeit einer Therapie, meist im Vergleich zu Placebo, unter streng kontrollierten Bedingungen. In diesen Studien können Patienten mit Komorbiditäten meist nicht eingeschlossen werden. Weiters sind bei randomisiert kontrollierten Studien für Asthmatherapien ehemalige Raucher mit mehr als 10 Pack-years sowie Patienten mit fehlender Reversibilität nach GINA-Kriterien fast immer ausgeschlossen. In einer britischen Studie wurde gezeigt, dass weniger als 10 % der Patienten mit schwerem Asthma in solche Studien eingeschlossen werden können.18 Daher ist es wichtig nach erfolgreicher Zulassung Real-life-Effectiveness bei Patienten, welche die Therapie tatsächlich erhalten, nachzuweisen. Studien der Autoren dieses Beitrags konnten zeigen, dass die Real-life-Effectiveness von Mepolizumab, Reslizumab und Benralizumab bei österreichischen Patienten mit schwerem eosinophilem Asthma vergleichbar mit der Wirksamkeit in randomisiert kontrollierten Studien ist.19–21 Insbesondere die Real-life-Studie zu Benralizumab konnte eine sehr rasche Verbesserung von Asthmakontrolle und Lungenfunktion innerhalb der ersten Wochen zeigen.21 Diese klinische Verbesserung war in Subgruppenanalysen ident bei Patientengruppen, welche aufgrund von Raucheranamnese (ehemalige Raucher, > 10 Pack-years) oder fehlender Reversibilität nicht in randomisiert kontrollierten Studien untersucht wurden. Für diese Patientengruppen konnte überhaupt erstmalig ein Therapieeffekt nachgewiesen werden.21 In einer französischen Real-life-Studie wurde die Wirksamkeit auch für Dupilumab nachgewiesen.22 Österreichische Daten dazu sind vergleichbar und wurden zur Publikation eingereicht.
Kontrollparameter: Parameter, welche bei allen mAb-Therapien regelmäßig kontrolliert werden müssen, sind Asthmakontrolle (z. B. Asthma Control Test und/oder Asthma Control Questionnaire), Lungenfunktion und, falls vorhanden, die OCS-Dosis. Nach einer Therapiedauer von 4 Monaten erfolgt die erste Reevaluierung. Bei sehr gutem Ansprechen (z. B. sofortige Verbesserung von Asthmakontrolle oder Lungenfunktion über der „minimal clinically important difference“) wird die Therapie fortgeführt.
Patienten mit einer „intermediate response“ (z. B. Verbesserung von Asthmakontrolle oder Lungenfunktion, jedoch klinisch nicht eindeutig relevant) wird das Präparat initial für 12 Monate weiter verabreicht. Bei ausbleibendem Ansprechen muss die Therapie geändert werden. Die Indikationsstellung, Erstverabreichung und Überprüfung des Therapie-Ansprechens sollen in spezialisierten Zentren erfolgen.
T2-low
Deutlich schlechter sind die Therapieoptionen beim schweren T2-low-Asthma. Eine langfristige Off-label-Therapie mit Azithromycin 500 mg 3-mal pro Woche kann unter Berücksichtigung des Nebenwirkungsprofils versucht werden und hat bei neutrophilem Asthma gute Erfolge gezeigt.23
COVID-19 und Asthma
Entgegen unbegründeten Gerüchten zu Anfang der COVID-19-Pandemie gibt es keine Evidenz, dass Patienten mit schwerem Asthma unter einer Antikörpertherapie (mABs gegen IL-5 bzw. IL-5-R) ein erhöhtes Risiko für eine Infektion mit SARS-CoV-2 und für einen schweren Verlauf haben. Im Gegenteil, höchstwahrscheinlich hat die verbesserte Asthmakontrolle durch diese mAB-Therapie einen protektiven Effekt. Da es hierzu noch keine größeren Datenanalysen gibt, stammt die Evidenz primär aus Fallberichten. Die weltweit ersten zu diesem Thema publizierten Fälle sind von der Pneumologischen Abteilung des Krankenhauses Hietzing, Wien.24, 25
Conclusio
Es gibt eine zunehmende Anzahl an potenten Therapieoptionen für Patienten mit schwerem T2-high-Asthma. Bevor jedoch eine mAb-Therapie gestartet wird, müssen die „Basics“ stimmen: Die Diagnose muss genau überprüft werden, die Basistherapie muss korrekt und konsequent eingenommen werden, und Confounding Factors müssen so gut wie möglich behandelt werden.
- To T et al., BMC Public Healt 2012; 12:204
- Hekking PP et al., J Allergy Clin Immunol 2015; 35(4):896–902
- Sadatsafavi M et al., Can Respir J 2010; 17(2):74–80
- Buhl R et al., S2k-Leitlinie zur Diagnostik und Therapie von Patienten mit Asthma [Internet]. [cited 2018 Jan 20]. Available from: http://www.awmf.org/leitlinien
- Dahlén SE et al., Am J Respir Crit Care Med 2002; 165(1):9–14
- Colombo GL et al., Ther Adv Respir Dis 2019; 13:1753466619841350
- Chupp GL et al., Lancet Respir Med 2017; 5(5):390–400
- Ortega HG et al., N Engl J Med 2014; 371(13):1198–207
- Bel EH et al., N Engl J Med 2014; 371(13):1189–97
- Castro M et al., Lancet Resp Med 2015; 3(5):355–66
- Murphy K et al., J Allergy Clin Immunol Pract 2017; 5(6):1572–1581.e3
- Mukherjee M et al., Am J Respir Crit Care Med 2018; 197(1):38–46
- Bleecker ER et al., Lancet 2016; 388(10056):2115–27
- FitzGerald JM et al., Lancet 2016; 388(10056):2128–41
- Nair P et al., N Engl J Med 2017; 376(25):2448–58
- Busse WW et al., Lancet Respir Med 2019; 7(1):46–59
- Castro M et al., N Engl J Med 2018; 378(26):2486–249
- Brown T et al., Eur Respir J 2018; 52(6)
- Renner A et al., Pulm Pharmacol Ther 2020; 64:101946
- Marth K et al., Eur Respir J 2018; 52(suppl 62):OA3568
- Renner A et al., Allergy 2020; DOI: 10.1111/all.14441. Online ahead of print.
- Dupin C et al., Clin Exp Allergy 2020; 50(7):789–98
- Gibson PG et al., Lancet 2017; 390(10095):659–68
- Renner A at al., J Asthma 2020; DOI: 10.1080/02770903.2020.1781165. Online ahead of print.
- Renner A et al., ERJ Open Res 2020; 6(4):00457–2020