ECTRIMS 2012: Nuklearmedizin und MS !?
PET und Myelin-Imaging
2011 wurde eine erste Arbeit veröffentlicht, in der die In-vitro- und In-vivo-Markierung des Myelins mittels [11C]PIB (Pittsburgh Compound B) beschrieben wurde. PIB – ein Thioflavin-Derivat – ist vor 8 Jahren zur Markierung der Amyloid-Plaques unter Verwendung der PET (Positronen-Emissions-Tomographie) entwickelt worden; bis heute sind mehr als 200 Publikationen mit PIB-PET und dem Schwerpunkt Alzheimer-Demenz veröffentlicht worden.
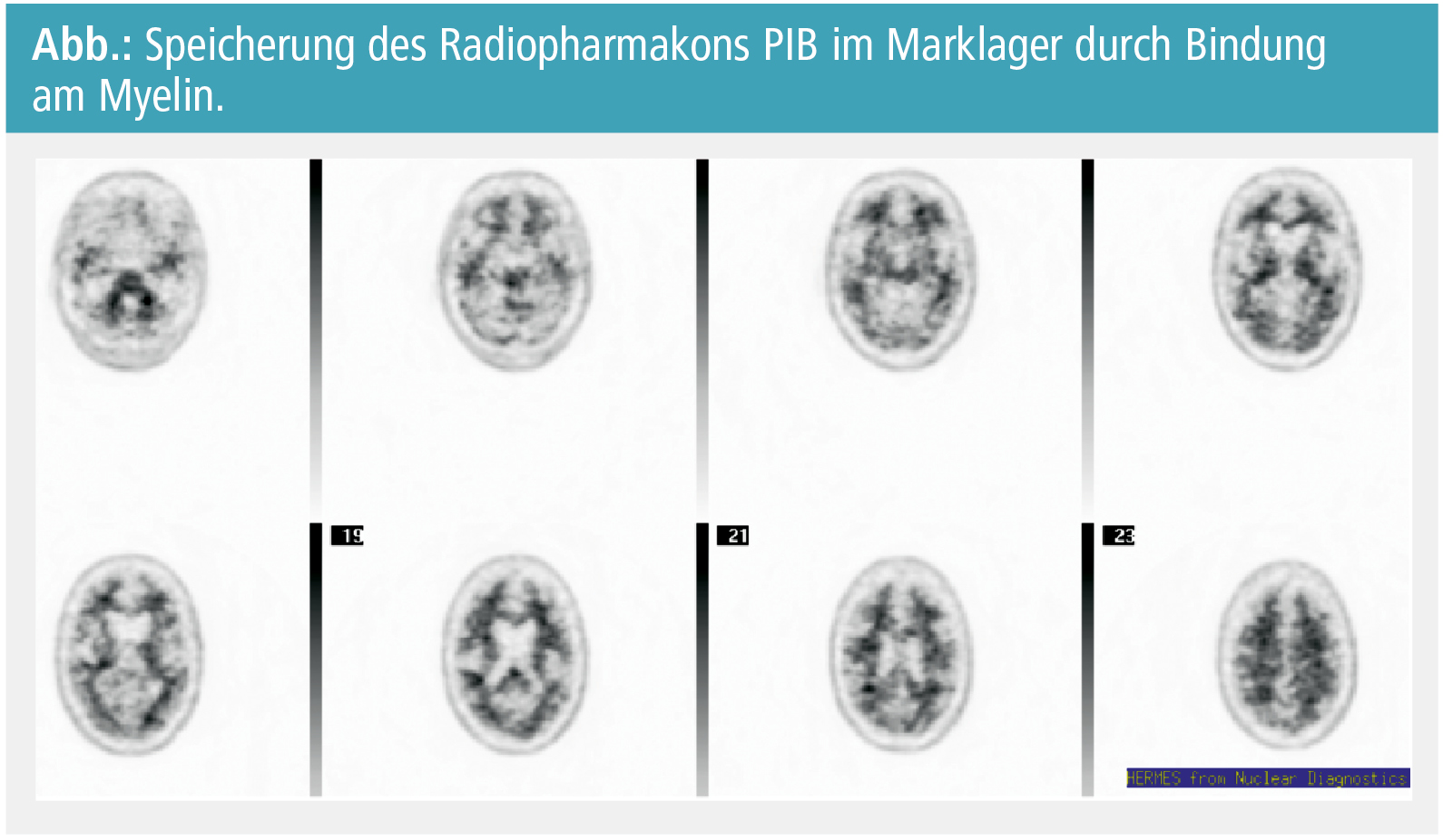
Ein gemeinsamer Nenner der Bindung an Amyloid-Peptid und am Myelin könnte die ß-Sheet-Struktur des Amyloid-Peptids und von Bestandteilen des normalen Myelins wie z. B. des MBP (Myelin Basic Protein) sein. In dieser ersten Arbeit von Stankoff et al. 2011 wurde gezeigt, dass PIB proportional zum vorhandenen Myelin im ZNS am Myelin bindet, wenn auch mit niedrigerer Affinität als am Amyloid-Plaque (Abb.). Und es stellte sich die Frage, ob auch demyelinisierte oder remyelinisierte Herde im Marklager von normal myelinisierten Bereichen zu unterscheiden wären.
Einschränkend für die PET-Technik ist die im Vergleich zur MRT eindeutig schlechtere Auflösung. Stankoff et al. konnten jedoch periventrikuläre, juxtakortikale und subkortikale Läsionen differenzieren.
In demyelinisierten Arealen im Marklager, die anhand der T2-gewichteten MRT-Aufnahmen definiert wurden, war die PIB-Aufnahme in unterschiedlichem Ausmaß reduziert; im Vergleich zur normal erscheinenden weißen Substanz (NAWM) fanden die AutorInnen im Mittel eine Reduktion um 22 %. In Gadolinium(Gd)-positiven Läsionen ergab sich gegenüber Gd-negativen Läsionen eine höhere PIB-Bindung; ursächlich dafür könnte eine noch unvollständige Demyelinisierung im Bereich der Gd-positiven Läsionen, aber auch entzündliche Reaktionen und eine Störung der Blut-Hirn-Schranke sein.
Am ECTRIMS 2012 wurde von B. Stankoff schließlich über eine Kohorte von MS-PatientInnen berichtet, die innerhalb eines Zeitraums von 10 Wochen zweimal mit PIB-PET untersucht wurden. Läsionen wurden anhand der MRT als aktiv oder inaktiv definiert. Im Zeitverlauf fand sich in 19 % der Läsionen (mehr aktive als inaktive) eine Abnahme des PIB-Uptake um > 10 % (im Mittel um 23 %); diese Veränderungen wurden einer Demyelinisierung zugeschrieben. 60 % der Läsionen waren im Untersuchungszeitraum stabil (inaktiv > aktiv), bei 21 % (aktive > inaktive) konnte eine Zunahme des PIB-Uptakes um > 10 % (im Mittel 17 %) aufgezeigt werden. Dieses Verhalten könnte einer Remyelinisierung entsprechen. Bezüglich des Ausmaßes der PIB-Bindung lag ein abnehmender Gradient zwischen NAWM, periläsioneller weißer Substanz und den MRT-Läsionen vor.
Bodini et al. präsentierten schließlich ein Poster, in dem ein Vergleich des PIB-Uptakes zwischen MS-Läsionen im Marklager, periläsionellem Marklager und der NAWM vorgenommen wurde. Zur Definition der Regionen wurde ein 3T-MR-Tomograph verwendet, die PET-Auflösung betrug 2,5 mm.
Die PIB-Bindung in den Marklagerläsionen war signifikant niedriger als in der NAWM (–15 %), ebenso periläsionell im Vergleich zu NAWM (–6 %) und auch in der Läsion selber gegenüber der periläsionellen Region (–9 %).
PIB scheint die graduellen Unterschiede in der Myelin-Konzentration in vivo nachvollziehen zu können und scheint daher als Monitor für Demyelinisierung oder Myelin-Reparatur geeignet. Geplant ist in Zukunft ein Myelin-Mapping auf Voxel-Basis für Verlaufskontrollen.
PET und aktivierte Mikroglia
Als 2. Tracer wurde [11C]PK11195 vorgestellt. Dieses Radiopharmakon wurde bereits vor vielen Jahren in nuklearmedizinischen Kreisen eingeführt, damals noch als Ligand für den peripheren Benzodiazepinrezeptor und damit als Marker für aktivierte Mikroglia. Zwischenzeitlich spricht man vom TSPO, dem „translocator protein“ – ein makromolekularer Komplex, der von Mitochondrien exprimiert wird.
Es stellte sich die Frage, ob bei MS eine Darstellung der pathogenen Mikroglia möglich ist. Rissanen et al. untersuchten daher den Einsatz von [11C]PK11195 bei PatientInnen mit sekundär progredienter MS: Es ergab sich eine signifikant erhöhte Bindung des Radiopharmakons in der NAWM der PatientInnen, die eine Korrelation zur reduzierten FA (fraktionale Anisotropie) in der MRT zeigte. Zusätzlich war PK11195 auch vermehrt periläsionell in der NAWM abgelagert.
Entwicklungsmöglichkeiten für PET bei MS
Weitere Möglichkeiten des molekularen Imagings mittels PET wären die Untersuchung des neuronalen Schadens (mittels [11C]Flumazenil) oder der Astrogliose ([11C]D-Deprenyl), die Darstellung von Entzündung (z. B. mit Liganden für Sub-Sets von Entzündungszellen wie B-Lymphozyten oder für assoziierte Marker wie VCAM), von mitochondrialem oxidativem Stress ([62Cu]ASTM) oder Zelltod ([18F]ML-10) sowie Stammzellen – bis auf Flumazenil alles experimentelle, neue und innovative Vorhaben!
Fazit
Insgesamt stellen die vorgestellten Radiopharmaka PIB und PK11195 einen guten Ansatz zur Untersuchung pathologischer Prozesse bei der MS dar. Offen bleiben allerdings die Probleme der Quantifizierung der PET-Daten und die räumliche Auflösung der PET-Systeme. Auch ist ein verbreiterter Einsatz der PET-Technologie u. a. auch von der Verfügbarkeit des Nuklids abhängig: [11C] kann auf Grund der Halbwertszeit nur am Ort der Produktion (= Zyklotron) verwendet werden. Daher ist eine Markierung mit dem längerlebigen [18F] anzustreben. Für Verwandte des PIB ist dies bereits geschehen, für PK11195 sind diese Vorgaben noch in der Entwicklung. Sollten all diese Einschränkungen beherrscht werden, so würden auch die neuen kombinierten PET-MRT-Systeme mit der Untersuchung (wissenschaftlicher) Fragestellungen bei MS ein neues Aufgabengebiet erhalten.