DGHO–JAHRESTAGUNG 2018 | Interview mit H. Greinix
Univ.-Prof. Dr. Hildegard Greinix: In den Anfangsjahren wurden Versuche unternommen, die Dosis zu steigern, oder es wurden bewusst 3 Dosierungen verwendet. Es hat sich dann aber herausgestellt, dass durch das spezifische Design der CAR-T-Zellen mit der gezielten Antigenerkennung und der Eigenschaft dieser Zellen, sich in vivo innerhalb von etwa 2, 3 Tagen schon um das 1.000-Fache zu vermehren, dass dadurch wiederholte Infusionen nicht notwendig sind. Diese rapide Expansion mit einem Peak nach etwa einer Woche ist in frühen Studien nachgewiesen.
Chiara Bonini aus Mailand hat in ihren Arbeiten T memory stem cells untersucht und konnte nachweisen, dass solche Zellen aus dem Produkt 15 und mehr Jahre im Patienten persistieren, während alle anderen Zellpopulationen eine kürzere Lebensdauer haben. Diese Daten haben Einfluss auf die aktuelle Forschung. Es geht in die Richtung, dass wir für längerfristige Antitumoreffekte, wenn wir diese haben wollen, sicherstellen müssen, dass genau solche Zellen vermehrt im Produkt enthalten sind. So wie die Stammzelle für das blutbildende System gibt es Vorläuferzellen für T-Gedächtniszellen, die sich über viele Jahre, auch Jahrzehnte erhalten und ihre Funktion ausüben.
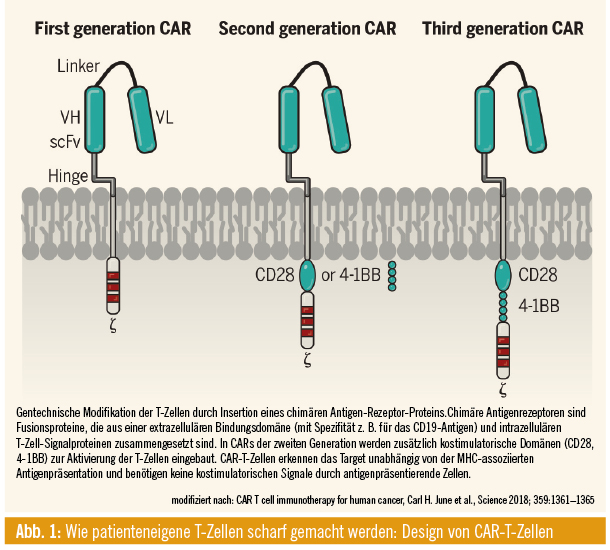
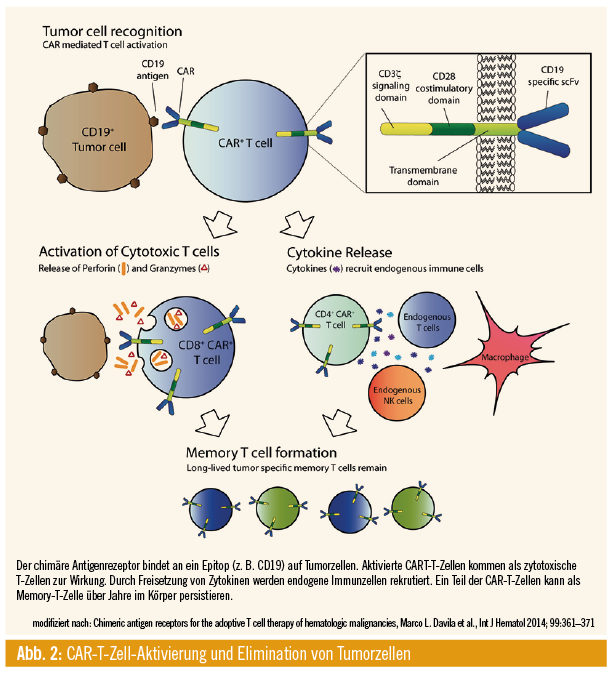
Es gibt Zentren, die beim fertigen Produkt auf ein ausgewogenes Verhältnis von CD4- und CD8-T-Zellen achten. Bei den zugelassenen Produkten ist das nicht so, bei diesen werden alle T-Zellen verwendet. Prinzipiell aber beruht der Erfolg einerseits auf der Wirkung der Zellen als tumorspezifische zytotoxische T-Zellen, die das Target sofort erkennen und eradizieren. Daneben gibt es Bystander-Effekte, nämlich dass im Rahmen dieser massiven Zytotoxizität auch Zytokine freigesetzt werden, die wieder andere Immunzellen aktivieren, sodass z. B. auch CD4-Zellen oder andere antigenpräsentierende Zellen ihre Wirkung entfalten. Daher ist es schwierig, zu sagen, welcher einzelne Aspekt des Produkts essenziell ist: der Rezeptor, die kostimulatorischen Domänen oder die Signaling-Domänen. Man muss das mehr als Package betrachten. Die technischen Unterschiede erklären aber wahrscheinlich auch Unterschiede in den Nebenwirkungen.
Erste Daten weisen in die Richtung, dass Lymphozyten von Patienten, die multiple Chemotherapien hinter sich haben, vermehrt dem „exhausted“ Phänotyp entsprechen. Man weiß von Patienten mit schweren Infektionskrankheiten oder auch nach allogener Transplantation, deren Lymphozyten häufig stimuliert wurden, dass ein nicht mehr stimulierbarer Phänotyp resultiert, der sozusagen erschöpft, „exhausted“ ist. Es sind anerge Zellen. Ein solcher Phänotyp wurde auch in Zusammenhang mit Checkpointinhibitoren untersucht. Davon ausgehend gibt es nunmehr Ansätze, die CAR-T-Zell-Wirkung durch die Kombination mit Checkpointinhibitoren weiter zu verbessern. Mit der Rationale, dass die autologen Lymphozyten von Patienten mit massiver Vortherapie dadurch aktiviert werden können. Denn es ist schon so: Sollten diese Zellen tatsächlich nicht aktiviert werden, dann ist es auch schwer vorstellbar, dass sie zunächst das Tumorantigen erkennen und in der Folge expandieren.
Die Diskussion ist daraus entstanden, dass CAR-T-Zellen eine Weiterentwicklung der allogenen Transplantation darstellen. Die allogene HSCT ist die erste etablierte zelluläre Immuntherapie, allerdings sehr unspezifisch, weil praktisch alle T-Lymphozyten im Graft vorhanden sind und man damit nicht weiß, was genau in vivo aktiviert wird. Demgegenüber ist die CAR-T-Zell-Therapie spezifischer. Es gibt ein klar definiertes Target wie CD19, und die Zellen sind so weit verändert, dass sie in vivo als zytotoxische T-Zellen massiv expandieren und ihr Target auf Anhieb finden. Daraus ist der Vergleich entstanden. Richtig ist, dass bei Lymphomen, vor allem in Europa, überwiegend die autologe Transplantation durchgeführt wird. Im allogenen Setting gibt es diesbezüglich nur unbefriedigende Daten, vor allem aus Registern. Es sind retrospektive Daten einzelner Zentren, keine prospektiven und schon gar keine randomisierten Erhebungen. Wenn wir also Patienten mit refraktärer Erkrankung der allogenen HSCT zuführen, so wissen wir nicht, ob die Ergebnisse gleich gut, besser oder schlechter sind als mit CAR-T-Zellen. Dazu kommt, dass auch die aktuell laufenden Studien im Standardarm die autologe HSCT anwenden. Das heißt, wir werden aus diesen Studien erfahren, ob die CAR-T-Zell-Therapie der autologen HSCT überlegen ist oder nicht. Die allogene Fragestellung wird noch länger unbeantwortet sein.
Die neuen Substanzen haben eine Zulassung bei aggressiven B-Zell-Neoplasien nach Versagen von zumindest zwei Therapielinien, d. h. diese Patienten sind weit fortgeschritten. Das setzt auch voraus, dass eine intensivere Salvage-Therapie vertragen wurde. Komorbiditäten sind ein Thema. Dazu kommt, dass die Datenmenge aus den Zulassungsstudien überschaubar ist, sodass man erst mit Real-World-Patienten sehen wird, wie die Therapie tatsächlich vertragen wird, wie Patienten das Zytokinfreisetzungssyndrom (CRS) oder die Neurotoxizität tolerieren können. Der Konsens derzeit ist, dass wir Patienten mit schweren neurologischen Vorerkrankungen oder Einschränkungen nicht mit CAR-T-Zellen behandeln sollten. Wir sind in der Schätzung von Patientenzahlen derzeit noch zurückhaltend und diskutieren vor allem die medizinischen Voraussetzungen, die Patienten mitbringen müssen.
Das ist für Österreich nur schwer festzulegen, weil wir die Stammzelltransplantation nicht als eine Therapie abrechnen. Wir haben LKF-Punkte für verschiedene Teilbereiche, z. B. eine schwere GvHD und Immunsuppression, für eine Thrombozytenkonzentratsubstitution u. a. m. Der intramurale Bereich ist vom ambulanten zu trennen. Es gibt Jahresbudgets für verschiedene Bereiche, z. B. Zytostatika, Antiinfektiva, die in der ärztlichen Verantwortung liegen und auch umgeschichtet werden können. Aus all diesen Gründen heraus werden wir so bald nicht in der Lage sein, das zu vergleichen.
Interessant wäre es für Patienten, die sich über lange Zeit in kompletter molekularer Remission befinden. Dann könnte man CAR-T-Zellen eliminieren, in der Hoffnung, dass sich die B-Zellen regenerieren und der Patient nicht über lange Zeiträume B-Zell-aplastisch und damit immundefizient ist. Die Situation ist derzeit aber nicht ganz klar. Für die Patienten wäre es prinzipiell positiv. Die Befürchtung in einer solchen Situation ist aber immer die, dass der CAR-T-Zelleffekt verloren geht und ein Rezidiv auf
tritt.
Wir kennen inzwischen viele Bilder der Neurotoxizität. Mitarbeiter werden geschult, auf Veränderungen, z. B. im Schriftbild, frühzeitig zu reagieren, auch wenn diese anfangs nicht wirklich auffällig sind. Anders als beim Zytokinfreisetzungssyndrom, bei dem IL6 steigt oder sinkt und man einen Risikobereich abschätzen kann, gibt es keinen Biomarker, der uns die Neurotoxizität anzeigen würde. Die therapeutischen Möglichkeiten sind begrenzt. Letztlich wird der Patient observiert und supportiv unterstützt. Prinzipiell ist die Neurotoxizität selbstlimitierend, man muss aber darauf achten.
Ich denke, bei der autologen Stammzelltransplantation haben Patienten nach 3 Monaten eine sehr gute Regeneration. Im allogenen Bereich hängt es davon ab, ob eine chronische GvHD auftritt oder nicht. Ohne chronische GvHD sind die Patienten in der Regel nach 9–12 Monaten gut regeneriert, was durchaus altersabhängig ist. Wir haben inzwischen viele Patienten im Alter von 60 Jahren und darüber. Die Phase der Immundefizienz mit dem Risiko für opportunistische Infekte ist unter Verwendung eines Fremdspenders länger, dauert etwa 2–3 Jahre. Darüber hinaus wissen wir im Transplantbereich auch sehr gut über Langzeitfolgen Bescheid. Das alles ist derzeit mit der CAR-T-Zell-Therapie nur schwer vergleichbar. Die Nachbeobachtungszeiten sind noch zu kurz, um Folgewirkungen einschätzen zu können. Man kann aber festhalten: Es gibt erstaunlich wenig schwere Infekte für die Tatsache, dass im Rahmen von CAR-T-Zell-Therapien auch B-Zell-Aplasien vorkommen. Auch eine febrile Neutropenie ist nur bei etwa 10 % der Patienten aufgetreten, was im Vergleich zu etlichen Chemotherapien wenig ist. Patienten haben nach einer CAR-T-Zell-Therapie zwar vorübergehend eine gewisse Zytopenie, werden aber nicht aplastisch und sind offenbar auch immunologisch insgesamt weniger beeinträchtigt.
Wir sind in eine Studie mit Axicabtagen-Ciloleucel involviert und machen im Rahmen dieser Studie einen Zertifizierungsprozess durch. Als Team haben wir uns vorgenommen, dass wir auf diesem Weg zunächst Erfahrungswerte sammeln wollen. Das Hauptaugenmerk liegt also derzeit auf der Bereitstellung der Infrastruktur und der Schulung der Mitarbeiter, um mit der Studie gut beginnen zu können. Aber es ist sicher so, dass der Lymphombereich in Zukunft für den Einsatz von CAR-T-Zell-Therapien besonders relevant werden wird.
Technologisch am spannendsten sind aus meiner Sicht die „Off the shelf“-Entwicklungen, weil es nach wie vor ein enormer Aufwand ist, die Produkte für jeden Patienten spezifisch herzustellen. Solange wir die CAR-T-Zell-Therapie derart individuell durchführen, werden auch die Kosten hoch bleiben. Es ist eine logistische, technologische und wissenschaftliche Herausforderung und nicht vergleichbar mit der Produktion einer Tablette, was sicher einen Teil der Kosten erklärt. Die Durchführung ist für Zentren sehr fordernd. Das Attraktive an einem „Off the shelf“-Produkt wäre die rasche Verfügbarkeit für alle Patienten. „Off the shelf“ heißt, dass T-Zellen von einer gesunden Person genommen werden. Diese werden dann nicht nur mit dem Oberflächenmerkmal ausgestattet, sondern es wird durch gentechnische Veränderungen im T-Zell-Rezeptor auch die Alloreaktivität ausgeschaltet, um Abstoßungen und GVhD zu vermeiden. Ich kann mir sehr gut vorstellen, dass dieser Ansatz wegweisend sein wird.