Aufbau und Struktur eines urologischen molekularen Tumorboards
Technologischer Fortschritt ermöglicht Präzisionsonkologie: Die vollständige Entschlüsselung des menschlichen Genoms zusammen mit Fortschritten in Hochdurchsatzverfahren zur Analyse des Genoms, Epigenoms, Transkriptoms, Proteoms und Metaboloms („Omics“-Technologien) ermöglicht die Suche nach individuellen Merkmalen von Tumoren. Auch die Anwendung der „liquid biopsy“ gehört zu den Schlüsseltechnologien in der modernen Onkologie. Diese ermöglicht eine nichtinvasive Überwachung der Tumorlast, eine Analyse auf Genom, Transkriptom- und oder Proteomebene und somit eine dynamische Therapiesteuerung. Diese technologischen Fortschritte ermöglichen eine Präzisionsonkologie mit besonders effektiven und nebenwirkungsarmen Therapien. Zielgerichtete Therapien nach der Bestimmung des individuellen Mutationsprofils eines Tumors erzielen bei bestimmten Tumorentitäten große Erfolge. Auch für urologische Tumoren sind die Therapiemöglichkeiten in den letzten Jahren vielschichtiger und individueller geworden. Die Herausforderung für den behandelnden Arzt liegt in der Wahl der besten Therapie für den richtigen Patienten zum optimalen Zeitpunkt.
Molekulare Charakterisierung: Durch die Fortsetzung des TCGA-(The Cancer Genome Atlas-)Projekts ist beim Harnblasenkarzinom ein umfassenderer Vorschlag zur molekular basierten Subtypisierung mit nachfolgend angepassten therapeutischen Möglichkeiten erarbeitet worden.1 Auch das bessere Verständnis der immunmodulierenden Interaktionen zwischen Tumorzellen und Immunzellen hat zu neuen vielversprechenden Therapiestrategien wie dem Einsatz der Checkpoint-Inhibitoren beim Blasen- und Nierenzellkarzinom geführt.2, 3 Für das metastasierte Prostatakarzinom gibt es zahlreiche neue systemische und zielgerichtete Behandlungsoptionen. So zeigten Mateo und Mitarbeiter, dass beim Prostatakarzinom – wie auch schon bei vielen anderen Tumorentitäten – eine molekulare Charakterisierung vor Initiierung einer Therapie prädiktiv sein kann. Patienten mit metastasierten, kastrationsrefraktären Prostatakarzinomen mit DNA-Reparaturdefekten – durch Mutationen in den BRCA1- und BRCA2-Genen – sprechen auf eine systemische Therapie mit PARP (Poly-[ADP-Ribose-]Polymerase-)Inhibitoren an.4 Für Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom stehen neben Docetaxel, Cabazitaxel, Radium-223 auch gegen den Androgenrezeptor (AR) gerichtete endokrine Substanzen (Abirateron, Apalutamid und Enzalutamid) zur Verfügung; weitere zielgerichtete Substanzen für Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom sind in klinischer Prüfung.5
Implementierung eines urologischen molekularen Tumorboards
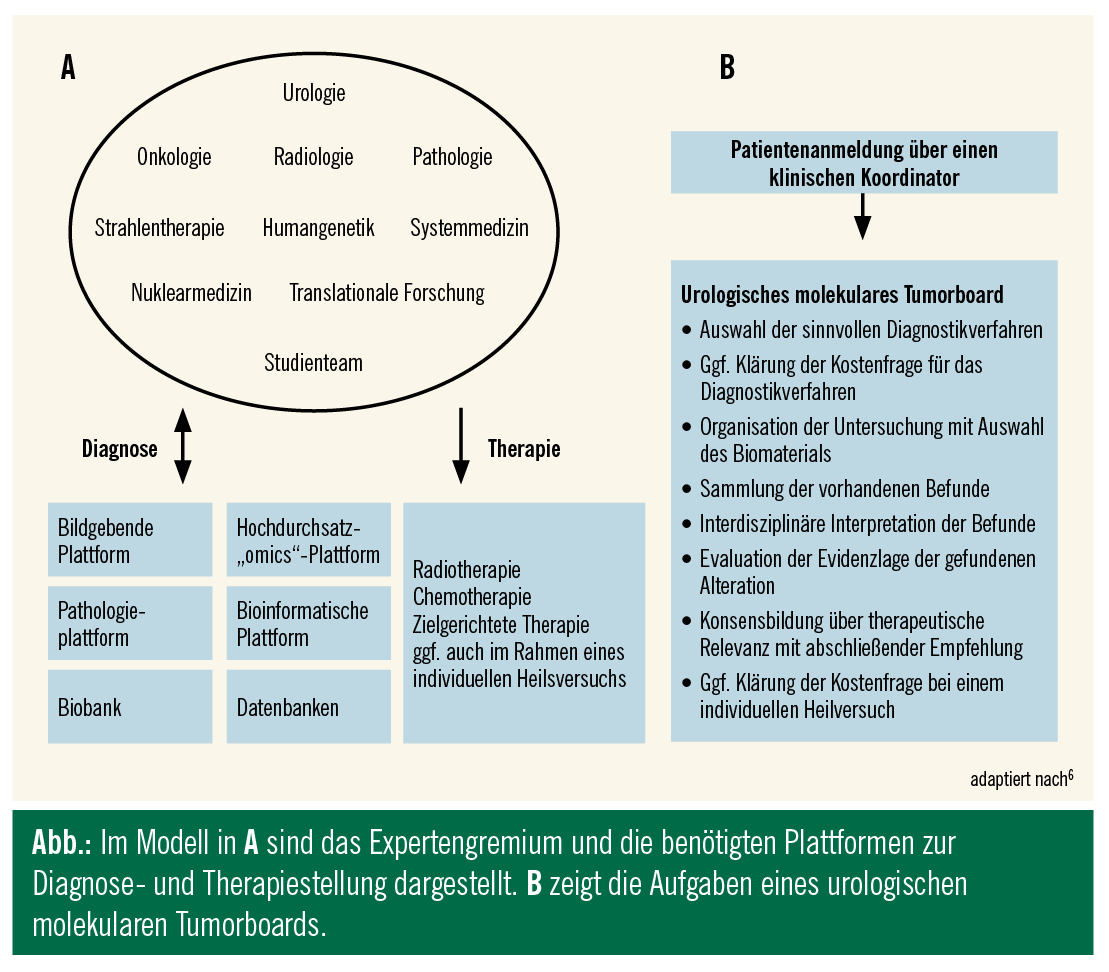
Die Bestimmung des individuellen Mutationsprofils und die zeitnahe Integration von Forschungsergebnissen ermöglichen eine verbesserte Therapie, allerdings stellen die versorgungsgerechte Interpretation der molekularen Befunde und die darauf basierende Therapieentscheidung noch eine beträchtliche zeitliche und personelle Herausforderung dar. Der Implementierung eines urologischen molekularen Tumorboards kommt deshalb eine zentrale Bedeutung zu (Abb.).
In diesem urologischen molekularen Tumorboard können Patienten mit fortgeschrittener Tumorerkrankung, ohne erfolgversprechende Therapieoption, mit seltener Tumorentität/molekularpathologischem Profil und mit ungewöhnlichen klinischen Verläufen, und/oder nach Versagen aller zugelassenen Therapieoptionen erörtert werden. Die Zusammensetzung des Expertengremiums des urologischen molekularen Tumorboards umfasst neben an der Behandlung des Patienten unmittelbar beteiligten Ärzten (Urologie, Onkologie, Pathologie, Radiologie, Strahlentherapie, Nuklearmedizin) immer auch Experten aus allen benachbarten in molekularer Diagnostik geschulten Fachdisziplinen (Molekularpathologie, Humangenetik, Bioinformatik, Systembiologie, translationale Forschung, Studienteam u. a.), die für die Analyse und Interpretation der vorhandenen Daten benötigt werden. Dieses Expertenteam bespricht alle erhobenen Patientendaten und erörtert zuerst die noch durchzuführenden diagnostischen Verfahren.
Erleichtert wird die Planung und Durchführung des urologischen molekularen Tumorboards durch eine prozessorientierte Informations- und Kommunikationsplattform. Diese gewährleistet die nötige lückenlose Dokumentation aller Patientinnen/Patienten und die Bereitstellung aller erforderlichen Informationen zur Diskussion des Falles (Bildgebung, Pathologie, genetische Informationen etc.). Diese Informationen werden vor der Besprechung eingestellt. Weiterhin kann durch diese Plattform ggf. eine ortsunabhängige, standardisierte Vernetzung von Experten ermöglicht und die Tools für die Datenanalyse und klinische Studien standortübergreifend bereitgehalten werden.
Fazit
Nach Durchführung umfassender diagnostischer Verfahren werden die Hochdurchsatz-Datensätze in Zusammenschau aller erhobenen Patientendaten besprochen und fächerübergreifend ausgewertet. Ziel dieses urologischen molekularen Tumorboards ist es, Patienten durch die Anwendung neuer Verfahren den Zugang zu neuen, zielgerichteten Therapien, auch im Rahmen von klinischen Studien oder im Sinne eines individuellen Heilversuchs, zu ermöglichen.