Fortgeschrittenes Basalzellkarzinom – Die Prognose verbessern
Bislang standen Patienten mit fortgeschrittenem Basalzellkarzinom nur die chirurgische Sanierung und Strahlentherapie zur Verfügung. V. a. bei rezidivierenden Tumoren im Gesichtsbereich kommen diese Therapieoptionen oft nicht mehr in Betracht. Mit dem „small molecule“ Vismodegib, das am Hedgehog(Hh)-Signalweg ansetzt, steht nun erstmals auch eine zielgerichtete Therapie zur Verfügung. Die neue Substanz hat bereits eine Zulassung der FDA für die Therapie erwachsener Patienten mit einem Rezidiv eines lokal fortgeschrittenen oder metastasierten Basalzellkarzinoms nach Operation und für die Therapie von Patienten, bei denen weder ein chirurgischer Eingriff noch eine Radiotherapie in Frage kommt.
12-Monate-Follow-up der ERIVANCE-BCC-Studie
In der pivotalen nichtrandomisierten ERIVANCE-BCC-Studie sprachen 30 % der Patienten mit lokal fortgeschrittenem Basalzellkarzinom und 43 % der Patienten mit metastasierendem Basalzellkarzinom auf die Therapie mit Vismodegib an1. Beim ESMO 2012 wurden nun die 12-Monate-Follow-up-Daten2 präsentiert.
Die ERIVANCE-BCC-Studie ist eine multizentrische, internationale, nichtrandomisierte 2-Kohorten-Studie.
Eingeschlossen wurden insgesamt 104 Patienten mit metastasiertem oder mit lokal fortgeschrittenem, als inoperabel beurteiltem Basalzellkarzinom. Voraussetzung war eine Radiotherapie von zumindest einer Läsion, sofern medizinisch sinnvoll und nicht kontraindiziert.Die Patienten erhielten oral Vismodegib 150 mg einmal täglich bis zur Krankheitsprogression, bis zum Auftreten einer nicht tolerierbaren Toxizität oder bis zum Studienabbruch. Bei Auftreten einer Toxizität war eine Therapieunterbrechung für bis zu 4 Wochen erlaubt. Die Wirksamkeit wurde sowohl von den Studienärzten als auch von unabhängigen Reviewern beurteilt. Endpunkte waren die objektive Responsrate (ORR), das progressionsfreie Überleben („progression-free survival“, PFS) und das Gesamtüberleben („overall survival“, OS).
Am 28. November 2011 waren 29 Patienten (27,9 %) noch unter Vismodegibtherapie. Die mediane Therapiedauer betrug durchschnittlich 12,9 Monate, die mediane Dosisintensität lag bei über 97 %.
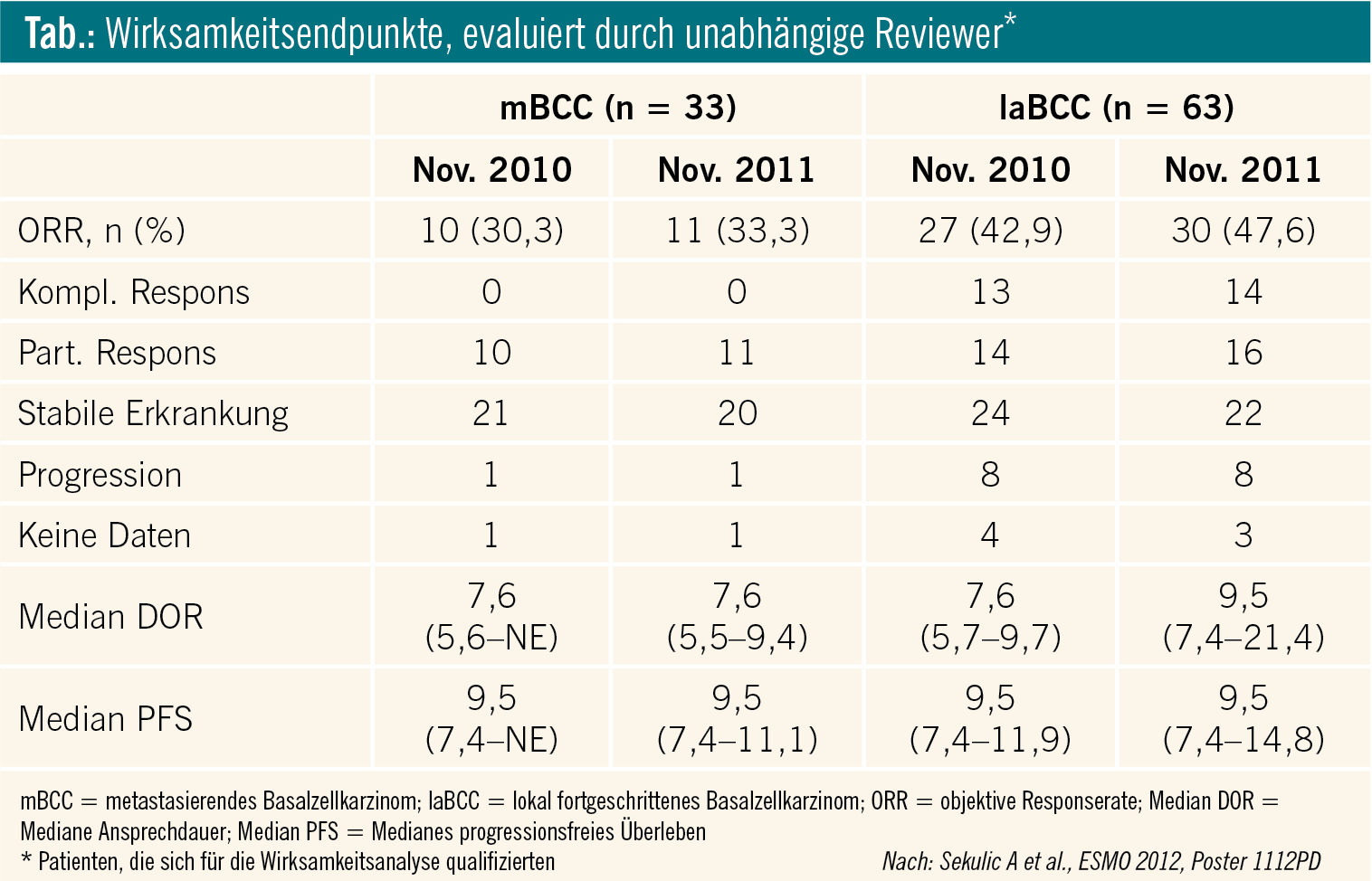
Die ORR entsprachen im 12-Monats-Update denen der primären Analyse; die unabhängigen Reviewer bestätigten bei vier zusätzlichen Patienten einen Respons (Tab.). 14 Patienten mit lokal fortgeschrittenem Basalzellkarzinom wiesen einen vollständigen Respons auf, 16 einen partiellen Respons und 22 eine stabile Erkrankung (Patienten mit metastasiertem Basalzellkarzinom: 0 %, 11 %, 20 %).
In beiden Kohorten waren das von den unabhängigen Reviewern bewertete PFS und OS identisch mit dem Ergebnis der ersten Analyse. In der Beurteilung der Studienärzte entsprach das PFS bei Patienten mit metastasiertem Basalzellkarzinom nach dem 12-monatigen Follow-up ebenfalls dem Ergebnis der ersten Analyse, während es bei Patienten mit lokal fortgeschrittenem Basalzellkarzinom um 1,6 Monate länger war.
Die 2-Jahres-Überlebensraten lagen bei Patienten mit metastasiertem Basalzellkarzinom bei 60,3 % und bei Patienten mit lokal fortgeschrittenem Basalzellkarzinom bei 85,2 %.
Sicherheit und Verträglichkeit
Am Ende des 12-monatigen Follow-ups hatten 75 Patienten (72,1 %) innerhalb der Kontrollphase abgebrochen. Hauptgründe waren bei Patienten mit metastasierendem Basalzellkarzinom die Krankheitsprogression (14 von 26 Abbrüchen; 53,8 %) und die Entscheidung des Patienten (4 Patienten). Patienten mit lokal fortgeschrittenem Basalzellkarzinom brachen die Therapie ebenfalls am häufigsten aufgrund eigener Entscheidung (20 Patienten) und aufgrund von Krankheitsprogression (8 Patienten) ab.
Das Sicherheits- und Verträglichkeitsprofil von Vismodegib entsprach dem bisher gezeigten Profil. Rund die Hälfte der therapieassoziierten Nebenwirkungen waren mild oder moderat (Grad 1–2).
Fazit
Die Daten des 12-Monate-Follow-ups weisen somit auf ein langfristiges Ansprechen auf Vismodegib und ein beherrschbares Nebenwirkungsprofil hin.