ABPA – allergische bronchopulmonale Aspergillose
Schimmelpilze finden sich ubiquitär und werden häufig mit respiratorischen Erkrankungen in Verbindung gebracht. Schimmelpilzallergiker leiden in Österreich am häufigsten unter einer Alternaria‑, aber auch unter Cladosporium- oder Penicilliumallergie.
Schimmelpilze sind Saprophyten und ernähren sich von organischen Substanzen wie verfaulenden Blättern, Stroh (Viehfütterung!), Biomüll aber auch von Lebensmitteln. Aspergillus kann sowohl im Freien, wie etwa in Wäldern, Wiesen oder Sumpfgebieten, aber auch im Haus an feuchten Wänden gefunden werden. Die Sporengröße beträgt zwischen 2 µm und 20 µm. Die wichtigsten Unterarten von Aspergillus sind Aspergillus fumigatus, A. flavus und A. niger. Von Aspergillus fumigatus sind bisher 26 Allergene beschrieben1.
Häufigkeit und Klinik: Obwohl Aspergillus ein ubiquitärer Pilz ist, sind aspergillusassoziierte Erkrankungen selten. Insbesondere die allergische bronchopulmonale Aspergillose (ABPA) ist eine Erkrankung, die vor allem schwere Asthmatiker (Häufigkeit 1–2 %) und Patienten mit zystischer Fibrose (CF, Häufigkeit 2–15 %) betrifft.
Im Rahmen der Kolonialisierung der Bronchien mit Aspergillus kann es zu einer Sensibilisierung (IgE-, IgA- und IgG-Antikörper gegen Aspergillus) kommen (serologische ABPA). Grundvoraussetzung für das Auftreten der floriden ABPA sind Bronchiektasien. Somit kann eine ABPA auch bei Patienten mit angeborenen Bronchiektasien auftreten. Pathophysiologisch ist die ABPA eine Typ-1(IgE-Spätreaktion)- und Typ-3(IgG)-Überempfindlichkeitsreaktion, die im Rahmen der chronischen Inflammation zu Remodeling und Destruktion der Bronchien führt.
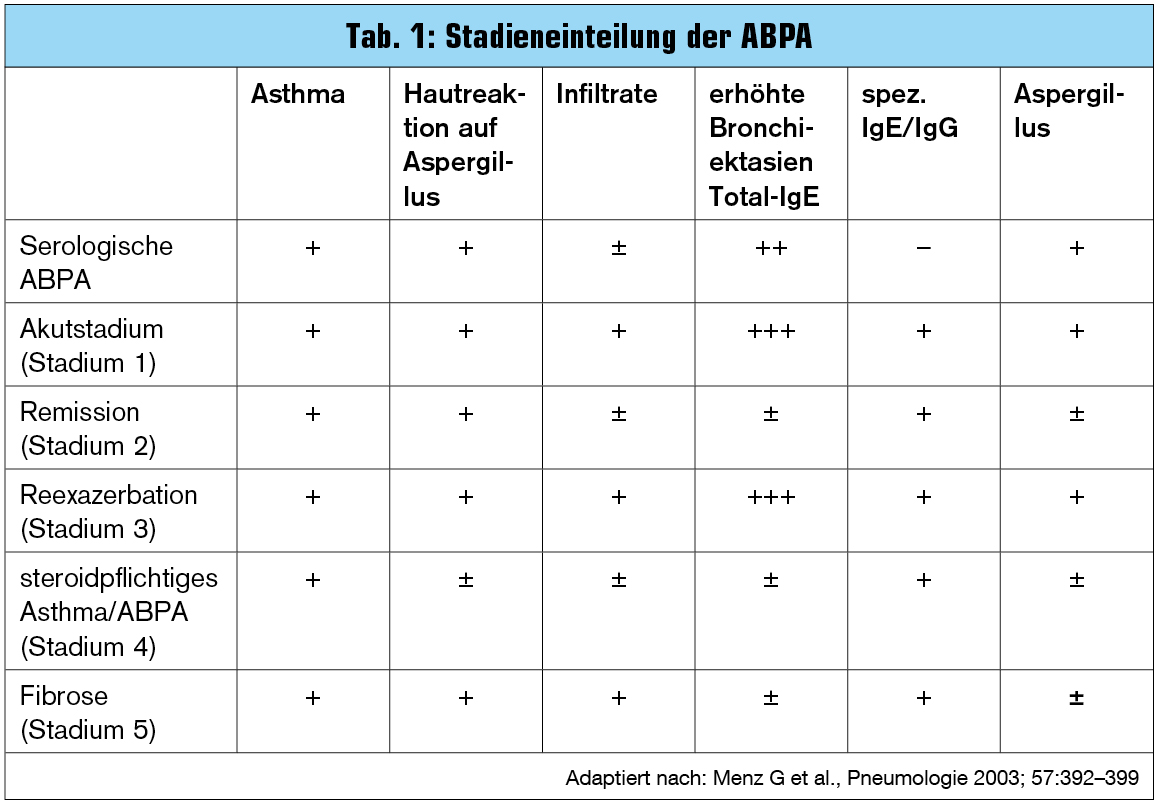
Die ABPA tritt in Stadien auf. Eine Kolonialisierung mit Aspergillus führt noch nicht zur Erkrankung, vorher muss sich der Patient sensibilisieren (serologische ABPA). In diesem Stadium kann der Patient jahrelang verbleiben, die Prognose ist bei Asthmatikern gut2 (Tab. 1). Das Stadium 1 ist bei erstmaligem Ausbruch der Erkrankung erreicht. Die Klinik der ABPA ist unspezifisch und geht mit Verschlechterung des Allgemeinzustandes, subfebrilen Temperaturen, Gewichtsverlust, Zunahme von Husten und bronchialer Obstruktion und mitunter bräunlich-bröckeliger Expektoration einher. Typisch sind das Fehlen von bakteriellen oder viralen Infekten und der frustrane Therapieversuch mit Antibiotika. Die Diagnostik der ABPA gestaltet sich schwierig und bedarf neben Klinik einer serologischen und radiologischen Aufarbeitung.
Diagnostik und Diagnosekriterien: Neben der bereits oben beschriebenen Klinik findet sich serologisch neben leicht erhöhten Entzündungszeichen mitunter eine periphere Eosinophilie. Typischerweise zeigt sich ein signifikant erhöhter Gesamt-IgE-Spiegel (> 1.000 kU/l; Vergleich zu Vorbefund!) und neben dem positiven Hautpricktest auf aspergillusspezifische IgE-Antikörper gegen Aspergillus im Blut.
Gerade die serologische Abklärung der ABPA hat in den letzten Jahren Fortschritte gemacht. Rekombinante Allergene können helfen, eine Sensibilisierung von einer floriden ABPA zu unterscheiden. Finden sich neben dem Gesamtextrakt positive Befunde auf Asp f1 und Asp f3, so liegt eine Sensibilisierung vor, bei positiven Asp-f4- und Asp-f6-Befunden ist an die ABPA zu denken. Die Bestimmung von TARC (thymus- and activation regulated chemokine) würde die Differenzialdiagnostik aufgrund der gegenüber Aspergillusantigen höheren Sensitivität und Spezifität weiter erleichtern, allerdings ist diese Untersuchung bisher nicht in die Routinediagnostik vorgedrungen. Die Typ-3-Serologie wurde früher mittels Präzipitationstests durchgeführt, heutzutage kann man spezifische IgG gegen Aspergillusantigene (z. B. mittels dem Thermo Fisher ImmunoCAP®) bestimmen (Tab. 2 und 3).
Therapie: Die ABPA ist eine inflammatorische Erkrankung der Bronchien. Somit steht die antiinflammatorische Therapie mit anfänglicher Hochdosissteroidtherapie im Vordergrund. Bezüglich der schrittweisen Reduktion der Steroidtherapie gibt es zwei Dosierungsregime. Die zweite Säule der Therapie, welche sich eher in frühen Stadien anbietet, ist die antimykotische Therapie mit Itraconazol, mitunter auch mit Voriconazol (Cave Leberparameter). Eine neuartige, wenn auch bisher nicht etablierte Therapie (off label) ist die Anti-IgE-Therapie mit Omalizumab. Diese Therapie kann auch dann von Erfolg sein, wenn der Gesamt-IgE-Spiegel deutlich über 1.300 kU/l liegt. Zunehmend finden sich positive Berichte über erfolgreiche Behandlungen der ABPA bei CF-Patienten. Meine persönlichen Erfahrungen mit der Anti-IgE-Therapie waren positiv, sowohl in Wirksamkeit als auch Verträglichkeit. Der Vorteil der Anti-IgE-Therapie besteht in seiner steroidsparenden Wirkung (Tab. 4).
Verlaufskontrolle, Reexazerbation und Prophylaxe: Bei Ansprechen der Therapie zeigt sich neben der klinischen Verbesserung und der Rückbildung der radiologischen Infiltrate zumeist eine Abnahme des Gesamt-IgE-Spiegels um 35 % bis 50 % innerhalb von 6 bis 12 Wochen.
Bei Verdacht auf Reexazerbation sind die diagnostischen Schritte ident zum Akutstadium. Typisch ist der massive Neuanstieg des Gesamt-IgE-Spiegels (Verdoppelung gegenüber Vorbefund). Auch die Therapie ist ident. Prophylaktisch sollten Patienten neben feuchten Wohnräumen vor allem jeden Kontakt zu Biomüll- und Kompostierungsanlagen – inklusive Biotonne – meiden.