Orale Diabetestherapie mit DPP-4-Inhibitoren – Differenzialtherapeutische Überlegungen
Die Therapie des Typ-2-Diabetes mit etablierten Substanzen ist mit Ausnahme der Datenlage über Metformin alles andere als evidenzbasiert. Auch bezüglich Metformin ist einschränkend zu bemerken, dass die zur Evidenz herangezogene Substudie der UKPDS (UKPDS Group, Lancet 1998) nach heutigen Standards kaum als gültig erachtet würde. Jedoch konnte die günstige Wirkung von Metformin, nicht nur auf die Glykämie beschränkt, in Beobachtungsstudien bestätigt werden, sodass Metformin als First-Line-Medikament in der Behandlung des Typ-2-Diabetes gilt (Clodi et al., Wien Klin Wochenschr 2009).
Anders verhält es sich mit den Sulfonylharnstoffen, wobei hier zwischen den verschiedenen Generationen zu differenzieren ist. Als unerwünschte Wirkungen sind hier vor allem die Hypoglykämien, Gewichtszunahme und eine mögliche Förderung der Betazellerschöpfung anzuführen (Inzucchi, JAMA 2002).
Die Insulinsensitizer oder Glitazone erlebten eine wechselvolle Geschichte, und der als einzig verfügbare Vertreter, Pioglitazon, muss aufgrund von Nebenwirkungen (Ödem, Frakturen) ebenfalls gezielt eingesetzt werden, um ein optimales Nutzen-Risiko-Verhältnis zu garantieren (Shah & Mudaliar, Expert Opin Drug Saf 2010). Mit Ausnahme von Pioglitazon verlangsamen die hier angeführten Medikamente nicht die Progression des Insulinsekretionsdefekts und beeinflussen somit nicht den Verlauf der Erkrankung. Diese Limitationen rechtfertigen somit die Entwicklung innovativer Medikamente mit alternativem Wirkmechanismus.
Das Inkretinsystem
Das Inkretinsystem mit den vielfältigen Wirkungen auf wichtige Akteure im Glukosestoffwechsel stellt ein neuartiges Ziel für eine therapeutische Intervention beim Typ-2- Diabetes dar (Drucker & Nauck, Lancet 2006). Die Inkretine Glucagon-like peptide 1 (GLP-1) und Glucose-dependent insulinotropic polypeptide (GIP) führen nach oraler Glukoseaufnahme zu einer Verstärkung der Insulinsekretion. GLP-1 supprimiert auch noch die Glucagonsekretion und in der Folge den hepatischen Glukose-Output, verzögert die Magenentleerung und induziert ein Sättigungsgefühl. Da die Halbwertszeit von GLP-1 aufgrund der Deaktivierung durch das Enzym Dipeptidylpeptidase 4 (DPP-4) im Bereich von 1–2 Minuten liegt, kann die therapeutische Anwendung entweder in der Verabreichung von Inkretinmimetika oder durch medikamentöse Hemmung von DPP-4 (DPP-4-Hemmer, Gliptine) erfolgen.
Im Folgenden sollen die einzelnen Vertreter der Gliptine hinsichtlich ihrer Gemeinsamkeiten und Unterschiede dargestellt werden.
Struktur, Pharmakokinetik und Sicherheit
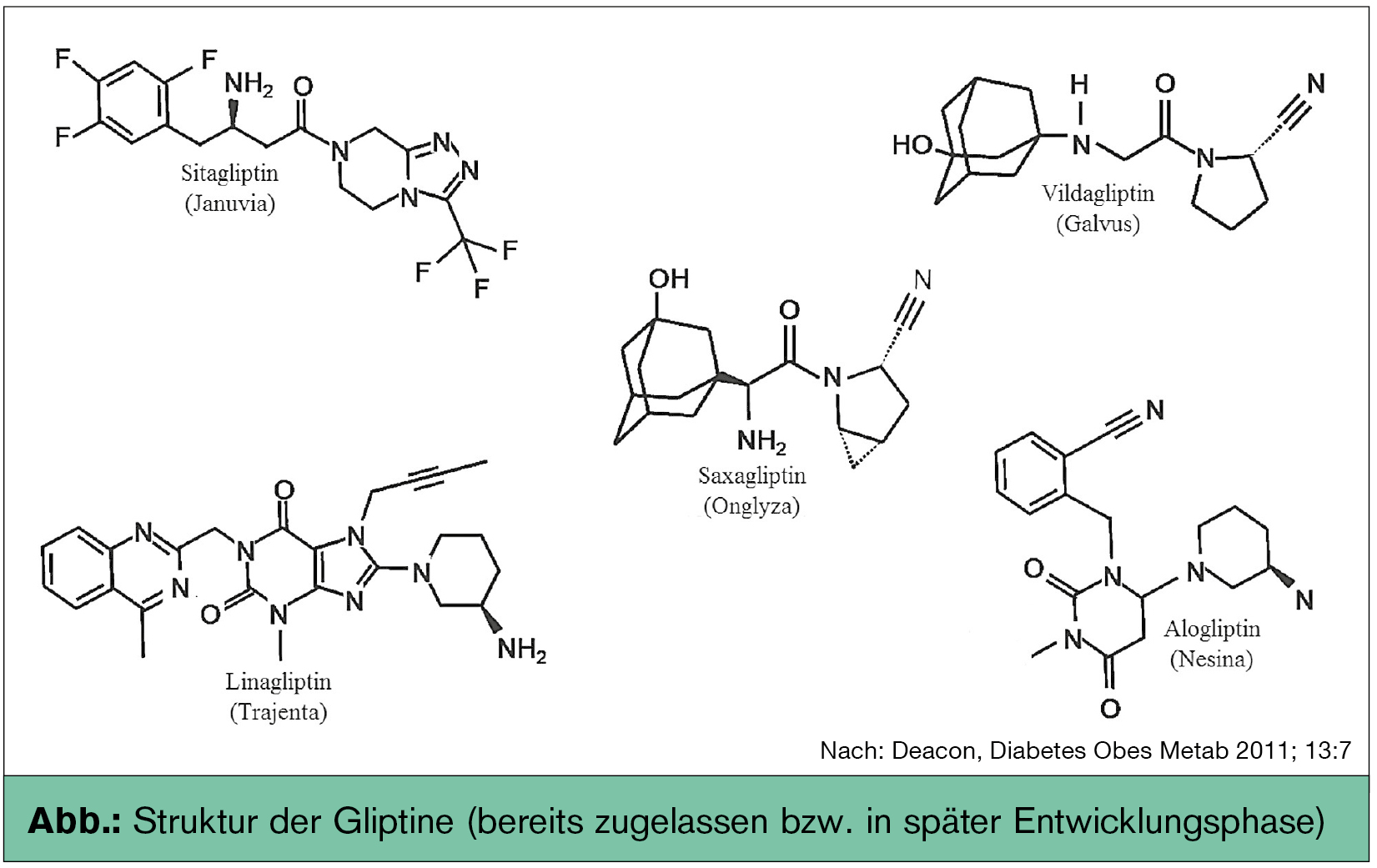
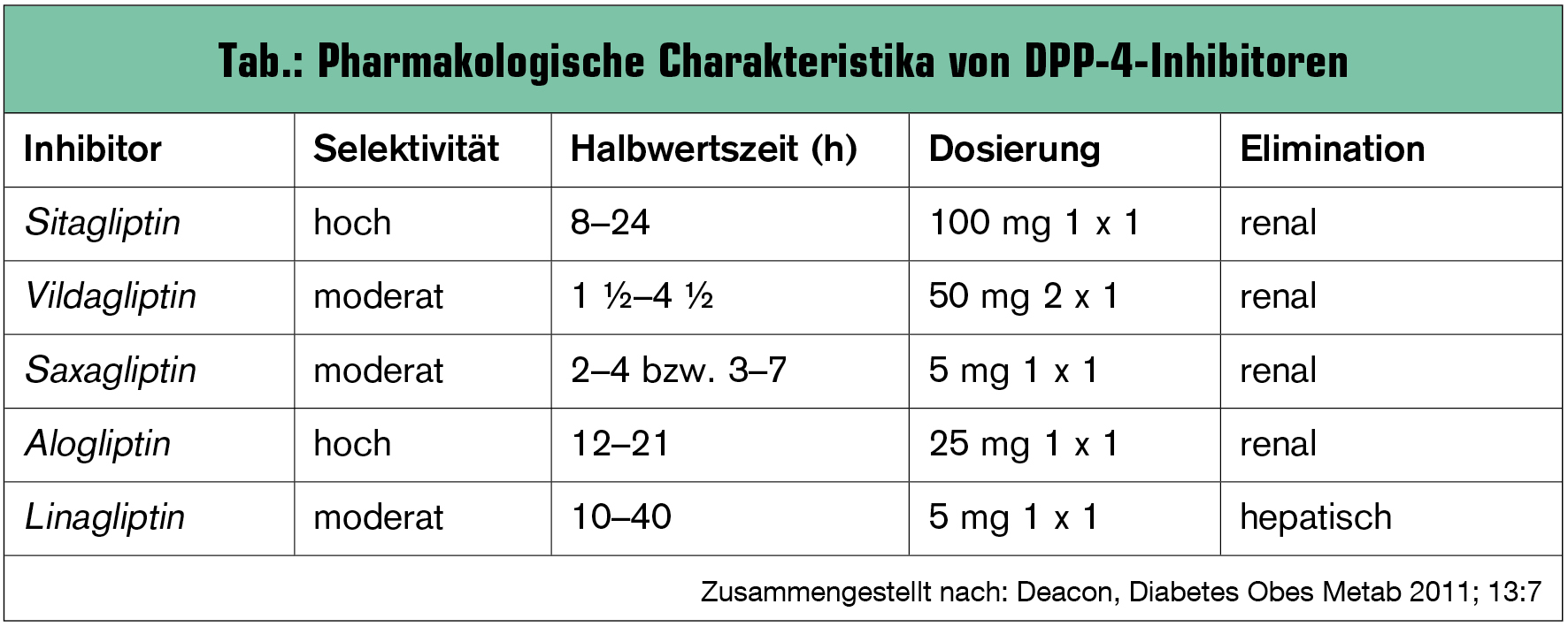
Die bereits zugelassenen oder sich in der Phase der Zulassung befindlichen Gliptine weisen durchaus unterschiedliche Strukturen auf (Abb.): Sitagliptin, Alogliptin und Linagliptin fungieren als kompetitive Inhibitoren von DPP-4, während Vildagliptin und Saxagliptin eine kovalente Bindung an die katalytische Region von DPP-4 eingehen (Deacon, Diabetes Obes Metab 2011). Dies führt durch eine langsame Equilibrierung trotz relativ kurzer Halbwertszeit zu einer längeren Wirkdauer. Unterschiede bestehen außerdem hinsichtlich der Halbwertszeit, Dosierung, Rezeptorselektivität sowie Eliminationsmodus (Tab.). Die Rezeptorselektivität bezieht sich auf die In-vitro-Selektivität für DDP-4 im Vergleich zu anderen DPP-Molekülen, deren Inhibierung möglicherweise toxische Folgen hätte. Unabhängig von diesen Unterschieden erhöhen sämtliche Gliptine die zirkulierenden GLP-1-Spiegel um das Zwei- bis Vierfache.
Die Verträglichkeit der Gliptine ist sehr gut. Anfängliche Beobachtungen über das vermehrte Auftreten von Harnwegsinfekten (Sitagliptin und Vildagliptin) sowie Nasopharingitis (Sitagliptin) konnten in gepoolten Analysen nicht bestätigt werden. Eine milde Erhöhung von Lebertransaminasen unter Vildagliptin mit einer Einmaldosierung von 100 mg im Vergleich zu einer zweimal täglichen Dosierung von 50 mg führte zur Empfehlung, die Leberfunktion unter Vildagliptin zu monitieren. Es findet sich jedoch kein Hinweis für eine relevante Hepatotoxizität (Ligueros-Saylan et al., Diabetes Obes Metab 2010).
Für alle inkretinbasierten Therapien ist das vermehrte Auftreten von Pankreatitiden nicht auszuschließen, sodass hier eine verstärkte Aufmerksamkeit sowie die Durchführung von prospektiven Sicherheitsstudien notwendig sind (Drucker et al., Diabetes Care 2010). Prinzipiell ist das Potenzial relevanter Interaktionen mit anderen Medikamenten sehr gering, lediglich für Saxagliptin ist bei gleichzeitiger Verabreichung starker CYP3A4-Inhibitoren (z. B. Ketokonazol) mit einer Erhöhung der Plasmaspiegel zu rechnen, sodass hier eine Dosisreduktion erfolgen sollte (Scheen, Clin Pharmacokinet 2010).
Klinische Wirksamkeit
Bezüglich der Effektivität der Gliptine hinsichtlich der Verbesserung der glykämischen Kontrolle dürften sich zwischen den derzeit am Markt befindlichen Substanzen keine wesentlichen Unterschiede finden. In Monotherapie wird das HbA1c zwischen 0,5 und 0,8 Prozentpunkte gesenkt, in Kombination mit Metformin, Sulfonylharnstoffen und Glitazonen zwischen 0,8 und 1,1 Prozentpunkten, wobei die initiale Stoffwechseleinstellung eine Rolle spielt (Deacon, Diabetes Obes Metab 2011). Die gemeinsame Verabreichung mit Metformin scheint besonders in Hinblick auf die additive Wirkung beider Substanzen hinsichtlich der Steigerung der GLP-1-Spiegel sinnvoll. In Kombination mit Insulin ist mit einer HbA1c-Senkung von 0,6 Prozentpunkten zu rechnen. Bezüglich etwaiger Unterschiede in der blutzuckersenkenden Potenz liegen lediglich die Ergebnisse einer direkten Vergleichsstudie (Scheen, Diabetes Metab Res Rev 2010) zwischen Sitagliptin und Saxagliptin vor, wobei sich bezüglich der HbA1c-Senkung (–0,6 vs. –0,5 Prozentpunkte) kein Unterschied fand; bezüglich der Senkung des Nüchternblutzuckers fand sich ein Vorteil für Sitagliptin (–0,9 vs. –0,6 mmol/l). Gliptine sind gewichtsneutral und führen nicht zu Hypoglykämien.
Betazellprotektives Potenzial
Sowohl für DPP-4-Hemmer als auch für Inkretinmimetika konnten im Tierversuch günstige Effekte auf die Betazellproliferation und Hemmung der Apoptose gefunden werden (Drucker & Nauck, Lancet 2006). Dies bewirkte eine Verzögerung bzw. Hemmung der Diabetesprogression im Tierversuch. Ob diese Effekte auch auf den Menschen übertragbar sind, lässt sich derzeit noch nicht abschätzen, sodass entsprechende Studien initiiert wurden. Dieser Mechanismus könnte aber, wenn er das duktale System des Pankreas betrifft, auch für ein möglicherweise vermehrtes Auftreten von Pankreatitiden verantwortlich sein. Diese potenziell ungünstige Wirkung kann aber in vitro durch Metformin verhindert werden (Matveyenko et al., Diabetes 2009).
Ob die Stimulierung von GLP-1-Rezeptoren im Bereich des Herz-Kreislauf-Systems eine zusätzliche, günstige Wirkung auf die kardiovaskuläre Morbidität bewirkt, ist derzeit Gegenstand prospektiver Studien. Bislang deutet die allerdings limitierte Datenlage auf ein diesbezüglich günstiges Profil hin.
Welches Gliptin für welchen Patienten?
Niereninsuffizienz: Wie aus der Tabelle ersichtlich, werden die meisten Gliptine mit Ausnahme von Linagliptin renal eliminiert. Die Dosis dieser Gliptine muss ab einer glomerulären Filtrationsrate (GFR) < 50 ml/min entsprechend vermindert werden, wobei die Dosis bei einer GFR zwischen 30 und 50 ml/min in der Regel halbiert wird. Lediglich Linagliptin bedarf aufgrund seiner hepatischen Elimination auch bei fortgeschrittener Niereninsuffizienz keiner Dosisanpassung.
Verminderte Leberfunktion: Aufgrund des renalen Eliminationsmechanismus der meisten Gliptine ist eine Dosisanpassung bei milder bis moderater Leberinsuffizienz nicht notwendig. Diese Substanzen werden aber nicht explizit bei Patienten mit Leberfunktionsstörungen empfohlen, da hier noch publizierte Daten fehlen. Vildagliptin zeigte in der einmal täglichen Dosis von 100 mg eine Erhöhung der Leberfunktionsparameter, sodass von einer Anwendung bei Patienten mit erhöhten Leberwerten Abstand genommen werden muss. Da Linagliptin hepatisch eliminiert wird, ist bei schwerer Einschränkung der Leberfunktion von einem Anstieg der Wirkspiegel auszugehen. Daher sollte bei diesem Kollektiv ein renal eliminiertes Gliptin angewandt werden.
Zusammenfassung: Die Wirksamkeit der DPP-4-Inhibitoren entspricht, wie aus Vergleichsstudien mit etablierten Substanzen ersichtlich ist, jener üblicher Antidiabetika. Gliptine sind gewichtsneutral, verursachen keine Hypoglykämien und bedürfen keiner Dosistitration. Die Verträglichkeit ist gut, Interaktionen mit anderen Medikamenten sind selten. Hinsichtlich der Sicherheit muss in Zukunft vermehrt auf das Auftreten von Pankreatitiden geachtet werden. Etwaige günstige kardiovaskuläre Effekte sind derzeit Gegenstand prospektiver Studien.