Die chronische Wunde – Herausforderungen in der Behandlung
Ein Integritätsverlust der Haut und einer oder mehrerer darunter liegender Strukturen mit einer fehlenden Abheilung innerhalb von acht Wochen definiert eine chronische Wunde. Abgesehen von dieser zeitlich orientierten Definition gibt es Wunden, welche von Beginn an als chronisch anzusehen sind. Hierzu gehören unter anderem das diabetische Fußsyndrom, arterielle/venöse Ulzera oder Dekubitus.2
Warum wird eine Wunde chronisch?
Jede Wunde durchläuft die physiologischen Wundheilungsphasen. Nach der initialen Hämostase folgt die Exsudationsphase (Tag 1–3) mit Ablauf einer physiologischen Entzündung, dieser schließt sich die Proliferationsphase (Tag 4–7) mit Ausbildung von Granulationsgewebe an. In der abschließenden Reparationsphase (ab dem 8. Tag) erfolgt die Kollagensynthese mit Narbenbildung sowie Gewebemodellierung. Dieses komplexe System besteht aus einer Kaskade zellulärer und extrazellulärer Komponenten, die einer Regulation durch Zytokine, Wachstumsfaktoren und Mediatoren unterliegen. Eine Vielzahl pathogener Einflüsse kann zu einer Störung der Wundheilung führen und eine Wunde chronifizieren.3
Wundinfekte (≥ 105 Keime/g Gewebe) führen zu einer Verlängerung der Exsudationsphase sowie zu einer Verzögerung oder Verhinderung der Proliferationsphase und der Reparationsphase. Fremdkörper sowie körpereigenes Material (Knochensequester bei Osteomyelitis) dienen als Nährboden für Keime und bewirken wiederum eine lokale Infektion. Ödeme (phlebo-lymphatisch) verursachen durch Kompression kleiner Gefäße eine Minderperfusion und Hypoxie. Fehlende oder verminderte Oxygenierung reduziert die Fibroblastenstimulation (Proliferationsphase).4, 5
Systemisch beeinflussen ein höheres Lebensalter, Adipositas, psychischer Stress, Lifestyle (Nikotin-, Alkoholabusus, nutritive Defizite), Malignome und Medikamenteneinnahme (Kortikoide) die Wundheilung negativ. Weiters stören hereditäre Ursachen (Epidermolysis bullosa, Ehlers-Danlos-Syndrom, Marfan-Syndrom, Progerie, Homozystinurie) diese. Stoffwechselstörungen, allen voran Diabetes mellitus, können ebenso zu Wundheilungsstörungen führen. Aufgrund der Sensibilitätsstörung durch die diabetische Neuropathie kommt es zu vermehrten Verletzungen. Die Mikroangiopathie bringt eine verminderte Gewebsperfusion mit sich, zudem liegt eine gestörte zelluläre Immunabwehr mit fünffach erhöhtem Infektionsrisiko vor. Die Kollagensynthese wird durch die Beeinträchtigung des Vitamin-C-Transportes direkt reduziert, auch laufen Chemotaxis und Phagozytose verlangsamt ab.4–6
Diagnose und Therapie
Zur Diagnostik chronischer Wunden hat sich die ABCDE-Regel etabliert (Tab. 1).
Für eine erfolgreiche Therapie chronischer Wunden sind die Ursachenklärung und die Behandlung zugrunde liegender pathophysiologisch relevanter Erkrankungen beziehungsweise die Eliminierung von Störfaktoren unumgänglich. Parallel dazu erfolgt die stadiengerechte Lokaltherapie.
Stadiengerechte Lokaltherapie
Die Vorbereitung des Wundbettes ist essenziell, um eine chronische Wunde in eine aktive, heilende Wunde umzuwandeln. Die Wundheilung wird durch avitales Gewebe, Fremdkörper, Beläge und Detritus behindert, weshalb eine Abtragung bis zu intakten anatomischen Strukturen durchgeführt werden muss (chirurgisches Débridement). Dies beinhaltet die Wundreinigung, die Voraussetzung für eine optimale Wundbeurteilung und die Grundlage für einen Heilungserfolg ist. Man unterscheidet die aktive periodische Wundreinigung (APW), eine gezielte wiederkehrende mechanische Wundreinigung im Rahmen des Verbandwechsels, von der passiven periodischen Wundreinigung (PPW), dem beabsichtigten fortlaufenden Reinigungsprozess ohne Zerstörung intakten Granulationsgewebes, der unter dem Sekundärverband stattfindet (enzymatisch, autolytisch, biochirurgisch, osmotisch). Nach der Entfernung nekrotischen Gewebes wird versucht, in eine granulierende Wunde überzugehen.8 Als Orientierungshilfe zur phasengerechten Therapie dient das MOIST-Konzept (Tab. 2).
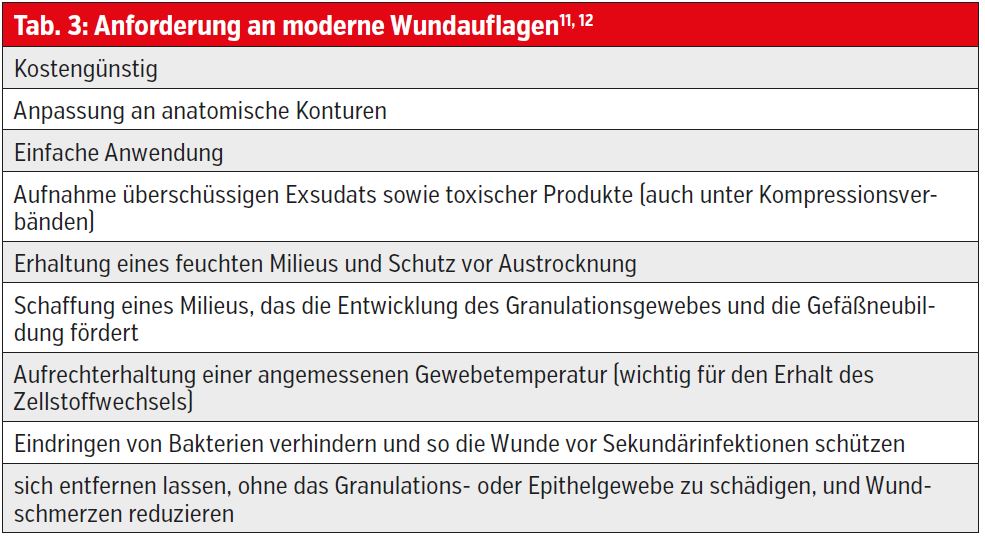
Als State of the Art gilt heute die an den Phasen der Wundheilung orientierte feuchte Wundbehandlung. Metaanalysen belegen ihren positiven Einfluss auf die Abheilungsraten chronischer Wunden.10 In chronischen Wunden finden sich im Exsudat auch wundheilungshemmende Substanzen, weshalb das Exsudatmanagement durch die angewandte Wundauflage von großer Bedeutung ist. Für die praktische Umsetzung einer modernen feuchten Wundbehandlung wird für einen Großteil der Patienten mit chronischen Wunden die Anwendung von Verbandstoffen empfohlen. Es existiert allerdings keine für jede Wunde geeignete optimale Wundauflage. Die korrekte Auswahl bedarf Erfahrung mit dem Produkt, Kenntnis über die Wundheilungsphasen und dadurch einen stadiengerechten Einsatz. Die Anforderungen an moderne Wundauflagen sind hoch (Tab. 3).
Fazit
- Die Behandlung chronischer Wunden stellt eine Herausforderung an den Behandler dar.
- Kenntnisse über die Wundheilungsphasen und mögliche Störfaktoren sowie über die Eigenschaften einsetzbarer Wundauflagen sind unumgänglich.
- Eine Ursachenabklärung und Mitbehandlung möglicher Störfaktoren sowie die Vorbereitung des Wundbettes sind essenziell für den Heilungserfolg.
Literatur
- Wundreport 2015.
- J. Dissemond, A. Bültemann, V. Gerber, B. Jäger, C. Münter, K. Kröger. Definitionen für die Wundbehandlung. Hautarzt. 2016, DOI: 10.1007/s00105-016-3761-y.
- P. Kujath, A. Michelsen. Wunden – von der Physiologie zum Verband. Deutsches Ärzteblatt CME Kompakt. 2009, 1(1).
- S. Guo, L. A. DiPietro. Factors Affecting Wound Healing. J Dent Res. 2010, 89(3): 219–229.
- Overview of Chronic Wounds. https://www.woundsource.com. 2018.
- S. Trainotti, M. Scheithauer. Phasen, Störungen und Förderung der Wundheilung. HNO – Springer Medizin Verlag. 2017, DOI: 10.1007/s00106-017-0381-5.
- Dissemond, J. ABCDE-Regel der Diagnostik chronischer Wunden. Journal der deutschen Dermatologischen Gesesllschaft. 2017, 15(7):732-734.
- D. Childs, A. Murthy. Overview of Wound Healing and Management. Surg Clin North Am. 2017, 97:189–207.
- J. Dissemond, B. Assenheimer, P. Engels, V. Gerber, K. Kröger, P. Kurz, S. Läuchli, S. Probst, K. Protz, J. Traber, S. Uttenweiler, R. Strohal. M.O.I.S.T. – ein Konzept für die Lokaltherapie. Journal of the German Society of Dermatology. 2017, 1610-0379/2017/1504.
- K. Heyer, M. Augustin, K. Protz, K. Herberger, C. Spehr, S.J. Rustenbach. Effectiveness of Advanced versus Conventional Wound Dressings on Healing of Chronic Wounds: Systematic Review and Meta-Analysis. Dermatology. 2013, 226(2):172–184.
- J. Dissemond, M. Augustin, S. A. Eming, T. George, T. Horn, S. Karrer, H. Schumann, M. Stücker. Moderne Wundtherapie – praktische Aspekte der lokalen, nichtinterventionellen Behandlung von Patienten mit chronischen Wunden. JDDG. 2015, DOI: 10.1111/ddg.12351.
- S. T. Tan, N. Winarto, R. Dosan, P. B. Aisyah. The Benefits Of Occlusive Dressings In Wound Healing. The Open Dermatology Journal. 2019, Bd. 13, 10.2174/1874372201913010027, 27-33.
- Kramer, A. Wundantiseptik-Evidenz, Wirkstoffauswahl und Perspektiven. Ars Medici. 2016, 9:419–426.
- S. K. Saikaly, A. Khachemoune. Honey and Wound Healing: An Update. American Journal of Clinical Dermatology. 2017, DOI: 10.1007/s40257-016-0247-8.
- https://www.wundwissen.info/ [Online].