Diabetes und Nierenerkrankung: Prävention und Therapie
Trotz zahlreicher Fortschritte im Diabetesmanagement ist die diabetische Nephropathie nach wie vor die häufigste Ursache einer terminalen Niereninsuffizienz und Dialysepflichtigkeit in den westlichen Industrieländern. Basierend auf Daten der NHANES-Population sind bis zu 40 % der Patienten mit Diabetes mellitus von einer chronischen Nierenerkrankung unterschiedlichen Ausmaßes betroffen, fast 25 % der Patienten entwickeln eine Nephropathie im CKD-Stadium G3 oder höher.1 In Österreich erhalten 0,3 % von geschätzten 600.000 Diabetespatienten eine Nierenersatztherapie.2 In den meisten europäischen Ländern sowie in den USA wurde in den letzten Jahren ein Rückgang der terminalen Niereninsuffizienz beobachtet. Die Inzidenz der dialysepflichtigen Nierenerkrankung bei Diabetes mellitus konnte laut US-amerikanischen Daten von 1990 bis 2010 um 28 % abgesenkt werden, im Vergleich zur Reduktion der makrovaskulären Ereignisse war dieser Rückgang jedoch am geringsten ausgeprägt.3
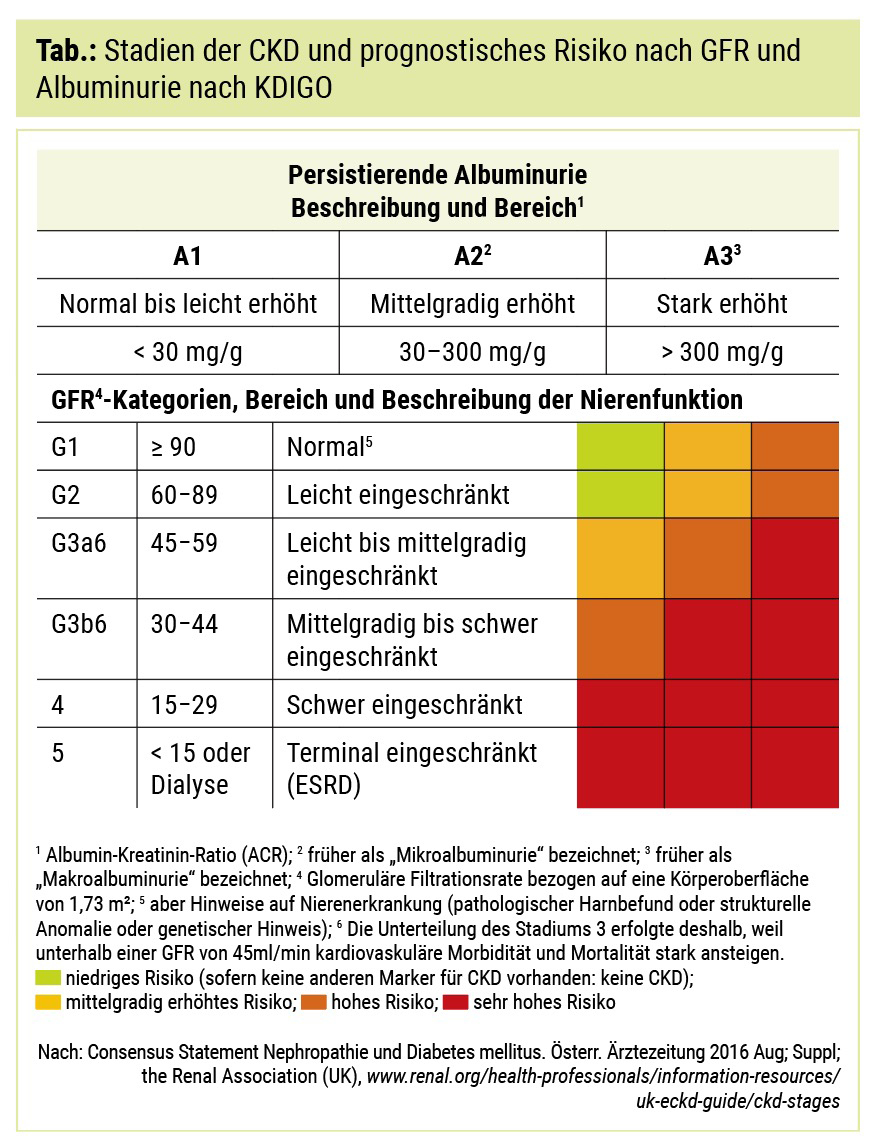
Die KDIGO-Einteilung der chronischen Nierenerkrankung je nach Ausmaß der Albuminurie und Einschränkung der Nierenfunktion sowie deren Auswirkung auf die kardiovaskuläre Morbidität und Mortalität wird in der Tabelle dargestellt. Eine rechtzeitige Diagnose der diabetischen Nephropathie ist nicht nur für die Behandlung dieser Erkrankung, sondern auch für die kardiovaskuläre Risikoabschätzung essenziell. Insbesondere ab einem CKD-Stadium G3b (entsprechend einer eGFR unter 45 ml/min/KO) steigt die Wahrscheinlichkeit kardiovaskulärer Ereignisse stark an,4 sodass diese Patienten auch bezüglich weiterer Risikofaktoren strikt überwacht und therapiert werden sollten.
Daher wird bei Neudiagnose des Diabetes mellitus Typ 2 sowie bei unauffälligem Verlauf empfohlen, zumindest einmal jährlich nach mikro- und makrovaskulären Folgeschäden zu fahnden. Für das Screening der diabetischen Nephropathie werden die Bestimmung der Albumin-Kreatinin-Ratio im Harn sowie des Kreatinins im Serum inkl. eGFR-Berechnung mit der MDRD- und CKD-EPI-Formel herangezogen. Ein positiver Albuminbefund im Harn sollte kurzfristig kontrolliert werden, da intermittierend positive Ergebnisse auch z. B. bei Harnwegsinfekten, Fieber, ausgeprägter Hyperglykämie, erhöhtem Blutdruck oder nach körperlicher Anstrengung auftreten können.
Rolle der Hyperglykämie und zusätzliche renale Effekte
Zu einem wesentlichen Teil wird die Entwicklung einer diabetischen Nierenerkrankung durch das Ausmaß der Hyperglykämie bestimmt. In der Pathophysiologie der mikrovaskulären Folgeschäden spielen unter anderem Hyperglykämie-getriggerte Störungen der Endothelfunktion, der Gefäßregeneration und Angiogenese sowie inflammatorische Prozesse und direkte vaskuläre Schädigungen durch oxidativen Stress oder AGEs (Advanced Glycated Endproducts) eine Rolle.5
Ein HbA1c im Zielbereich als primäres Ziel des Diabetesmanagements kann somit auch das Risiko dieser mikrovaskulären Veränderungen verringern. Prävention und Therapie der diabetischen Nierenerkrankung beinhalten folgerichtig eine möglichst gute glykämische Kontrolle, die Behandlung weiterer Risikofaktoren (v. a. Rauchen, Dyslipidämie, arterielle Hypertonie, Übergewicht) und den Einsatz ausgewählter Antidiabetika mit positiven substanzspezifischen Effekten.
Im Folgenden wird der Fokus abseits der Blutzuckereinstellung auf zusätzliche renale Effekte der antidiabetischen Medikation liegen. In den letzten Jahren standen häufig die beeindruckenden kardiovaskulären Daten insbesondere von SGLT2-Hemmern und GLP-1-Analoga im Mittelpunkt. Die positiven Ergebnisse der kardiovaskulären Outcomestudien führten rasch zu entsprechenden Änderungen der nationalen und internationalen Therapieleitlinien, die Resultate meist sekundärer renaler Endpunkte sorgten für zusätzliche Aufmerksamkeit. Basierend auf diesen Erkenntnissen sollte laut ÖDG-Therapieleitlinien bei Vorliegen einer chronischen Nierenerkrankung (eGFR 30–60 ml/min/KO oder Albumin-Kreatinin-Ratio > 30 mg/g, insbesondere > 300mg/g) ein SGLT2-Hemmer mit bewiesener Verlangsamung der CKD-Progression bevorzugt werden. Sollte der Einsatz eines SGLT2-Hemmers aufgrund zu eingeschränkter eGFR oder durch Unverträglichkeit nicht möglich sein, so wird alternativ ein GLP-1-Analogon mit kardiovaskulärem Benefit empfohlen (Abb.).
SGLT2-Hemmer: Neben dem positiven Effekt auf die glykämische Kontrolle durch Hemmung der Glukoserückabsorption im proximalen Tubulus haben SGLT2-Hemmer auch direkte günstige renale Effekte. In der Literatur finden sich neben Gewichtsreduktion und Blutdrucksenkung durch SGLT2-Hemmer auch eine Verringerung des intraglomerulären Drucks und des oxidativen Stresses sowie günstige Effekte auf Inflammation und Angiotensinogenspiegel.
Bereits in den kardiovaskulären Outcomestudien der SGLT2-Hemmer Empagliflozin (EMPA REG-OUTCOME), Dapagliflozin (DECLARE) und Canagliflozin (CANVAS) wurden renale Komplikationen und der Verlauf einer chronischen Nierenerkrankung als sekundäre Endpunkte definiert und ausgewertet. Diese kombinierten renalen Endpunkte zeigten übereinstimmend einen positiven Effekt, sind jedoch aufgrund unterschiedlicher Populationen, Studiendesigns und Definitionen der renalen Endpunkte nicht direkt vergleichbar.
Eine entsprechende Metaanalyse dieser 3 Studien zeigte eine konsistente Reduktion der Wahrscheinlichkeit für das Auftreten einer Verschlechterung der Nierenfunktion, einer terminalen Niereninsuffizienz oder eines renalen Todes um 44 %.6 Diese ermutigenden Analysen führten zur Durchführung weiterer Studien mit Fokus auf eine bereits renal vorerkrankte Diabetespopulation. Die CREDENCE-Studie untersuchte die Wirkung von Canagliflozin versus Placebo bei Patienten mit Diabetes mellitus Typ 2 und chronischer Nierenerkrankung (Albumin-Kreatinin-Ratio 300–5.000 mg/g und eGFR 30 bis 90 ml/min/KO) auf die Kombination aus Notwendigkeit einer Dialyse oder Nierentransplantation oder Entwicklung einer anhaltenden eGFR < 15 ml/min/KO. Dieser primäre Endpunkt konnte in solch einer Hochrisikogruppe durch Canagliflozin um 30 % (HR 0,70; 95%-KI 0,59–0,82) reduziert werden.7
In weiterer Folge wurde in der DAPA-CKD-Studie die Wirkung von Dapagliflozin bei über 4.300 Patienten mit einer chronischen Nierenerkrankung (eGFR 25–75 ml/min/KO und Albumin-Kreatinin-Ratio 200–5.000 mg/g) mit und ohne Diabetes mellitus untersucht. Der kombinierte primäre Endpunkt (Abnahme der eGFR um mindestens 50 %, terminale Niereninsuffizienz oder Tod aufgrund einer kardiovaskulären oder renalen Ursache) wurde mit Canagliflozin um 39 % (HR 0,61; 95%-KI 0,51–0,72) reduziert, dieser positive Effekt war unabhängig vom Vorliegen eines Diabetes mellitus.8
Auch für Empagliflozin wurden rezent positive renale Effekte unabhängig vom Diabetesstatus beschrieben. In EMPEROR-Reduced konnte bei Patienten mit einer chronischen Herzinsuffizienz mit reduzierter Pumpfunktion unter Empagliflozin versus Placebo eine langsamere jährliche Verschlechterung der eGFR (–0,55 vs. –2,28 ml/min/KO pro Jahr, p < 0,001) dokumentiert werden.9
Diese durchwegs positiven Daten stehen teilweise noch im Widerspruch zu den Fachinformationen der Substanzen, welche den Einsatz der SGLT2-Hemmer bei einer GFR < 45 ml/min/KO limitieren. Entsprechende Zulassungsänderungen mit einer Indikationserweiterung zur Behandlung der chronischen Niereninsuffizienz werden jedoch in Kürze erwartet und machen den Weg frei für einen zielgerichteten Einsatz dieser Substanzen in noch breiterer Indikation.
GLP-1-Analoga: Während die DPP-IV-Hemmer in ihren kardiovaskulären Outcomestudien neutrale Ergebnisse im Sinne eines sicheren Einsatzes zeigten, liegen für Liraglutid (LEADER), Semaglutid (SUSTAIN 6) und Dulaglutid (REWIND) positive renale Daten vor. Das Risiko kombinierter renaler Endpunkte konnte in diesen Studien um 15–36 % gesenkt werden, ein direkter Vergleich ist wiederum bei relevanten Unterschieden in der Auswahl der Endpunkte, des Studiendesigns und der untersuchten Populationen nicht sinnvoll.
Resümee
Die diskutierten günstigen kardiorenalen Effekte moderner Antidiabetika haben bereits zu Aktualisierungen der Therapieleitlinien des Diabetes mellitus Typ 2 geführt. SGLT2-Hemmer und GLP-1-Analoga haben das Potenzial, neben kardiovaskulärer Mortalität und Morbidität auch den Verlauf der chronischen Nierenerkrankung positiv zu beeinflussen. Diese Daten sind in Zukunft insbesondere bei Therapieentscheidungen im Hochrisikokollektiv mit bestehenden kardiovaskulären Erkrankungen, einem hohen Risiko für eine solche atherosklerotische Erkrankung, mit einer bestehenden Herzinsuffizienz oder einer bekannten chronischen Nierenerkrankung zwingend zu berücksichtigen.
- Koro CE et al., Clin Ther 2009; 31: 2608–17
- Prischl FC et al., Nephrol Dial Transplant 2015; 30(11): 1920–7
- Gregg EW et al., N Engl J Med 2014; 370: 1514–23
- Go AS et al., N Engl J Med 2004; 351: 1296–305
- Madonna R et al., Vascular Pharmacol 2017; 90: 1–7
- Zelniker TA et al., Lancet 2019; 393(10166): 31–9
- Perkovic V et al., N Engl J Med 2019; 380(24): 2295–306
- Heerspink HJL et al., N Engl J Med 2020; 383(15): 1436–46
- Packer M et al., N Engl J Med 2020; 383(15): 1413–24