Komplikation der Antitumortherapie – Osteoporose bei der jungen gynäkologischen Patientin
Dn ie Osteoporose stellt eine systemische Skeletterkrankung dar, definiert durch eine niedrige Knochenmasse und Störung der Mikroarchitektur des Knochengewebes mit konsekutiver Erhöhung des Frakturrisikos. Frauen erkranken 4–5-mal häufiger als Männer, wobei das Lebenszeitrisiko, eine Osteoporose-bedingte Wirbelkörperfraktur zu erleiden, 16 % für Frauen bzw. 5 % für Männer beträgt. Weltweit sind in etwa 200 Mio. Frauen von Osteoporose betroffen; in Österreich leiden ca. 740.000 Personen (617.000 Frauen) an Osteoporose. Unter Annahme eines Gauß’schen Verteilungsmusters der Knochendichte in der Gesamtbevölkerung ist davon auszugehen, dass ca. 0,5 % junger Erwachsener eine nach WHO-Kriterien definierte Abnahme der Knochendichte aufweisen.
Knochenwachstum im Laufe des Lebens
Vor der Pubertät erfolgt die Regulierung des Knochenwachstums sexualhormonunabhängig über genetische Prädisposition, das Kalzium-Vitamin-D-System, Ernährung und physikalische Belastung. Ab der Pubertät erfolgt eine sexuelle Differenzierung des Skeletts und die Sexualhormone Östradiol bzw. Testosteron determinieren den Knochenaufbau, wodurch die Spitzenknochenmasse (PBM) im Mittel zwischen dem 25.–35. Lebensjahr erreicht wird. Mit dem Eintritt in die Menopause setzt schließlich bedingt durch eine physiologische Östradioldeprivation ein zunehmender Knochenabbau ein (postmenopausale [Typ I] Osteoporose). Demgegenüber scheint eine prämenopausal auftretende Osteoporose (idiopathische Osteoporose des jungen Erwachsenen) eher durch eine A-priori-Reduktion der PBM determiniert zu werden, wobei neben den bereits oben angeführten Faktoren sich zudem ein niedriger BMI, eine Menarche nach dem 15. Lj. und der Konsum von Genussmitteln negativ auf die PBM auswirken. Dieser frühen, idiopathischen Osteoporose (ca. 50 % aller Osteoporoseerkrankungen in der Adoleszenz) stehen verschiedene Formen der sekundären Osteoporose gegenüber (Tab. 1).
Osteoporoserisiko bei gynäkoonkologischen Patientinnen
Osteoporose induziert durch Hypogonadismus: Östradiol beeinflusst die Knochenresorption über eine Hemmung der Osteoklastenproliferation basierend auf einer Interaktion mit Zytokinen (IL-1, IL-6, TNF, Osteoprotegerin), welche ihrerseits die Differenzierung von Osteoklastenprogenitoren mediieren. Östradiolmangel induziert eine Frequenzerhöhung des Knochenumbaus und eine verstärkte Osteoklastenproliferation. Eine kompensatorische Akzeleration des Knochenaufbaus bleibt jedoch insuffizient, da infolge des Östradiolmangels die Aktivierung von Wachstumsfaktoren (TGF-_, IGF-1) ausbleibt. Indirekt führt Östradiolmangel zu einer Abnahme der Muskelkraft und einem biomechanisch basierten Knochenabbau.
Prämenopausale Patientinnen nach ovarieller Ablation – sei es chirurgisch, zytotoxisch oder unter GnRH-Analoga – verlieren innerhalb des ersten Behandlungsjahrs 13 % ihrer PBM, zudem induziert Chemotherapie mit Cyclophosphamid, Fluorouracil, Anthrazyklinen, Methotrexat u. a. innerhalb eines Jahres bei 63–96 % prämenopausaler Mammakarzinompatientinnen eine ovarielle Dysfunktion. In Tierversuchen wurde für Cyclophosphamid neben einer dosisabhängigen, direkten Schädigung der Primordial- und Antralfollikel auch die Zerstörung der für die Östradiolkonversion wichtigen Granulosazellen gezeigt. Das Ausmaß der ovariellen Schädigung ist abhängig vom Alter der Patientin, der kumulativen Dosis und der Therapiedauer. Eine Amenorrhö um das 30. Lj. bleibt meist dauerhaft bestehen.
Osteoporoserisiko unter endokriner Therapie:
- Die kontinuierliche Zufuhr von GnRH-Analoga führt zur Downregulation von GnRH-Rezeptoren, einer Inhibition der LH-Sekretion und damit zur Ovarialinsuffizienz. Innerhalb der ersten 6 Monate weisen mehr als 95 % der Patientinnen eine sekundäre Amenorrhö und Abnahme der Knochendichte auf. In der ZEBRA-Studie, welche den therapeutischen Effekt einer 2-jährigen Goserelin- Therapie gegenüber 6 Zyklen CMF beim Mammakarzinom (prämenopausal) untersuchte, wurde in der GnRH-Gruppe eine signifikant höhere Abnahme der Knochendichte verzeichnet (–10,5 % vs. –6,5 % Lendenwirbelsäule; –6,4 % vs. –4,5 % Femurhals). Ein Jahr nach Therapieende zeigte sich jedoch in der Gruppe der GnRH-Behandelten im Vergleich zur CMFGruppe eine leichte Erholung der Knochendichte.
- Tamoxifen (TAM), die zweite Säule der endokrinen Therapie des Mammakarzinoms, bewirkt in Abhängigkeit des Gewebes und des prätherapeutisch bestehenden Östradiolspiegels sowohl antagonistische als auch partiell agonistische Effekte. Während postmenopausale Patientinnen nach 2-jähriger TAM-Einnahme eine Zunahme der mittleren Knochendichte aufzeigten, wiesen gesunde prämenopausale Patientinnen unter TAM eine signifikante Abnahme der Knochendichte (1,44 % pro Jahr) auf.
- Bei Kombination von GnRH/Aromatasehemmer (Anastrozol) zeigten die Ergebnisse der ABCSG-12-Studie zusätzliche negative Einflüsse verglichen mit GnRH/TAM. GnRH/TAM für 3 Jahre führte zu einer Knochendichtereduktion um 11,6 % in der Lendenwirbelsäule, GnRH/Anastrozol sogar zu einer 17,3%igen Reduktion. Der Knochendichteabfall konnte jedoch durch die Gabe einer präventiven i. v. Bisphosphonattherapie (4 mg/6 Mo.) weitgehend kompensiert werden.
Hormonunabhängiges Osteoporoserisiko:
- Methotrexat-(MTX)-Osteopathie: Der negative Einfluss von Hochdosis-MTX (ab 1 g/m2) beruht wahrscheinlich auf einer Reduktion des Knochenaufbaus bei gleichzeitig gesteigerter Knochenresorption. Im Tierversuch konnte gezeigt werden, dass MTX eine verminderte Osteoblastenrekrutierung aus dem Precursor-Pool induziert. Demgegenüber scheint MTX weniger toxisch auf Osteoklasten-Precursor-Zellen zu wirken, was einen gesteigerten Knochenabbau erklärt. Bei ALL-Patienten konnte gezeigt werden, dass eine Langzeit-MTX-Therapie zu schwerer Osteoporose und erhöhtem Frakturrisiko führt.
- Glukokortikoid-induzierte Osteoporose (GiO): Die tägliche Einnahme von 7,5–15 mg Prednison über 3 Monate führt zu einer signifikanten Abnahme des trabekulären Knochens. Im Gegensatz zu einer durch Östradioldefizienz bedingten Osteoporose basiert eine GiO auf einer Inhibition der Osteoblas – tenaktivität. Daneben scheinen indirekte Effekte wie Abnahme der Kazium-Resorption und konsekutiver, sekundärer Hyperparathyreoidismus eine Induktion der Knochenresorption zu bewirken. Obwohl der Knochenverlust unter Glukokortikoidtherapie im ersten Jahr am höchsten ist (mehr als 20 % in den ersten 6–12 Monaten), scheint das Osteoporoserisiko von der Dauer und Kontinuität der Applikation abhängig zu sein. Andererseits reduzieren Glukokortikoide durch die Therapie einer bestehenden Knochenmarkinfiltration (beim Mammakarzinom, multiplen Myelom u. a.) schädigende Einflüsse auf die Knochenarchitektur.
- Malnutrition/Malabsorption: Tumor- oder therapiebedingte Störungen der Kalzium- und Vitamin-D-Resorption, welche nach ausgedehnter Dünndarmresektion oder als Folge einer chronischen Strahlenenteritis auftreten, können Mischformen einer Osteoporose/Osteomalazie induzieren.
Therapeutische Ansätze
Das Problem der Osteoporose wird bei Tumorpatientinnen häufig unterschätzt. Allgemeine Empfehlungen für prä- und postmenopausale Patientinnen sind vergleichbar. Vor Therapiebeginn sollten gemäß den ASCO-Richtlinien (2003) eine Erhebung von Risikofaktoren und eine Knochendichtemessung nach der DXA-Methode erfolgen.
Allgemeine Präventionsmaßnahmen umfassen eine ausreichende körperliche Betätigung, suffiziente Aufnahme von Kalzium (1.000–1.500 mg/die) und Vitamin D (400–800 IU/die), eine Optimierung des Körpergewichts und die Vermeidung von Nikotin und Alkohol.
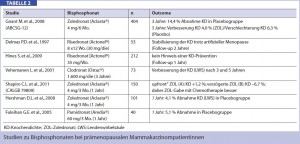
Die Anwendung von Bisphosphonaten zur Therapie einer bestehenden Osteopenie (T-Score –1,0 bis –2,5 SD) oder einer manifesten Osteoporose (T-Score < –2,5 SD) ist zu empfehlen. Im Bezug auf die Prävention einer therapieinduzierten Osteoporose bei der prämenopausalen Patientin ist die Datenlage zwar vielversprechend, jedoch teilweise inkongruent (Tab. 2). Einer i. v. Applikation ist aus Gründen der niedrigen Compliance oraler Bisphosphonattherapien (60–70 % Therapieabbrüche innerhalb eines Jahres) der Vorzug zu geben.